Spectrophotométrie UV-Visible en Pharmacie : Cours Complet pour les Étudiants en 3ème Année
Introduction : Pourquoi la Spectrophotométrie UV-Visible est Indispensable en Pharmacie ?
La spectrophotométrie UV-Visible est l’une des techniques analytiques les plus puissantes et les plus utilisées dans les laboratoires pharmaceutiques. Simple à mettre en œuvre, rapide, précise et non destructive, elle constitue un pilier incontournable du contrôle qualité des médicaments.
Plus de 90 % des analyses médicales s’appuient sur la spectroscopie d’absorption UV-Visible, ce qui témoigne de son importance capitale dans les sciences de la santé.
La spectrophotométrie UV-Vis est citée dans plus de 500 monographies de la Pharmacopée Européenne, allant des identifications qualitatives aux dosages quantitatifs des principes actifs.
Dans ce cours, vous découvrirez le principe physique de la méthode, les types de transitions électroniques, les chromophores essentiels, et tous les facteurs qui influencent les spectres d’absorption — le tout avec des exemples concrets appliqués à la pharmacie.
1. Introduction : Bases de la Méthode
La spectrophotométrie UV-Visible repose sur l’étude des modifications de la structure électronique des molécules lorsqu’elles interagissent avec le rayonnement lumineux.
De nombreux principes actifs présents dans les médicaments possèdent dans leur structure des groupements chimiques qui absorbent dans l’ultraviolet et peuvent ainsi être dosés avec précision.
La technique est inscrite dans toutes les Pharmacopées mondiales. Sa popularité s’explique par trois atouts majeurs :
- Sa simplicité d’utilisation au quotidien
- Sa flexibilité grâce à un large choix d’instruments adaptés
- Sa rapidité : un résultat en quelques secondes
2. Principe Physique : Comment Fonctionne la Transition Électronique ?
2.1 Le Mécanisme d’Absorption
Lorsqu’une molécule est irradiée par de la lumière ultraviolette ou visible, un électron de valence peut absorber cette énergie et passer de l’état fondamental (EF) à un état excité (EE).
Deux types d’électrons sont impliqués dans ce phénomène :
- Les électrons de liaison (simples et multiples)
- Les électrons non liants (paires libres, notés n)
La différence d’énergie entre les deux états correspond à la fréquence de la radiation :
ΔE = hν
(où h est la constante de Planck et ν la fréquence de la radiation)
2.2 Spectre de Bande : Pourquoi des Bandes et Non des Raies ?
Contrairement aux atomes, les molécules produisent des spectres en bandes larges. Cela s’explique parce qu’une transition électronique induit simultanément de nombreuses transitions vibrationnelles et rotationnelles.
Après avoir absorbé l’énergie, la molécule la restitue le plus souvent sous forme de chaleur : c’est la relaxation non rayonnante.
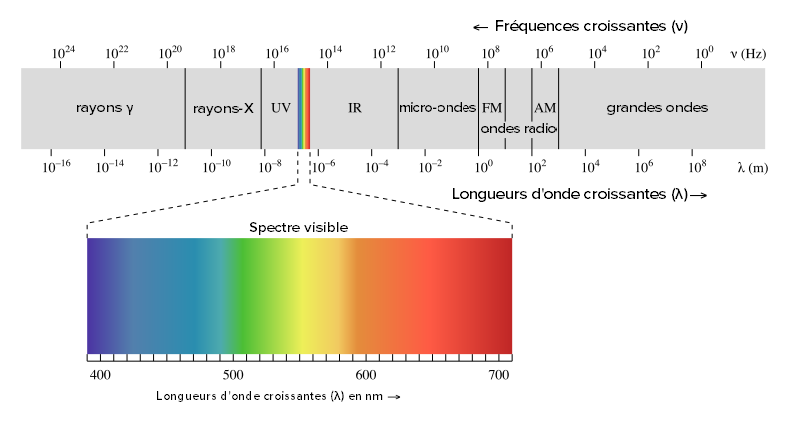
3. Les Régions du Spectre UV-Visible
Le domaine UV-Visible se divise en trois plages distinctes :
| Région | Plage de longueurs d’onde |
|---|---|
| UV lointain | 185 – 200 nm |
| UV proche | 200 – 400 nm |
| Visible | 400 – 800 nm |
À retenir pour les examens : La région la plus couramment utilisée en analyse pharmaceutique est l’UV proche (200 – 400 nm). En dessous de 200 nm, l’air lui-même absorbe le rayonnement, rendant les mesures impossibles sans travailler sous vide.
4. Terminologie Essentielle : Chromophore et Auxochrome
Deux notions clés structurent toute l’analyse des spectres UV-Visible :
4.1 Le Chromophore
Un chromophore est un groupe insaturé covalent responsable de l’absorption électronique.
Exemples courants en pharmacie :
- La double liaison carbone-carbone C=C
- La fonction carbonyle C=O
- Le groupement nitro NO₂
4.2 L’Auxochrome
Un auxochrome est un groupe saturé portant des électrons libres qui, lorsqu’il est lié à un chromophore, modifie les caractéristiques d’absorption de ce dernier.
Exemples : -OH, -NH₂, -Cl
L’auxochrome en lui-même n’absorbe pas dans l’UV, mais il décale et intensifie les bandes du chromophore adjacent — un effet crucial dans l’analyse structurale des médicaments.
5. Les Quatre Types de Transitions Électroniques
Les transitions électroniques se classifient selon les orbitales moléculaires impliquées :
5.1 Transition σ → σ*
- Électrons concernés : liaisons C-C dans les hydrocarbures saturés
- Domaine d’absorption : ≈ 130 nm (UV lointain, inaccessible en pratique)
- Exemple : Hexane, λmax = 135 nm
5.2 Transition n → σ*
- Électrons concernés : hétéroatomes porteurs de liaisons saturées (C-O, C-N, C-S)
- Domaine d’absorption : 150 – 250 nm
- Exemple : Méthanol, λmax = 210 nm, ε = 50 L.mol⁻¹.cm⁻¹
5.3 Transition n → π*
- Électrons concernés : hétéroatomes porteurs de liaisons insaturées (C=O)
- Domaine d’absorption : 270 – 290 nm
- Exemple : Éthanal, λmax = 293 nm, ε = 12 L.mol⁻¹.cm⁻¹
5.4 Transition π → π*
- Électrons concernés : liaisons insaturées (C=C, C=O conjugués)
- Domaine d’absorption : à partir de 170 nm pour les composés éthyléniques
- Exemple : Éthylène, λmax = 165 nm, ε = 16 000 L.mol⁻¹.cm⁻¹
Astuce mnémotechnique : Plus l’énergie de la transition est faible, plus la longueur d’onde est grande. La transition n → π* est la moins énergétique, donc la plus bathochrome.
6. Nomenclature des Bandes d’Absorption : La Classification de BURAWOY
La notation la plus utilisée en pratique est celle d’A. BURAWOY, qui distingue quatre types de bandes :
| Bande | Transition | Origine | Particularité |
|---|---|---|---|
| R (radicalaire) | n → π* | Chromophores isolés (C=O, NO₂) | εmax faible < 100 |
| K (conjuguée) | π → π* | Systèmes conjugués (diène, styrène) | εmax élevé > 10 000 |
| B (benzénoïde) | π → π* | Molécules aromatiques | Structure fine, ε < 1000 |
| E (éthylénique) | π → π* | Structures aromatiques | E1 (180 nm) et E2 (200 nm) |
7. Les Principaux Chromophores en Chimie Pharmaceutique
7.1 Le Chromophore Éthylénique
Le double lien C=C isolé absorbe dans l’UV lointain (λmax = 165 nm) et est peu accessible en pratique. Mais lorsque plusieurs doubles liaisons sont conjuguées, le phénomène change radicalement.
Effet de la conjugaison :
Dans le butadiène, la conjugaison des deux doubles liaisons crée de nouveaux niveaux d’énergie. Le résultat est un double effet :
- Effet bathochrome : déplacement de l’absorption vers les grandes longueurs d’onde
- Effet hyperchrome : augmentation de l’intensité d’absorption (εmax)
Ce principe est essentiel pour comprendre l’absorption des médicaments à structure polyénique (vitamine A, β-carotène, tétracyclines…).
7.2 Le Chromophore Carbonyle (C=O)
La fonction carbonyle est l’un des chromophores les plus importants en pharmacie. Elle présente trois types de transitions :
- n → σ* : λmax ≈ 190 nm
- π → π* : λmax ≈ 150 nm (intense)
- n → π* : λmax = 270 – 300 nm (bande R, faible intensité)
Exemples concrets :
| Composé | λmax (nm) | εmax | Solvant |
|---|---|---|---|
| Acétone | 279 | 15 | Hexane |
| Acétaldéhyde | 293 | 11,8 | Hexane |
| Acide acétique | 204 | 4 | Éthanol |
7.3 Le Chromophore Benzénique
Le noyau benzénique est omniprésent dans les médicaments (paracétamol, aspirine, ibuprofène…). Il présente trois bandes caractéristiques :
| Bande | λmax (nm) | εmax (L.mol⁻¹.cm⁻¹) | Nature |
|---|---|---|---|
| K (E1) | 184 | 60 000 | Transition permise |
| K (E2) | 204 | 7 900 | Transition interdite |
| B | 256 | 200 | Bande de structure fine |
Application pratique : Le principe actif de l’ibuprofène peut être analysé par spectrophotométrie UV-Vis en déterminant le coefficient d’extinction à 264 et 273 nm. Selon la Pharmacopée américaine (USP), l’écart entre l’étalon et l’échantillon doit être inférieur à 3,0 %.

8. Les Effets Spectraux : Bathochrome, Hypsochrome, Hyperchrome, Hypochrome
Ces quatre termes reviennent constamment dans l’étude des spectres. Voici comment les retenir :
| Effet | Signification | Déplacement |
|---|---|---|
| Bathochrome | “Red shift” | λmax augmente → vers le rouge |
| Hypsochrome | “Blue shift” | λmax diminue → vers le bleu |
| Hyperchrome | Intensification | εmax augmente |
| Hypochrome | Atténuation | εmax diminue |
Ces effets sont causés par les substituants, le solvant, le pH ou les effets stériques.
9. Facteurs Influençant les Spectres d’Absorption
9.1 Influence des Substituants
Groupes alkyles : Ils provoquent un léger effet bathochrome sur la bande B du benzène, via l’effet inductif positif (donneur d’électrons).
Groupes auxochromes (-OH, -NH₂) : Ils engendrent un fort effet bathochrome-hyperchrome sur les bandes B et E, grâce à la conjugaison avec le noyau aromatique.
Groupes électroattracteurs (-NO₂, -COOH, -NH₃⁺) : Ils induisent un effet hypsochrome par abaissement du niveau énergétique de l’état excité π*.
9.2 Effets Stériques
La géométrie moléculaire peut perturber profondément l’absorption UV :
Empêchement de rotation :
Dans le 2,2′-diméthylbiphényle, les deux méthyles empêchent la rotation libre autour de la liaison centrale. La coplaneité des deux cycles est réduite, ce qui diminue la conjugaison → effet hypsochrome (λmax passe de 256 nm à 228 nm).
Isomérie cis-trans :
| Isomère | λmax (nm) | εmax |
|---|---|---|
| Trans-stilbène | 295 nm | 2 500 |
| Cis-stilbène | 283 nm | 12 300 |
Dans le cis-stilbène, l’encombrement stérique brise la coplaneité → diminution de la conjugaison → effet hypsochrome et modification de l’intensité.
9.3 Influence du Solvant
Le choix du solvant est déterminant. Chaque solvant possède une limite d’utilisation (cut-off point) en dessous de laquelle il absorbe lui-même le rayonnement et perturbe la mesure :
| Solvant | Limite (nm) |
|---|---|
| Eau | 205 |
| Méthanol | 210 |
| Acétonitrile | 210 |
| Dichlorométhane | 235 |
| Acétone | 330 |
En solvant polaire, deux effets opposés se produisent :
- Pour les transitions π → π* (bande K) : effet bathochrome (stabilisation de l’état excité)
- Pour les transitions n → π* (bande R) : effet hypsochrome (les liaisons hydrogène stabilisent l’état fondamental n)
Remarque importante pour la CLHP : La plupart des détecteurs HPLC sont des spectrophotomètres UV-Visible. Le cut-off du solvant doit impérativement être pris en compte dans le choix de la phase mobile.
9.4 Influence du pH
Le pH modifie l’état d’ionisation des molécules et change leurs propriétés d’absorption.
Exemple du phénol :
- Forme moléculaire (milieu acide) → λmax faible
- Forme ionisée phénolate (milieu basique) → effet bathochrome-hyperchrome marqué
Exemple des amines :
- Amine libre R-NH₂ → absorption normale
- Forme protonée R-NH₃⁺ → effet hypsochrome (la paire libre n est engagée dans la liaison N-H)
10. Applications Concrètes en Pharmacie et Industrie
La spectroscopie UV-Visible est utilisée pour la détermination des principes actifs dans les médicaments et cosmétiques, ainsi que pour le contrôle qualité en vérifiant la pureté des substances et leur conformité aux spécifications réglementaires.
Voici les applications les plus fréquentes :
En contrôle qualité pharmaceutique :
- Dosage des antibiotiques, vitamines, analgésiques
- Vérification de la concentration des principes actifs
- Détection des produits de dégradation
En biologie moléculaire :
- Quantification de l’ADN à 260 nm
- Dosage des protéines à 280 nm
- Le rapport A260/A280 permet d’évaluer la pureté des extractions
Couplée à d’autres techniques : La spectroscopie UV-Visible peut être associée à la CLHP (Chromatographie Liquide Haute Performance) pour analyser des mélanges complexes, permettant le dosage des flavonoïdes, antibiotiques ou vitamines après séparation chromatographique.
La Pharmacopée Européenne (10ème édition, en vigueur depuis janvier 2020) couvre désormais non seulement les mesures classiques en cuve, mais aussi les applications intégrées associant un détecteur UV-Visible et un système chromatographique, ainsi que l’utilisation dans le contrôle analytique des procédés (PAT).

Conclusion : Ce qu’il Faut Retenir pour vos Examens
La spectrophotométrie UV-Visible est une technique analytique centrale en pharmacie. Voici les points clés à maîtriser absolument :
- Le principe : une transition électronique d’un état fondamental vers un état excité sous l’effet d’un rayonnement UV ou visible
- Les 4 transitions : σ→σ*, n→σ*, n→π*, π→π* — chacune avec son domaine d’absorption spécifique
- Les chromophores essentiels : C=C éthylénique, C=O carbonyle, noyau benzénique
- La nomenclature de Burawoy : bandes R, K, B, E
- Les effets spectraux : bathochrome, hypsochrome, hyperchrome, hypochrome
- Les facteurs d’influence : substituants, stéréochimie, solvant, pH
- Les applications pratiques : dosage des principes actifs, contrôle qualité, CLHP-UV
Conseil méthodologique : Pour chaque molécule étudiée, identifiez d’abord ses chromophores, puis déterminez les effets des substituants et du solvant sur les bandes d’absorption. Cette démarche systématique vous permettra de prédire et d’interpréter tout spectre UV-Visible.