Spectroscopie Atomique : Absorption et Émission — Guide Complet pour les Étudiants en Pharmacie
La spectroscopie atomique est l’une des techniques analytiques les plus puissantes en chimie pharmaceutique. Maîtriser ses principes, c’est acquérir un outil indispensable pour le dosage des métaux traces dans les médicaments, le contrôle qualité et le respect des normes de la Pharmacopée Européenne.
Dans cet article, vous trouverez une synthèse complète et structurée de la spectroscopie d’absorption atomique (SAA) et de la spectroscopie d’émission atomique (SEA), avec des exemples concrets, des schémas de principe et des applications directement issues du terrain pharmaceutique.

I. Qu’est-ce que la Spectroscopie Atomique ?
La spectroscopie atomique est une méthode d’analyse quantitative et qualitative basée sur les interactions entre la matière et le rayonnement électromagnétique.
Elle permet de doser plus de 70 éléments chimiques, souvent à l’état de traces (concentrations de l’ordre du ppb), ce qui en fait une technique de choix pour l’analyse des métaux dans les matrices biologiques, environnementales et pharmaceutiques.
Son fondement théorique repose sur la règle de Kirchhoff :
« Un corps soumis à certaines conditions d’excitation ne peut émettre que les radiations qu’il est susceptible d’absorber dans les mêmes conditions. »
Autrement dit, chaque élément possède un spectre d’absorption et d’émission qui lui est propre — une véritable empreinte spectrale.
Absorption vs Émission : quelle différence ?
- En absorption atomique (SAA) : un atome à l’état fondamental absorbe un photon et passe à l’état excité. On mesure la lumière absorbée.
- En émission atomique (SEA) : un atome excité retourne à l’état fondamental en libérant un photon. On mesure la lumière émise.
Les deux phénomènes sont complémentaires et leur choix dépend de l’élément à doser et de la sensibilité requise.
II. Fondements Théoriques
Les transitions électroniques
Seuls les électrons de valence (les plus éloignés du noyau) participent aux transitions en spectroscopie atomique. Ces transitions sont induites par des rayonnements dans le domaine UV/visible.
Exemple concret — le sodium (Na) :
Le sodium possède 11 électrons avec la configuration : 1s² 2s² 2p⁶ 3s¹
Sa transition la plus intense correspond au passage 3s → 3p, qui génère la célèbre raie D à 589 nm (lumière jaune caractéristique des lampadaires à vapeur de sodium).
La loi de Beer-Lambert adaptée à la SAA
En absorption atomique, la relation entre l’intensité lumineuse incidente (I₀) et transmise (I) suit une loi exponentielle :
I = I₀ × exp(−K × l × N₀)
Avec :
- l : longueur de la flamme
- N₀ : nombre d’atomes à l’état fondamental
- K : coefficient propre à l’élément pour la longueur d’onde choisie
Dans des conditions expérimentales constantes, cette relation se simplifie et l’absorbance devient directement proportionnelle à la concentration : A = k × C
La loi de Maxwell-Boltzmann : choisir entre SAA et SEA
La distribution de Maxwell-Boltzmann permet de calculer le rapport entre les atomes excités (Nₑ) et les atomes à l’état fondamental (N₀).
Quelques exemples à T = 2000 K :
| Élément | Longueur d’onde | Nₑ / N₀ |
|---|---|---|
| Sodium (Na) | 589 nm | 1,305 × 10⁻⁵ |
| Cuivre (Cu) | 325 nm | 4,77 × 10⁻¹⁰ |
Conclusion pratique : la grande majorité des atomes restent à l’état fondamental → la SAA est systématiquement privilégiée pour la plupart des éléments. La SEA est préférée pour les métaux alcalins (Na, K, Li) dont l’excitation est facile même à basse température.
III. Préparation des Échantillons
Avant toute analyse, l’échantillon doit être converti en solution homogène contenant l’élément sous forme atomique libre. Trois voies principales existent :
1. La voie humide (digestion acide) Décomposition en milieu acide (HNO₃, HCl, H₂SO₄) avec ajout d’oxydants (H₂O₂). Simple mais parfois incomplète. Déconseillée pour la nébulisation ultrasonique.
2. La minéralisation à sec Calcination à 450°C puis reprise des cendres en solution acide. Minéralisation totale, mais attention : certains éléments volatils (As, Hg, Se) se perdent à des températures supérieures à 450°C.
3. L’extraction liquide-liquide Formation d’un chélate avec extraction en phase organique. Permet à la fois d’éliminer les interférents et de préconcentrer les traces.
IV. Instrumentation : Le Spectrophotomètre d’Absorption Atomique
Un spectrophotomètre d’absorption atomique comprend quatre composants essentiels :
1. La Source Lumineuse
La source doit émettre la raie de résonance caractéristique de l’élément à doser. Deux types principaux :
La lampe à cathode creuse (HCL) — la plus utilisée +++
- Cylindre en verre rempli de gaz rare (Ar ou Ne) sous faible pression
- Cathode creuse revêtue du métal à analyser
- Anode en nickel ou tungstène
- Fenêtre en quartz transparente aux UV
Principe : sous l’effet d’une décharge électrique, les ions du gaz bombardent la cathode, éjectent des atomes du métal, qui s’excitent et émettent leur rayonnement caractéristique.
⚠️ Contrainte majeure : une lampe par élément à doser. Des lampes multiéléments existent mais restent limitées.
La lampe à décharge sans électrodes (EDL) Un courant haute fréquence dans une bobine crée un champ magnétique qui ionise le gaz inerte et excite les atomes, produisant un rayonnement plus intense que la HCL — particulièrement utile pour As, Se, Te.
2. Les Générateurs d’Atomes (Atomiseurs)
L’atomisation est l’étape clé : elle consiste à transformer l’échantillon en vapeur d’atomes libres.
a) La flamme
La solution est nébulisée (transformée en aérosol fin) puis introduite dans la flamme. L’efficacité dépend de la géométrie du nébuliseur, du débit de comburant et de la viscosité de la solution.
Principales flammes utilisées :
| Mélange | Température | Éléments dosés |
|---|---|---|
| Air / Propane | 1800–1900°C | Li, Na, K |
| Air / Acétylène | 2300–2500°C | Ca, Mg, Cu, Zn, Fe |
| N₂O / Acétylène | jusqu’à 3200°C | Éléments formant des oxydes réfractaires |
b) Le four graphite (GF-AAS)

Le four graphite chauffe l’échantillon par étapes (séchage → minéralisation → atomisation) jusqu’à ~2700°C.
✅ Avantages majeurs :
- Consommation minimale d’échantillon (quelques microlitres)
- Limite de détection de l’ordre du ppb (µg/L)
- Possible analyse directe sans minéralisation pour les éléments volatils
❌ Inconvénients :
- Émission propre du graphite au-delà de 2500°C
- Les éléments réfractaires (W, V, Al) forment des monoxydes stables nécessitant des gaz réducteurs
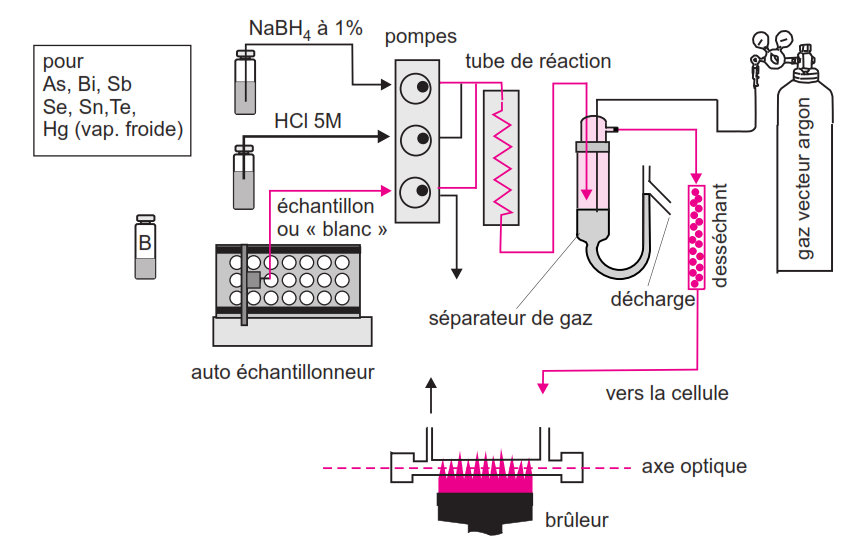
c) La génération d’hydrures
Utilisée pour As, Sb, Se, Te, Bi, Sn. L’élément réagit avec NaBH₄ en milieu acide pour former un hydrure gazeux. Celui-ci est entraîné dans un tube de quartz chauffé à ~1000°C où il est atomisé.
d) Cas particulier du mercure (Hg)
Le mercure est réduit directement à l’état métallique par NaBH₄ ou SnCl₂ :
Hg(II)Cl₂ + Sn(II)Cl₂ → Hg(0) + Sn(IV)Cl₄
Sa pression de vapeur élevée à température ambiante suffit à l’état gazeux → technique dite “vapeur froide”, sans chauffage nécessaire.
3. La Séparation des Rayonnements : Le Monochromateur
Placé entre l’atomiseur et le détecteur, le monochromateur isole la longueur d’onde analytique. Il élimine :
- Les raies non analytiques de la lampe
- Les raies du gaz de remplissage
- Les impuretés spectrale
- L’émission propre de la flamme
4. La Détection
Trois types de détecteurs sont utilisés :
- Détecteurs thermiques
- Détecteurs pyroélectriques
- Photomultiplicateur +++ (le plus courant, haute sensibilité)
Le signal est converti en absorbance, directement reliée à la concentration via la loi de Beer-Lambert.
5. L’Injection FIAS (Flow Injection Atomic Spectrometry)
Système d’introduction innovant permettant une injection automatisée de l’échantillon dans un flux porteur continu.
Avantages clés :
- Flux continu et bonne reproductibilité
- Dilution non indispensable (dispersion contrôlée)
- Injection de petits volumes (0,2 à 1 mL) → limite l’encrassement du brûleur
- Idéal pour les analyses en série
V. Spectroscopie d’Émission Atomique (SEA) et ICP-AES
La photométrie de flamme
Technique simple et robuste, idéale pour les métaux alcalins (Na, K, Li, Ca).
L’échantillon est atomisé et excité dans une flamme. Chaque atome excité émet sa longueur d’onde caractéristique lors du retour à l’état fondamental. L’intensité émise est directement proportionnelle à la concentration :
Iₑ = K × C
L’ICP-AES : la technique multiélémentaire de référence

L’ICP (Inductively Coupled Plasma) génère un plasma d’argon à des températures comprises entre 5 000 et 8 000 K, voire jusqu’à 10 000 K dans certains systèmes modernes.
À ces températures extrêmes, tous les atomes de l’échantillon sont simultanément excités et émettent leurs raies caractéristiques.
Avantages de l’ICP-AES :
- Analyse multiélémentaire en une seule injection
- Limites de détection très basses (ppb à ppt)
- Faibles interférences chimiques
- Plage linéaire étendue
- Adapté aux matrices complexes
Application concrète : un laboratoire peut doser simultanément 30 à 40 éléments traces dans un seul échantillon pharmaceutique en quelques minutes — ce qui serait impossible en SAA classique.
VI. Les Interférences et Leurs Corrections
Toute méthode analytique est susceptible d’interférences. En spectroscopie atomique, trois types sont identifiés :
Interférences spectrales
- Superposition de raies : corrigée par l’effet Zeeman (application d’un champ magnétique qui modifie les niveaux d’énergie atomiques)
- Absorptions moléculaires : dues aux molécules de la matrice (ex. : CaOH perturbe le dosage du Ba). Corrigées par lampe au deutérium
- Diffusion de la lumière : sur des particules solides ou liquides, corrigée par effet Zeeman
Interférences chimiques (effets de matrice)
Réactions parasites dans la flamme (oxydation, ionisation, formation de composés réfractaires). Corrigées par l’addition de modificateurs de milieu (ex. : La₂O₃ pour libérer le Ca en présence de phosphates).
Interférences physiques
Différences de viscosité entre solutions étalons et échantillons. Corrigées par préparation d’étalons à matrice adaptée ou par la méthode des ajouts dosés.
VII. Méthodes de Dosage
Méthode de la courbe d’étalonnage (Procédé I)
- Préparation de solutions étalons de concentrations connues
- Tracé de la courbe Absorbance = f(Concentration)
- Lecture de la concentration de l’inconnu par interpolation
- ⚠️ Validité uniquement dans la zone de linéarité (concentrations faibles)
Méthode des ajouts dosés (Procédé II)
- Ajout de quantités connues de l’élément à la matrice même de l’échantillon
- Permet de s’affranchir des effets de matrice
- Particulièrement recommandée pour les matrices complexes (sang, urine, extraits végétaux)
VIII. Applications en Pharmacopée Européenne
La spectroscopie atomique est officiellement inscrite dans la Pharmacopée Européenne sous deux rubriques :
- SAA : rubrique 2.2.23 — Spectrométrie d’absorption atomique
- SEA : rubrique 2.2.22 — Spectrométrie d’émission atomique en flamme
- ICP-AES : rubrique 2.2.57 — Spectrométrie d’émission à plasma
Exemples concrets de dosages réglementaires
Solution d’albumine humaine : → Dosage du sodium par SEA (λ = 589 nm, Procédé I) → Norme : entre 95 % et 105 % de la teneur indiquée sur l’étiquette
Dextranomère : → Dosage du bore par ICP-AES (rubrique 2.2.57) → Norme : maximum 30,0 ppm
Autres applications courantes :
- Contrôle des métaux lourds (Pb, Cd, As, Hg) dans les médicaments
- Dosage des oligo-éléments dans les solutions de nutrition parentérale
- Suivi thérapeutique du lithium (traitement des troubles bipolaires)
- Contrôle de la teneur en fer, zinc, magnésium dans les compléments alimentaires
IX. Tableau Comparatif : SAA vs SEA vs ICP-AES
| Critère | SAA | SEA (flamme) | ICP-AES |
|---|---|---|---|
| Principe | Absorption | Émission | Émission |
| Température | 2000–3200°C | 1800–3200°C | 5000–10 000 K |
| Limite de détection | ppb | ppm–ppb | ppb–ppt |
| Nombre d’éléments/analyse | 1 | 1 | 30–40 |
| Éléments préférentiels | Métaux traces | Na, K, Li, Ca | Tous les éléments |
| Interférences chimiques | Modérées | Faibles | Très faibles |
| Coût | Modéré | Faible | Élevé |
X. Avantages, Limites et Évolutions Récentes
✅ Avantages de la spectroscopie atomique
- Haute sensibilité : détection jusqu’au ppb (µg/L) et au-delà
- Grande spécificité : chaque élément possède sa signature spectrale unique
- Rapidité d’analyse : résultats en quelques minutes
- Faible volume d’échantillon : 1 mL peut suffire
- Faible influence de la matrice comparé à d’autres techniques
❌ Limites à connaître
- Nécessité d’une source spécifique par élément en SAA (une lampe = un élément)
- Technique destructrice de l’échantillon
- Applicable quasi exclusivement aux métaux et métalloïdes
- Concentrations élevées → non-linéarité, nécessité de dilution
🔬 Évolutions technologiques récentes
Les progrès récents portent sur l’automatisation accrue (systèmes robotisés de préparation), l’amélioration des sources lumineuses (optiques à fibres optiques dans la gamme PinAAcle de PerkinElmer), et le développement de la SAA à source continue haute résolution (HR-CS AAS) permettant l’analyse multiélémentaire sans changement de lampe.
En 2018, la Commission Européenne de la Pharmacopée a mis à jour les chapitres relatifs à la spectrométrie, intégrant les nouvelles technologies et confirmant la place centrale de la SAA dans le contrôle qualité pharmaceutique.
Conclusion : La Spectroscopie Atomique, un Pilier de l’Analyse Pharmaceutique
La spectroscopie atomique — qu’il s’agisse de la SAA, de la SEA ou de l’ICP-AES — représente un outil analytique incontournable en pharmacie, en toxicologie et en sciences environnementales.
Elle se distingue par sa sensibilité exceptionnelle, sa spécificité élémentaire et sa conformité réglementaire avec la Pharmacopée Européenne.
À retenir en 5 points clés :
- La SAA mesure l’absorption d’atomes à l’état fondamental — idéale pour les traces
- La SEA mesure l’émission d’atomes excités — idéale pour Na, K, Li
- L’ICP-AES permet une analyse multiélémentaire à très haute sensibilité
- La loi de Beer-Lambert est le fondement quantitatif de la SAA
- Les interférences (spectrales, chimiques, physiques) doivent toujours être identifiées et corrigées