Interactions Rayonnement–Matière : Comprendre les Bases de la Spectroscopie en Pharmacie
Par le Département de Pharmacie d’Alger – Chimie Analytique, 3ème année Pharmacie
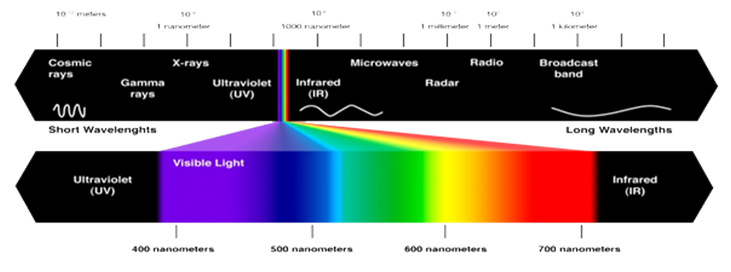
Le spectre électromagnétique, fondement de toute analyse spectroscopique
Introduction : Qu’est-ce qu’un Spectre ?
Étymologiquement, un spectre est une image. Ce terme est apparu pour la première fois en français en 1675, dans la traduction d’un ouvrage de Newton, pour désigner l’image formée par la décomposition de la lumière à travers un prisme.
Aujourd’hui, le mot “spectre” désigne toute trace de la réponse de la matière à une perturbation extérieure. Cette perturbation est le plus souvent une onde électromagnétique.
La spectroscopie est une discipline centrale en chimie analytique pharmaceutique. Elle permet d’identifier, de caractériser et de quantifier les substances chimiques sans les détruire — un atout majeur dans le domaine du médicament.
💡 Le saviez-vous ? Plus de 70 % des analyses en laboratoire pharmaceutique reposent sur des techniques spectroscopiques (UV-Visible, IR, RMN, fluorescence…).
I – Rappels sur les Radiations Lumineuses
Qu’est-ce qu’une radiation lumineuse ?
Une radiation lumineuse est constituée de deux composantes vectorielles perpendiculaires qui varient de façon sinusoïdale :
- Un vecteur champ électrique (E)
- Un vecteur champ magnétique (B)
C’est pourquoi on parle de Rayonnement Électro-Magnétique (REM).
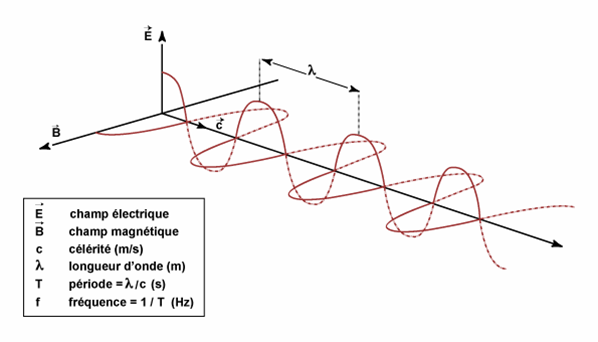
Propagation d’une onde électromagnétique dans l’espace
La Dualité Onde-Corpuscule
Le rayonnement électromagnétique possède une double nature, concept fondamental de la physique quantique :
En tant qu’onde électromagnétique : L’analyse spectrale permet de décomposer cette onde en ondes monochromatiques de longueurs d’onde λ et de fréquences ν différentes.
En tant que photon (corpuscule) : Le photon est un corpuscule de masse nulle dont l’énergie est :
E = h × ν
Où :
- h = constante de Planck = 6,626069 × 10⁻³⁴ J·s
- ν = fréquence = c / λ
- c ≈ 3 × 10⁸ m/s (célérité de la lumière dans le vide)
Tableau I : Paramètres Caractéristiques de l’Onde
| Paramètre | Symbole | Définition | Relation | Unités |
|---|---|---|---|---|
| Longueur d’onde | λ | Distance entre deux crêtes successives | λ = C / ν | m, nm, Å, μm |
| Fréquence | ν | Nombre d’oscillations par seconde | ν = C / λ | Hertz (Hz) |
| Nombre d’ondes | ν̃ | Nombre d’ondes par unité de distance | ν̃ = 1 / λ | cm⁻¹ |
| Amplitude | A | Mesure de la force du champ électrique ou magnétique | — | Correspond au champ électrique |
| Période | T | Temps pour un cycle complet | T = 1 / ν | Secondes |
II – Énergie d’une Molécule
Les Niveaux d’Énergie Moléculaire
Lorsqu’une molécule absorbe de la lumière, elle subit une modification de la distance entre ses particules (électrons, noyaux). La molécule passe alors par un phénomène appelé transition énergétique.
L’absorption moléculaire d’un photon (hν) provoque 3 types de transitions selon l’énergie apportée :
- Transitions Électroniques → les plus énergétiques
- Transitions Vibrationnelles → énergie intermédiaire
- Transitions Rotationnelles → les moins énergétiques
On a la relation :
E électronique > E vibrationnelle > E rotationnelle

Représentation des niveaux d’énergie quantiques d’une molécule
Relation entre Énergie et Domaine Spectral
- Faible énergie (micro-ondes) → provoque uniquement la rotation de la molécule
- Énergie moyenne (infrarouge) → la molécule est en état rovibrationnel : E = Eᵣ + Eᵥ → la molécule tourne et vibre
- Grande énergie (UV) → produit simultanément rotation, vibration et saut d’électrons
III – Interactions Rayonnement–Matière
Les Deux Processus Fondamentaux
Il existe deux grands types de processus d’interaction entre un rayonnement et la matière :
1 – L’Absorption
Lorsqu’un photon d’énergie hν rencontre une molécule M au niveau d’énergie fondamental, il peut être absorbé si son énergie correspond exactement à la différence entre deux niveaux d’énergie :
M + hν → M*
La condition d’absorption est : hν = E₂ – E₁
La molécule passe ainsi à un état excité M*.
2 – L’Émission
La molécule excitée M* est instable. Elle retourne à son état fondamental en émettant un photon de même énergie :
M* → M + hν
💡 Application pharmaceutique : Ces deux phénomènes sont exploités dans des techniques comme la spectrophotométrie UV-Visible (dosage de médicaments), la fluorimétrie (détection de contaminants) ou encore la Spectrométrie d’Absorption Atomique (SAA) (dosage des métaux dans les médicaments).
IV – Notion de Spectre
Définition
Un spectre est la décomposition du rayonnement électromagnétique selon ses différentes composantes en termes de :
- Fréquence (ou période)
- Énergie des photons
- Longueur d’onde associée
Les Régions Spectrales
Le spectre électromagnétique s’étend sur un très large domaine de longueurs d’onde :
Tableau II : Domaines du Spectre Électromagnétique
| Domaine | Longueur d’onde | Caractéristiques |
|---|---|---|
| Rayons γ | 10⁻⁵ nm à 10⁻³ nm | Très énergétiques, émis par éléments radioactifs, très nocifs |
| Rayons X | 10⁻³ nm à 10 nm | Très énergétiques, traversent la matière et les matériaux |
| Ultraviolet (UV) | 10 nm à 400 nm | Assez énergétiques, nocifs pour la peau |
| Visible | 400 nm à 750 nm | Partie perceptible par l’œil humain |
| Infrarouge (IR) | 750 nm à 1 mm | Émis par tout corps à T > –273°C |
| Ondes radar / hyperfréquences | 1 cm à 1 m | Localisation et identification d’objets |
| Ondes radio | Quelques cm à plusieurs km | Transmission de l’information |
 Le spectre électromagnétique complet, de la radio aux rayons gamma
Le spectre électromagnétique complet, de la radio aux rayons gamma
V – Aspect d’un Spectre
1 – Le Spectre d’Absorption
Un spectre d’absorption est un graphe représentant :
- En ordonnée : l’Absorbance (A) ou la Transmittance (T) — paramètres caractéristiques de l’absorption
- En abscisse : la Longueur d’onde (λ), la Fréquence (ν), ou le Nombre d’onde (σ) — paramètres caractérisant le photon
En UV-Visible, le spectre montre un pic caractéristique à une longueur d’onde maximale λₘax avec une absorbance maximale εₘax.
En Infrarouge (IR), le spectre est représenté en Transmittance en fonction du nombre d’onde.
2 – Le Spectre d’Émission
Un spectre d’émission représente :
- En ordonnée : l’Intensité ou l’énergie relative — paramètre caractéristique de l’émission
- En abscisse : Longueur d’onde (λ), Fréquence (ν) ou Nombre d’onde (σ)

Spectrophotomètre utilisé en laboratoire pharmaceutique pour l’analyse des médicaments
VI – Les Différents Types de Spectre
Il existe trois grandes catégories de spectres :
1 – Le Spectre de Raies
Séries de pics étroits et bien définis liés à l’excitation d’atomes individuels. Chaque élément chimique possède son spectre de raies unique, qui sert d’empreinte digitale en analyse qualitative.
2 – Le Spectre de Bandes
Constitué de plusieurs groupes de raies tellement proches les unes des autres qu’elles ne sont pas complètement résolues. Ces spectres sont dus aux molécules.
3 – Le Spectre Continu
Spectre sans raies, obtenu en chauffant des solides à haute température. Exemple classique : le rayonnement du corps noir.
A – Spectres d’Émission en Détail
1 – Spectre de Raies
Le spectre de raies est caractéristique de chaque élément chimique. Il peut être utilisé en analyse qualitative par comparaison du spectre observé avec des spectres de référence connus → identification des espèces chimiques.
2 – Spectre de Bandes
Formé de plusieurs groupes de raies trop proches pour être résolues individuellement. Raies émises par des molécules excitées.
3 – Spectre Continu d’Origine Thermique
Un corps solide porté à haute température émet un rayonnement continu sur un large spectre.
B – Spectres d’Absorption en Détail
1 – Bandes d’Absorption
Exemple : Spectre d’absorption du permanganate de potassium (KMnO₄)
- De la lumière blanche est envoyée vers la solution de KMnO₄
- On analyse la lumière transmise
- Observation : Le spectre ressemble à celui de la lumière blanche, mais est privé de certaines bandes (pas de vert ni de jaune)
- Interprétation : Les espèces chimiques présentes absorbent la lumière de certaines zones du spectre → spectre de bandes d’absorption
Conclusion : Les solutions colorées se comportent comme des filtres ne laissant passer que certaines couleurs. Les couleurs manquantes correspondent aux radiations absorbées par les espèces chimiques présentes en solution.
2 – Raies d’Absorption
Exemple : Spectre de la vapeur d’atome de sodium
- On envoie de la lumière blanche sur une flamme contenant des ions sodium
- Observation : Le spectre est privé d’une raie de lumière jaune, au même emplacement que la raie d’émission du sodium
- Conclusion : Les spectres d’absorption et d’émission sont complémentaires. Un élément chimique absorbe exactement les radiations qu’il est capable d’émettre.
VII – Classification des Méthodes Spectroscopiques
Les différentes méthodes analytiques en spectroscopie se classent selon le phénomène mis en jeu :
Méthodes basées sur l’Absorption :
- UV-Visible (moléculaire) → dosage de principes actifs
- Infrarouge – IR (moléculaire) → identification de groupements fonctionnels
- SAA – Spectrométrie d’Absorption Atomique (atomique) → dosage des métaux traces
Méthodes basées sur l’Émission :
- Fluorescence (moléculaire) → détection à très faibles concentrations
- SEA – Spectrométrie d’Émission Atomique (atomique) → analyse multi-élémentaire
- Diffusion Raman → analyse de structure moléculaire

Laboratoire d’analyse pharmaceutique utilisant les techniques spectroscopiques modernes
💡 Application concrète en pharmacie : La Pharmacopée Européenne impose l’utilisation de la spectrophotométrie UV-Visible et de la spectrométrie infrarouge pour le contrôle qualité de plus de 2 000 substances actives pharmaceutiques.
Conclusion : Pourquoi Maîtriser les Interactions Rayonnement–Matière ?
La compréhension des interactions rayonnement–matière est un fondement indispensable pour tout pharmacien analyste. Ces connaissances permettent de :
- Identifier des substances chimiques inconnues
- Doser avec précision les principes actifs dans les médicaments
- Contrôler la qualité des matières premières et des produits finis
- Détecter les contaminants et les impuretés à très faibles concentrations
Que vous travailliez en industrie pharmaceutique, en officine, en laboratoire de contrôle ou en recherche, la spectroscopie sera un outil quotidien incontournable.
📚 Pour aller plus loin :
- Skoog, Holler, Crouch – Principles of Instrumental Analysis, 7ème édition
- Pharmacopée Européenne – Méthodes générales de spectroscopie
- ANSM – Guides de validation des méthodes analytiques



