Les Anti-Inflammatoires Non Stéroïdiens (AINS) : Chimie, Synthèse et Mécanismes d’Action — Guide Complet
Introduction : Pourquoi les AINS sont-ils incontournables en pharmacologie ?
Chaque jour, des millions de personnes dans le monde prennent un comprimé d’aspirine, d’ibuprofène ou de diclofénac pour soulager une douleur, faire baisser une fièvre ou calmer une inflammation. Les anti-inflammatoires non stéroïdiens (AINS) font partie des médicaments les plus consommés au monde.
Le marché mondial des AINS était évalué à plus de 22 milliards de dollars en 2024, avec une croissance continue tirée par la prévalence croissante de la douleur chronique. Et ce chiffre ne cesse d’augmenter : les projections estiment que ce marché devrait atteindre 38 milliards de dollars d’ici 2031.
Mais au-delà de leur usage clinique quotidien, les AINS représentent un sujet fascinant en chimie thérapeutique. Comment sont-ils synthétisés en laboratoire ? Quels mécanismes moléculaires expliquent leurs effets ? Ce guide complet répond à toutes ces questions, du plus simple (l’aspirine) au plus sophistiqué (le célécoxib).
Qu’est-ce qu’un AINS ? Définition et mécanisme général
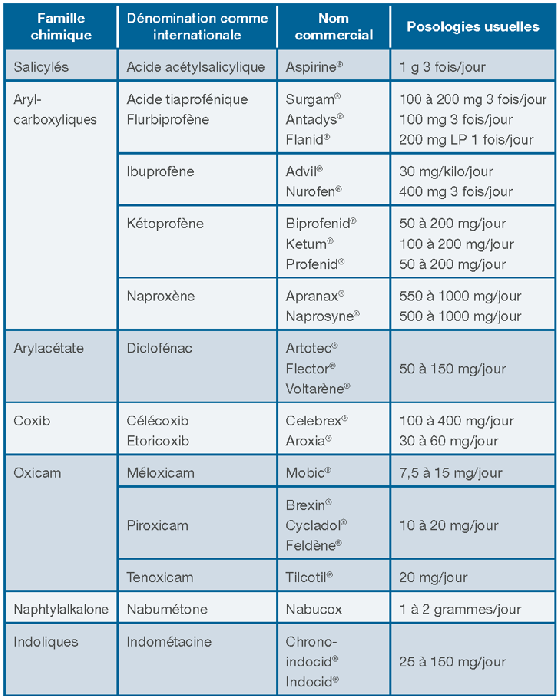
Les anti-inflammatoires non stéroïdiens, souvent abrégés en AINS, sont des médicaments aux propriétés antalgiques, antipyrétiques et anti-inflammatoires. Le terme « non stéroïdien » est utilisé pour les distinguer des glucocorticoïdes, qui ont une action anti-inflammatoire similaire.
Les AINS sont des inhibiteurs de la cyclooxygénase (COX). Ils produisent leurs effets en inhibant la formation de prostaglandines et de thromboxane. Les prostaglandines sont des médiateurs chimiques responsables de la douleur, de la fièvre et de l’inflammation.
On distingue deux grandes familles d’enzymes COX :
- COX-1 : enzyme constitutive, présente en permanence dans l’organisme, assure des fonctions protectrices (notamment au niveau gastrique).
- COX-2 : enzyme inductible, exprimée lors d’une inflammation ou d’un traumatisme tissulaire.
Les AINS classiques inhibent les deux isoformes (non sélectifs), ce qui explique à la fois leur efficacité thérapeutique et leurs effets indésirables gastriques. Les coxibs (comme le célécoxib) ont été développés pour cibler spécifiquement COX-2, réduisant ainsi les risques gastriques.

Les grandes familles d’AINS et leur synthèse chimique
1. Les Salicylates — L’aspirine, chef de file historique
Structure chimique et nomenclature
L’aspirine, ou acide acétylsalicylique (acide 2-acétoxybenzoïque), est le prototype des AINS. Sa structure comporte un noyau aromatique portant deux groupements fonctionnels : un acide carboxylique (–COOH) et un ester acétate (–OCOCH₃).
La réaction de Kolbe-Schmitt (1860) : point de départ de tout
La synthèse de l’aspirine commence par la préparation de l’acide salicylique via la réaction de Kolbe-Schmitt, une étape fondamentale découverte en 1860.
Le principe est le suivant :
- Le phénol est traité par la soude (NaOH) pour former le phénolate de sodium.
- Ce sel est soumis à du CO₂ sous pression (4 à 7 atmosphères) à 125°C.
- Il se forme le salicylate de sodium, acidifié ensuite pour donner l’acide salicylique.
C’est une réaction de carboxylation électrophile aromatique, où le CO₂ joue le rôle d’électrophile sur l’oxygène phénolate activé.
Acétylation de l’acide salicylique → Aspirine
L’étape finale consiste à acétyler le groupement hydroxyle phénolique de l’acide salicylique. On fait réagir l’acide 2-hydroxybenzoïque avec l’anhydride acétique en milieu acide :
Acide salicylique + Anhydride acétique → Aspirine + Acide acétique
Ce mécanisme implique une attaque nucléophile de l’oxygène phénolique sur le carbone carbonyle de l’anhydride acétique, suivie d’une élimination d’acide acétique.
Le saviez-vous ? L’aspirine est l’un des médicaments les plus consommés dans le monde. Au-delà de ses effets anti-douleur et anti-inflammatoires, elle est utilisée à faible dose comme antiagrégant plaquettaire (prévention des accidents cardiovasculaires).
2. Les Anthranilates — L’acide méfénamique
Structure et nomenclature IUPAC
L’acide méfénamique (acide 2-((2,3-diméthylphényl)amino)benzoïque) appartient à la famille des acides fénamiques ou anthranilates. Sa structure est caractérisée par un pont amino (–NH–) reliant deux noyaux aromatiques, l’un portant un groupement carboxylique et l’autre deux méthyles en positions 2 et 3.
Synthèse par condensation d’Ullmann
La voie de synthèse de l’acide méfénamique repose sur la condensation d’Ullmann, une réaction classique de couplage C–N ou C–C catalysée par le cuivre.
Les réactifs de départ sont :
- Le 2-chlorobenzoate de potassium (source du noyau carboxylique)
- La 2,3-diméthylaniline (source du noyau aminé)
En présence d’acétate de cuivre (Cu(CH₃COO)₂) comme catalyseur, les deux réactifs se couplent via substitution nucléophile aromatique pour donner directement l’acide méfénamique. Le mécanisme implique l’oxydation du Cu(I) en Cu(III), la formation d’un complexe organocuprate, puis une élimination réductrice.
Avantage clinique : L’acide méfénamique est particulièrement utilisé dans le traitement des dysménorrhées (douleurs menstruelles) et des douleurs musculaires légères à modérées.
3. Les Arylacétates — Le diclofénac
Structure chimique
Le diclofénac (acide 2-(2-((2,6-dichlorophényl)amino)phényl)acétique) est un AINS de la famille des arylacétates. Sa structure présente deux noyaux phényliques reliés par une liaison amino, l’un portant deux atomes de chlore en positions 2 et 6, et une chaîne acide acétique en position 2 de l’autre phényle.
La présence des deux chlores en positions ortho joue un rôle stérique crucial : ils bloquent la rotation du cycle dichlorophényle, ce qui confère à la molécule une conformation particulière favorable à l’inhibition de COX.
Voie de synthèse en 5 étapes
La synthèse du diclofénac est plus complexe et se déroule en plusieurs étapes :
Étape 1 — Condensation d’Ullmann : L’acide 2-chlorobenzoïque et la 2,6-dichloroaniline sont couplés en présence de KOH et de cuivre pour donner l’acide 2-((2,6-dichlorophényl)amino)benzoïque.
Étape 2 — Réduction par LiAlH₄ : L’acide carboxylique est réduit en alcool benzylique par l’hydrure de lithium et d’aluminium (LiAlH₄), un réducteur puissant. Le mécanisme passe par la formation d’un complexe aluminate qui transfère successivement deux ions hydrure sur le carbone carbonylique.
Étape 3 — Conversion en dérivé chloré (SOCl₂) : L’alcool obtenu est transformé en chlorure de benzyle par le chlorure de thionyle (SOCl₂). Le mécanisme implique la formation d’un intermédiaire chlorosulfite (ROSOCl) qui se décompose pour libérer SO₂ et HCl.
Étape 4 — Substitution nucléophile par NaCN : Le chlorure de benzyle réagit avec le cyanure de sodium (NaCN) pour donner un nitrile. C’est une réaction SN2 classique.
Étape 5 — Hydrolyse basique du nitrile : Le nitrile est hydrolysé en milieu alcalin (NaOH) pour donner l’acide carboxylique (diclofénac). Cette hydrolyse passe par un amide intermédiaire avant d’aboutir à l’acide final.
Usage clinique : Le diclofénac est disponible sous forme orale, injectable et topique. En Algérie, on le retrouve sous les noms commerciaux Biofenac, Clofenal, Voltarène, Votrex ou Rapidus.
4. Les Arylpropionates — L’ibuprofène
Structure chimique
L’ibuprofène (acide 2-(4-isobutylphényl)propanoïque) est sans doute l’AINS le plus connu du grand public après l’aspirine. Sa structure présente un noyau phénylique substitué en position 4 par un groupement isobutyle et portant une chaîne propanoïque chirale en position 1.
Point important : L’ibuprofène possède un carbone asymétrique en alpha de la fonction acide. La forme commerciale est un mélange racémique, mais c’est le (S)-ibuprofène qui est pharmacologiquement actif.
Synthèse en 4 étapes
Étape 1 — Chlorométhylation de Blanc : L’isobutylbenzène est traité par du formaldéhyde et HCl en présence de ZnCl₂ (acide de Lewis) pour introduire un groupement chlorométhyle (–CH₂Cl) en position para. Le mécanisme passe par la formation d’un cation chlorométhyle (⁺CH₂Cl) qui effectue une substitution électrophile aromatique.
Étape 2 — Substitution par NaCN : Le chlorure de benzyle (1-(chlorométhyl)-4-isobutylbenzène) réagit avec NaCN pour donner le nitrile correspondant (2-(4-isobutylphényl)acétonitrile).
Étape 3 — Alkylation par l’iodure de méthyle : Le nitrile est déprotoné par NaNH₂ (amidure de sodium, base forte) pour former un carbanion stabilisé, qui est ensuite alkylé par l’iodure de méthyle (CH₃I) pour introduire le groupement méthyle alpha et obtenir le (2-(4-isobutylphényl)propanenitrile).
Étape 4 — Hydrolyse basique du nitrile : Comme pour le diclofénac, le nitrile est hydrolysé en milieu NaOH pour donner l’acide ibuprofénique final.

5. Les Oxicams — Le piroxicam
Structure chimique
Le piroxicam (4-hydroxy-2-méthyl-N-(pyridin-2-yl)-2H-benzo[e][1,2]thiazine-3-carboxamide 1,1-dioxide) appartient à la famille des oxicams. Sa structure hétérocyclique est originale : elle comporte un cycle benzothiazinique fusionné portant une fonction acide énolique et une sulfonamide.
Cette structure unique lui confère une demi-vie plasmatique longue (environ 50 heures), ce qui permet une prise unique quotidienne — un avantage thérapeutique majeur.
Synthèse du piroxicam
La synthèse du piroxicam part de la saccharine, un composé commercial facilement accessible :
Étape 1 — Formation du sel de sodium de la saccharine : La saccharine est traitée par NaOH pour former son sel sodique.
Étape 2 — N-alkylation par le chloroacétate de méthyle : L’azote du sel est alkylé par le chloroacétate de méthyle en présence de DMSO pour introduire une chaîne ester.
Étape 3 — Méthylation par CH₃I : L’azote restant est méthylé par l’iodure de méthyle pour donner la 1,2-benzothiazin-4-one.
Étape 4 — Transposition de Smiles (réarrangement O→N) : En milieu basique (CH₃ONa/DMSO), l’ester subit un réarrangement intramoléculaire (transposition en 1,2-benzothiazin-4-one) conduisant à un intermédiaire clé.
Étape 5 — Addition-élimination avec la pyridin-2-amine : L’intermédiaire réagit avec la 2-aminopyridine via une séquence addition-élimination pour donner le piroxicam final.
6. Les Coxibs — Le célécoxib (inhibiteur sélectif de COX-2)
Qu’est-ce qu’un coxib ?
Les coxibs représentent la génération la plus récente des AINS. Ils inhibent sélectivement COX-2, l’enzyme pro-inflammatoire, sans toucher COX-1 (protectrice de la muqueuse gastrique). Ils ont donc un meilleur profil de tolérance digestive, mais des questions sont soulevées quant à leur risque cardiovasculaire.
Note historique : Le rofécoxib (Vioxx) de Merck a été retiré du marché mondial le 30 septembre 2004, car son utilisation à long terme semblait avoir entraîné de très nombreux accidents cardiovasculaires et décès. Le célécoxib, lui, reste commercialisé sous surveillance.
Structure chimique du célécoxib
Le célécoxib (4-(5-(p-tolyl)-3-(trifluorométhyl)-1H-pyrazol-1-yl)benzènesulfonamide) est caractérisé par un noyau pyrazole substitué, portant un groupement trifluorométhyle et une sulfonamide aromatique.
Synthèse en deux étapes clés
Étape 1 — Condensation de Claisen : La p-méthylacétophénone réagit avec le trifluoroacétate d’éthyle en présence de NaOCH₃ (méthanolate de sodium) pour donner une 1,3-dicétone intermédiaire via une condensation de Claisen. Le mécanisme implique la déprotonation du méthyle actif de la cétone, attaque nucléophile sur l’ester, puis élimination d’éthanol.
Étape 2 — Synthèse de KNORR (cyclisation pyrazolique) : La dicétone obtenue réagit avec la 4-sulfonamidophénylhydrazine en milieu éthanol sous reflux, selon la synthèse de Knorr classique pour la formation de pyrazoles. L’hydrazide attaque le carbonyle, forme une hydrazone, puis une cyclisation intramoléculaire conduit au cycle pyrazolique du célécoxib.
Le Paracétamol — AINS ou pas ?
Une classification à nuancer
Le paracétamol (N-(4-hydroxyphényl)acétamide), aussi appelé acétaminophène, mérite une mention spéciale. Le paracétamol n’est pas un AINS, ce qui autorise leur association dans la prise en charge de la douleur ou de la fièvre.
Il possède des propriétés analgésiques et antipyrétiques, mais sans effet anti-inflammatoire significatif et sans inhibition de COX périphérique notable aux doses thérapeutiques. Son mécanisme d’action reste partiellement débattu.
Synthèse industrielle du paracétamol
La synthèse du paracétamol est la plus simple des molécules présentées ici, ce qui explique sa large disponibilité et son faible coût :
Réactifs :
- Le p-aminophénol (4-aminophénol)
- L’anhydride acétique
Réaction : Le groupement amine (–NH₂) du p-aminophénol subit une acétylation sélective par l’anhydride acétique, libérant une molécule d’acide acétique pour donner le paracétamol. C’est une réaction de formation d’amide (liaison peptidique) simple et sélective, car la fonction amine est plus nucléophile que la fonction phénol dans ces conditions.
Dosage clinique : Le paracétamol est la molécule analgésique de première intention. Il est sans danger aux doses thérapeutiques (max. 3 à 4 g/jour chez l’adulte), mais une surdose peut entraîner une hépatotoxicité sévère par accumulation d’un métabolite toxique (N-acétyl-p-benzoquinoneimine, NAPQI).
Tableau comparatif des principaux AINS étudiés
| Molécule | Famille chimique | Voie de synthèse clé | Sélectivité COX |
|---|---|---|---|
| Aspirine | Salicylate | Kolbe-Schmitt + Acétylation | Non sélective |
| Acide méfénamique | Anthranilate | Condensation d’Ullmann | Non sélective |
| Diclofénac | Arylacétate | Ullmann + Réduction + CN | Non sélective |
| Ibuprofène | Arylpropionate | Blanc + Alkylation + Hydrolyse | Non sélective |
| Piroxicam | Oxicam | Saccharine → Transposition | Non sélective |
| Célécoxib | Coxib | Claisen + Knorr | Sélectif COX-2 |
| Paracétamol | Anilide | Acétylation directe | Aucune (non-AINS) |
Effets indésirables et précautions d’emploi
Les AINS sont efficaces, mais leur usage n’est pas sans risque. Voici les effets indésirables à connaître :
Au niveau digestif : Ulcères gastriques, gastrites, saignements. C’est pourquoi les AINS non sélectifs doivent souvent être associés à un protecteur gastrique (inhibiteur de pompe à protons) chez les patients à risque.
Au niveau cardiovasculaire : La plupart des anti-inflammatoires non stéroïdiens (hors aspirine) augmentent le risque de maladies cardiovasculaires lorsqu’ils sont pris de manière prolongée. Dès la première semaine, le risque d’infarctus augmente de 48 % avec l’ibuprofène et de 50 % avec le diclofénac.
Au niveau rénal : Les AINS réduisent la perfusion rénale en diminuant la synthèse des prostaglandines vasodilatatrices. Ils sont contre-indiqués en cas d’insuffisance rénale.
Grossesse : Les AINS sont contre-indiqués à partir du 6ème mois de grossesse (risque de fermeture prématurée du canal artériel).
Les réactions chimiques fondamentales à retenir
Pour les étudiants en pharmacie, voici un résumé des réactions organiques clés utilisées dans la synthèse des AINS :
Réactions de formation de liaisons C–C :
- Condensation de Claisen (formation de dicétones)
- Réaction de Kolbe-Schmitt (carboxylation aromatique)
Réactions de formation de liaisons C–N :
- Condensation d’Ullmann (couplage aromatique catalysé au cuivre)
- Synthèse de Knorr (formation de pyrazoles)
Réactions de transformation de groupements fonctionnels :
- Acétylation (anhydride acétique)
- Réduction de l’acide carboxylique en alcool (LiAlH₄)
- Conversion alcool → chlorure (SOCl₂)
- Substitution nucléophile (NaCN → nitrile)
- Hydrolyse basique du nitrile en acide carboxylique (NaOH)
- Chlorométhylation de Blanc (introduction de –CH₂Cl)
- Alkylation par l’iodure de méthyle (introduction d’un méthyle alpha)
Conclusion — Points clés à retenir
Les AINS constituent une famille médicamenteuse d’une importance capitale, tant sur le plan clinique que chimique. Les AINS détiennent environ 48 % des volumes mondiaux de prescriptions d’anti-inflammatoires, avec plus de 250 millions d’ordonnances dans le monde chaque année.
Voici ce qu’il faut retenir de ce cours :
- Tous les AINS classiques agissent en inhibant les enzymes COX-1 et COX-2, bloquant ainsi la synthèse des prostaglandines inflammatoires.
- Chaque famille chimique (salicylates, anthranilates, arylacétates, arylpropionates, oxicams, coxibs) présente une voie de synthèse originale mettant en jeu des réactions organiques fondamentales.
- La réaction de Kolbe-Schmitt est la clé de la synthèse des salicylates (aspirine).
- La condensation d’Ullmann est utilisée pour les acides méfénamique et diclofénac.
- La condensation de Claisen + synthèse de Knorr permettent d’obtenir le célécoxib, un inhibiteur sélectif de COX-2.
- Le paracétamol n’est pas un AINS, mais peut être associé aux AINS dans les protocoles antidouleur.
- Tout médicament possède un profil d’effets indésirables qu’il est essentiel de connaître pour une prescription raisonnée.
Pour aller plus loin, consultez les cours de chimie thérapeutique de votre programme ou explorez les bases de données moléculaires comme PubChem ou ChemSpider pour visualiser les structures 3D de ces molécules.