Dissolution et Filtration en Pharmacie Galénique : Guide Complet des Opérations Pharmaceutiques Clés
La qualité d’un médicament ne dépend pas uniquement de sa substance active. Elle repose aussi, et surtout, sur la maîtrise des opérations pharmaceutiques qui permettent de le fabriquer. Parmi elles, la dissolution et la filtration occupent une place centrale et indissociable.
Que vous soyez étudiant en pharmacie, technicien de laboratoire ou professionnel de l’industrie pharmaceutique, ce guide vous offre une vue complète et pratique de ces deux opérations fondamentales de la pharmacie galénique.

Pourquoi la Dissolution et la Filtration Sont-elles si Importantes ?
Avant d’entrer dans les détails techniques, il est essentiel de comprendre pourquoi ces deux opérations sont incontournables.
La dissolution est la pierre angulaire de nombreuses formes pharmaceutiques : solutions buvables, solutions injectables, émulsions, collyres… Sans une dissolution correcte du principe actif (PA), le médicament ne peut tout simplement pas exercer son effet thérapeutique.
Dans l’organisme, la dissolution joue un rôle encore plus crucial : elle conditionne le transport du PA à travers les liquides physiologiques, et donc sa rapidité d’action. C’est particulièrement vrai pour les médicaments administrés par voie orale ou injectable.
La filtration, quant à elle, vient compléter la dissolution en garantissant la limpidité et la pureté de la solution obtenue. Les deux opérations forment un tandem indispensable au sein du processus de fabrication.

Partie I — La Dissolution Pharmaceutique
1.1 Définition et Objectif
La dissolution est une opération qui consiste à diviser une substance à l’état moléculaire au sein d’un liquide, pour obtenir un mélange homogène et monophasique appelé solution.
Dans cette solution :
- La substance dissoute s’appelle le soluté (qui peut être gazeux, liquide ou solide)
- Le liquide dans lequel elle se dissout s’appelle le solvant
L’objectif final est d’obtenir une solution parfaitement homogène, sans particules en suspension, prête à être utilisée ou à subir d’autres opérations.
1.2 Les Facteurs qui Influencent la Dissolution
Deux grandes familles de facteurs interviennent : la solubilité et la vitesse de dissolution.
La Solubilité
La solubilité d’une substance dépend de plusieurs paramètres que le galéniste doit maîtriser :
a) La constitution chimique
La solubilité est avant tout une question d’affinité chimique entre le soluté et le solvant. On distingue :
- La solubilité par ionisation (dissociation en ions) : ex. le chlorure de sodium (NaCl) dans l’eau
- La solubilité par polarité : ex. le saccharose dans l’eau, grâce aux affinités entre groupements hydroxyles
Le principe galénique fondamental à retenir : “qui se ressemble s’assemble” — un soluté polaire se dissout dans un solvant polaire, et inversement.
b) La température
Dans la majorité des cas, augmenter la température améliore la solubilité. Cependant, des exceptions existent pour les dissolutions exothermiques. Par ailleurs, l’élévation de température est contre-indiquée pour les substances volatiles ou thermolabiles (comme certaines vitamines ou hormones).
c) Le pH
Le pH influence directement la charge électrique des molécules ionisables : amines, substances amphotères, acides faibles… Un ajustement du pH peut transformer une substance insoluble en substance parfaitement soluble. C’est un levier très utilisé pour formuler des médicaments injectables.
d) La structure cristalline vs. état amorphe
Les molécules organisées en réseaux cristallins réguliers sont plus difficiles à dissoudre que celles à l’état amorphe. Pour dissoudre une substance, il faut “briser” les liaisons entre molécules. Plus l’organisation est rigide, plus cela demande d’énergie.
Exemple concret : certains principes actifs sont intentionnellement formulés à l’état amorphe pour accélérer leur dissolution et améliorer leur biodisponibilité.
e) Les substances additives
Quand un PA est peu soluble dans l’eau, plusieurs stratégies existent :
- Les cyclodextrines : molécules cycliques à base de glucose qui “capturent” les substances hydrophobes par inclusion moléculaire, rendant ainsi soluble ce qui ne l’était pas naturellement.
- Les co-solvants : ajout d’un solvant miscible à l’eau comme l’éthanol ou le glycérol, pour lequel le PA a une meilleure affinité.
La Vitesse de Dissolution : La Loi de Noyes-Whitney
Le galéniste dispose de peu de moyens pour modifier la solubilité intrinsèque d’un PA. En revanche, il peut agir efficacement sur sa vitesse de dissolution, décrite par la loi de Noyes et Whitney :
dC/dt = K × S × (Cs − Ct)
Où :
- dC/dt = vitesse de dissolution
- K = constante (dépend de la température, de la viscosité, de l’agitation)
- S = surface de contact solide/liquide
- Cs = concentration à saturation
- Ct = concentration de la solution au temps t
Pour maximiser la vitesse de dissolution, deux leviers pratiques sont disponibles :
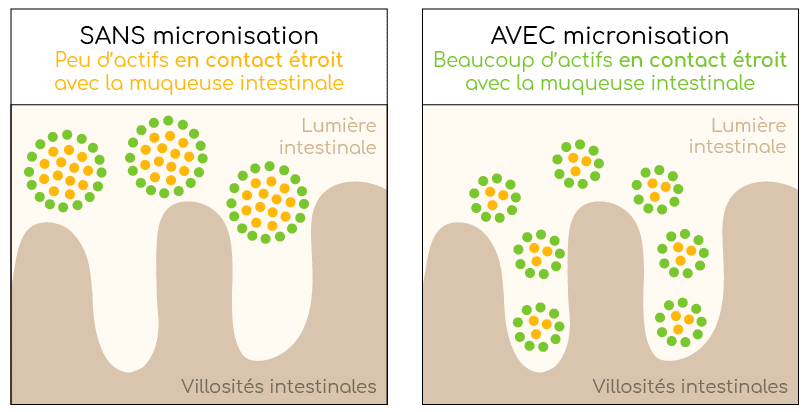
- Augmenter la surface S en fragmentant (micronisant) le solide → plus la poudre est fine, plus la dissolution est rapide
- Augmenter (Cs − Ct) en renouvelant constamment le solvant au contact des particules, grâce à une agitation efficace
1.3 Les Équipements de Dissolution
Pour réaliser une dissolution à l’échelle industrielle ou semi-industrielle, deux éléments sont indispensables : une cuve et un agitateur.
La Cuve
La cuve doit répondre à plusieurs critères stricts :
- Volume adapté : la solution doit occuper entre 20 % et 80 % du volume total de la cuve
- Matériau inerte : l’acier inoxydable 316L est le standard dans l’industrie pharmaceutique. Pour les produits agressifs (comme l’iode ou les dérivés halogénés) ou sensibles à l’oxydation (comme l’adrénaline), on préférera des cuves en plastique ou en verre
- Facilement nettoyable : aucun recoin où les résidus pourraient s’accumuler
Les Types d’Agitateurs
Le choix de l’agitateur est stratégique pour garantir une dissolution homogène :
- Agitateurs à hélice : efficaces pour les liquides peu visqueux, ils créent un flux axial
- Agitateurs à palette : la palette épouse la forme du fond du récipient, assurant une agitation proche des parois
- Turbines : particulièrement utiles pour les poudres très légères. Elles créent un effet cyclone qui aspire les particules restées en surface. Attention cependant au risque d’inclusion d’air dans la préparation
- Agitateurs électromagnétiques et ultrasons : utilisés à l’échelle du laboratoire pour des volumes réduits
1.4 Le Contrôle de la Dissolution
La dissolution doit être vérifiée avant de passer à l’étape suivante. Deux méthodes complémentaires sont utilisées :
- L’examen visuel : vérification de l’homogénéité et de l’absence de particules non dissoutes
- Le dosage des principes actifs dissous : analyse chimique ou spectrophotométrique pour confirmer que la concentration attendue est atteinte
1.5 La Dissolution Extractive (ou Partielle)
Contrairement à la dissolution simple qui vise une dissolution totale, la dissolution extractive est intentionnellement incomplète : elle laisse un résidu (appelé “marc”).
Cette opération est utilisée pour extraire les principes actifs des drogues végétales et animales. La qualité principale recherchée est la sélectivité : le solvant et la température doivent permettre d’extraire uniquement les PA utiles, sans altérer leur structure ni dissoudre les substances inertes.

Les Procédés de Fabrication des Tisanes
Quatre techniques traditionnelles permettent de préparer des tisanes :
- La macération : contact de la drogue avec de l’eau à température ambiante pendant 30 minutes à 4 heures. Technique douce, idéale pour les substances thermolabiles
- La digestion : contact avec de l’eau chauffée entre la température ambiante et l’ébullition (ex. 60 °C) pendant 1 à 15 heures
- La décoction : maintien à ébullition pendant 15 à 30 minutes. Réservée aux drogues dures (racines, écorces) dont les PA résistent à la chaleur
- L’infusion : versement d’eau bouillante sur la drogue, puis refroidissement progressif — la méthode classique pour les plantes aromatiques
La Fabrication des Extraits et Teintures
Pour les extraits et teintures pharmaceutiques, les procédés sont plus sophistiqués :
- Les teintures officinales : solutions médicamenteuses obtenues par action prolongée de l’alcool sur des substances végétales ou animales séchées
- Les extraits : on concentre la solution issue d’une extraction en évaporant le solvant. On obtient ainsi un produit à concentration déterminée en PA
La percolation (aussi appelée lixiviation) est le procédé le plus utilisé en industrie, car elle offre le meilleur rendement. Inspirée du passage du café à travers le filtre, elle consiste à faire traverser lentement (de haut en bas, à froid) la drogue pulvérisée par un solvant (eau ou éthanol). Le contact permanent entre le solvant frais et la drogue maximise l’extraction des PA.
Partie II — La Filtration Pharmaceutique
2.1 Définition et Intérêts
La filtration est une opération qui a pour but de séparer les contaminants particulaires (et parfois microbiens) d’un liquide ou d’un gaz, à l’aide d’un milieu filtrant poreux. Le fluide obtenu après filtration s’appelle le filtrat.
En pharmacie, la filtration remplit plusieurs rôles essentiels :
- Obtenir une solution parfaitement limpide après dissolution
- Vérifier la bonne dissolution du PA (absence de particules sur le filtre)
- Récupérer un précipité d’intérêt
- Assurer la stérilité de certaines préparations injectables ou ophtalmiques
2.2 Les Types de Filtration
Selon la disposition du filtre
Filtration frontale : la totalité du fluide traverse le milieu filtrant. C’est la méthode la plus courante dans les laboratoires et l’industrie.
Filtration tangentielle : le fluide circule parallèlement au filtre, et seule une fraction traverse la membrane. Le reste (rétentat ou concentrat) repart en circuit. Cette technique évite le colmatage et est utilisée pour les produits fragiles ou visqueux.
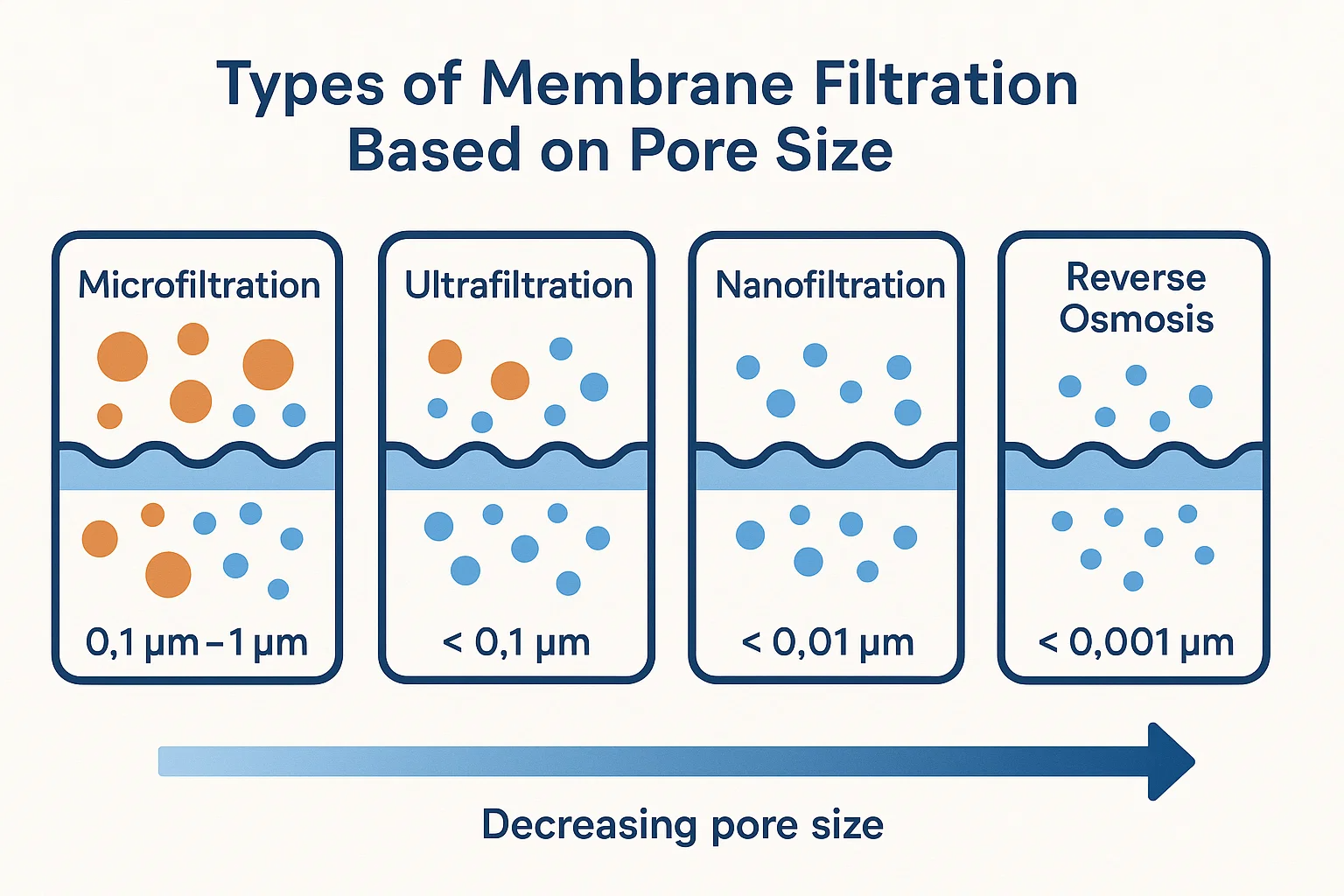
Selon la taille des particules à retenir
| Technique | Taille des particules retenues | Application |
|---|---|---|
| Filtration clarifiante | > 10 µm | Élimination de grosses impuretés |
| Microfiltration | 0,01 à 10 µm | Élimination de bactéries |
| Ultrafiltration | 0,001 à 0,01 µm | Séparation de macromolécules |
| Osmose inverse | < 0,001 µm | Purification de l’eau |
Quand l’objectif est d’éliminer tous les micro-organismes d’un fluide, on parle de filtration stérilisante — une technique capitale pour la fabrication des solutions injectables.
2.3 Les Mécanismes de Rétention
Deux mécanismes principaux expliquent comment un filtre retient les impuretés :
Le Criblage (ou Tamisage)
C’est un phénomène purement mécanique : le filtre retient toutes les particules dont la taille est supérieure à celle de ses pores.
L’inconvénient principal est le colmatage progressif, qui ralentit puis stoppe l’écoulement du filtrat. Les solutions pratiques incluent :
- L’augmentation de la surface filtrante (filtres plissés “en accordéon”)
- L’utilisation de pré-filtres pour retenir les grosses impuretés avant le filtre principal
- L’ajout d’adjuvants de filtration (terres filtrantes)
L’Adsorption
Phénomène physique : des particules plus petites que les pores sont retenues à l’intérieur des canaux du réseau poreux par des interactions électrostatiques ou physico-chimiques.
Ses limites :
- Une variation de pression peut provoquer une désorption (libération brusque des particules)
- Des compétitions entre particules adsorbables peuvent réduire l’efficacité
- Risque d’adsorption des PA dissous, ce qui constitue une perte inacceptable en fabrication pharmaceutique
Filtres Écrans vs. Filtres en Profondeur
Filtres écrans (membranes) : très faible épaisseur, rétention essentiellement par criblage. Pores de diamètre précis et reproductible — idéaux pour la stérilisation filtrante.
Filtres en profondeur : épaisseur supérieure au millimètre, obtenus par compactage de matériaux fibreux. Les impuretés sont arrêtées dans la masse du filtre grâce à la tortuosité des canaux. La rétention combine criblage et adsorption.
2.4 Matériaux et Équipements de Filtration
Les Substances Filtrantes
Le choix du matériau filtrant dépend de la nature du produit à filtrer :
- Fibres de cellulose (coton, papier filtre) : polyvalentes et économiques, disponibles en différentes textures et porosités
- Matières plastiques (polyamides, polyuréthanes, polyesters) : très résistantes mécaniquement, cèdent peu de fibres dans le filtrat
- Membranes organiques (esters de cellulose) : pores de diamètre parfaitement défini — indispensables pour la filtration stérilisante. Nécessitent un support rigide
- Verre fritté : réseau rigide et poreux d’une excellente inertie chimique, obtenu par fusion partielle de particules de verre calibrées
- Poudres filtrantes / adjuvants (charbon, kaolin, terres de diatomées) : déposés en couche sur le filtre principal pour prévenir le colmatage. Attention à leur fort pouvoir adsorbant qui peut retenir les PA
Les Montages de Filtration
Filtration sous pression : le liquide est poussé à travers le filtre par une pression positive. Elle peut utiliser des membranes planes ou des cartouches cylindriques pour augmenter la surface de filtration. C’est le montage le plus utilisé en industrie pour les grandes productions.
Filtration par aspiration (succion) : utilisation de filtres Büchner (porcelaine ou verre fritté) montés sur des fioles connectées à une source de vide. Plus adaptée à l’échelle laboratoire ou pour des volumes modérés.
2.5 Le Contrôle de la Filtration
Un système rigoureux de contrôle qualité encadre la filtration à chaque étape.
Avant la filtration — Test d’intégrité (Point de Bulle)
Ce test vérifie l’uniformité et l’intégrité du filtre :
- Humidifier le filtre avec un liquide adapté (eau ou éther)
- Appliquer une pression progressive
- Mesurer P1 (apparition des premières bulles) et P2 (bulles sur toute la surface)
- Critère de conformité : P1 ≈ P2, indiquant une porosité uniforme
Pendant la filtration
- Mesure du débit (ml/min) pour suivre l’évolution du colmatage
- Mesure de la différence de pression (ΔP) en amont et en aval du filtre : une variation brusque peut révéler une fissure dans la membrane
Après la filtration
- Test du point de bulle à nouveau pour confirmer l’intégrité du filtre
- Examen visuel et microscopique pour vérifier l’absence de particules
- Dosage des PA pour confirmer qu’ils n’ont pas été adsorbés par le filtre
- Recherche d’impuretés éventuellement apportées par les matériaux filtrants eux-mêmes
Conclusion — Maîtriser ces Deux Opérations pour Garantir la Qualité des Médicaments
La dissolution et la filtration ne sont pas de simples étapes techniques : elles sont le garant de la qualité, de la sécurité et de l’efficacité des formes pharmaceutiques liquides.
Les points clés à retenir :
- La dissolution vise une répartition homogène du PA dans le solvant. Sa vitesse peut être optimisée en jouant sur la taille des particules et l’intensité de l’agitation.
- La dissolution extractive, à travers macération, infusion, décoction ou percolation, permet l’obtention de teintures, d’extraits et de tisanes à partir de drogues végétales.
- La filtration assure la limpidité et, dans certains cas, la stérilité de la solution obtenue.
- Le choix du type de filtration, du matériau filtrant et du montage dépend des particules à retenir et des caractéristiques du produit.
- Un système de contrôle rigoureux encadre chaque étape, de l’intégrité du filtre à la vérification finale du filtrat.
La maîtrise de ces opérations, soutenue par un système robuste d’assurance qualité, est indispensable pour garantir des lots de médicaments reproductibles et conformes aux exigences des pharmacopées.



