Solubilité des Principes Actifs Hydrophobes : Solutions Micellaires, Cyclodextrines et Dispersions Solides
Introduction : Un Défi Majeur de la Pharmacie Moderne
La faible solubilité dans l’eau est l’un des obstacles les plus fréquents rencontrés lors du développement de nouveaux médicaments. On estime que plus de 40 % des principes actifs actuellement développés présentent une solubilité aqueuse insuffisante, ce qui compromet directement leur efficacité thérapeutique et leur biodisponibilité.
Selon le Système de Classification Biopharmaceutique (BCS), les médicaments à faible solubilité sont regroupés en classe II (faible solubilité / haute perméabilité) et classe IV (faible solubilité / faible perméabilité). Ces deux catégories représentent un défi considérable pour les formulateurs, car une molécule qui ne se dissout pas correctement ne peut pas traverser efficacement les barrières biologiques pour atteindre sa cible.
Face à ce problème, plusieurs stratégies innovantes ont été développées. Cet article vous présente en détail trois approches clés : les solutions micellaires, les cyclodextrines et les dispersions solides.

I. La Solubilité et la Solubilisation : Notions Fondamentales
Qu’est-ce que la solubilité ?
Une solution est formée d’un ou plusieurs solvants (en proportion majoritaire) et d’une ou plusieurs substances dissoutes appelées solutés. Le solvant peut être aqueux, huileux ou alcoolique.
La solubilité exprime le nombre de parties en volume de liquide nécessaires pour dissoudre une partie en poids de la substance. La Pharmacopée européenne l’exprime en millilitres de solvant nécessaires pour dissoudre 1 g de substance.
| Terme descriptif | Volume de solvant (mL/g) |
|---|---|
| Très soluble | Moins de 1 |
| Facilement soluble | 1 à 10 |
| Soluble | 10 à 30 |
| Assez soluble | 30 à 100 |
| Peu soluble | 100 à 1 000 |
| Très peu soluble | 1 000 à 10 000 |
| Pratiquement insoluble | Plus de 10 000 |
Les facteurs influençant la solubilité
La solubilité d’un principe actif dépend de plusieurs paramètres interdépendants :
- La nature chimique de la molécule et sa polarité
- La structure cristalline du composé
- La température et le pH du milieu de dissolution
Lorsque la solubilité d’un principe actif est insuffisante, le formulateur dispose de plusieurs stratégies. On distingue :
- Les méthodes chimiques : ajustement du pH, formation de sels, utilisation de co-solvants, recours aux prodrugs solubles
- Les méthodes physiques : micronisation, nano-suspensions, polymorphisme, dispersions solides, cyclodextrines, solutions micellaires
II. Les Solutions Micellaires : La Solubilisation par les Tensioactifs
Qu’est-ce qu’un surfactif ?
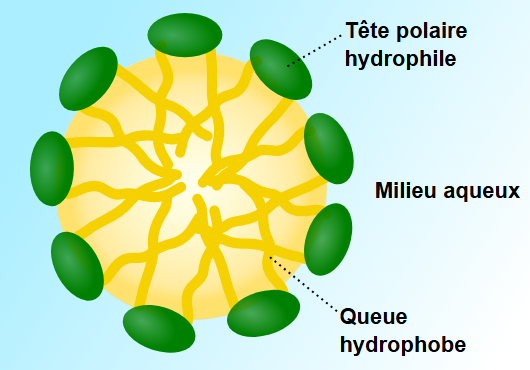
Les surfactifs (ou tensioactifs) sont des molécules amphiphiles, c’est-à-dire qu’elles possèdent simultanément :
- Une partie hydrophile (tête polaire, affinité pour l’eau)
- Une partie hydrophobe (chaîne carbonée, affinité pour les huiles et solvants organiques)
Cette double nature leur confère des propriétés de surface remarquables. On retrouve les surfactifs dans de nombreux médicaments injectables, mais aussi dans les formes orales et topiques.
La Concentration Micellaire Critique (CMC)
Lorsqu’on augmente progressivement la concentration d’un surfactif dans l’eau, les molécules se dispersent individuellement jusqu’à atteindre un seuil précis : la Concentration Micellaire Critique (CMC). Au-delà de ce seuil, les molécules de surfactif s’organisent spontanément en structures appelées micelles.
La CMC est déterminée expérimentalement en traçant la tension superficielle en fonction du logarithme de la concentration en surfactif. La rupture de pente sur ce graphique indique précisément la CMC.
Pour la plupart des surfactifs pharmaceutiques, la CMC se situe entre 0,05 % et 0,10 % en concentration massique.
Comment fonctionne la solubilisation micellaire ?
Le principe actif hydrophobe s’insère à l’intérieur des micelles, entre les chaînes hydrophobes des surfactifs. Puisque les micelles sont elles-mêmes solubles dans l’eau (grâce à leur couronne hydrophile externe), la substance devient indirectement soluble dans le milieu aqueux.
Il existe deux types de structures micellaires :
- Les micelles sphériques : les plus courantes, avec le cœur hydrophobe au centre
- Les micelles lamellaires : en feuillets, présentes à des concentrations plus élevées
À l’équilibre, le principe actif se répartit entre la phase aqueuse et la phase micellaire. La fraction incorporée dans les micelles est proportionnelle à leur concentration.
Avantages et Inconvénients des Solutions Micellaires
Avantages :
- Augmentation significative de la solubilité apparente
- Procédé relativement simple à mettre en œuvre
- Applicable à de nombreuses molécules hydrophobes
Inconvénients à considérer :
- La biodisponibilité peut être modifiée : la position du principe actif dans la micelle influence directement sa libération
- L’activité et la toxicité du principe actif peuvent être altérées
- Les agents de surface peuvent interférer avec le dosage analytique du médicament
III. Les Cyclodextrines : Des Molécules Cages au Service de la Solubilisation
Origine et Structure des Cyclodextrines
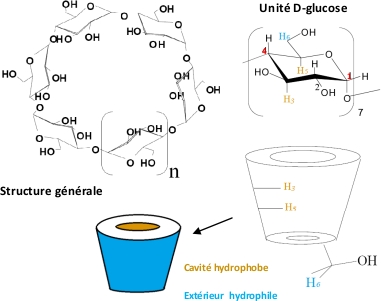
Les cyclodextrines sont des oligosaccharides cycliques issus de la dégradation enzymatique de l’amidon. Leur structure tridimensionnelle caractéristique ressemble à un cône tronqué dont l’extérieur est hydrophile et la cavité interne hydrophobe.
On distingue trois types naturels selon le nombre d’unités glucose liées par des liaisons α-1,4 :
- α-cyclodextrine : 6 unités glucose — la plus petite, cavité étroite
- β-cyclodextrine : 7 unités glucose — la plus utilisée en pharmacie
- γ-cyclodextrine : 8 unités glucose — la plus grande cavité, bonne tolérance orale
Comment les Cyclodextrines Améliorent-elles la Solubilité ?
La cyclodextrine agit comme une molécule cage : elle encapsule la molécule hydrophobe dans sa cavité interne, formant un complexe d’inclusion. La face externe hydrophile permet alors au complexe de se dissoudre facilement dans un milieu aqueux.
Lors de l’administration par voie orale, la libération du principe actif est facilitée par l’affinité naturelle de la muqueuse intestinale (riche en lipides) pour la molécule encapsulée. La dissociation du complexe est favorisée car la liaison cyclodextrine/principe actif est non covalente.
Formulation et Préparation des Complexes
Critères de sélection de la cyclodextrine :
- La taille de la cavité doit être adaptée à la taille du principe actif
- L’augmentation de solubilité dans l’eau doit être significative
- La stabilité du complexe formé doit être suffisante pour résister au stockage
Méthode de préparation générale :
- Ajout d’un excès de molécule lipophile à une solution aqueuse de cyclodextrine
- Agitation de la suspension pendant une durée pouvant aller jusqu’à une semaine
- Séparation du complexe par filtration ou centrifugation
- Obtention d’une forme solide par lyophilisation
Les Nombreux Avantages des Cyclodextrines
Les cyclodextrines offrent un profil d’avantages particulièrement intéressant :
- Amélioration de la solubilité aqueuse des principes actifs hydrophobes
- Augmentation de la vitesse de dissolution
- Amélioration de l’absorption et de la biodisponibilité
- Diminution des effets secondaires locaux
- Masquage du goût et de l’odeur désagréables
- Protection des substances sensibles à la lumière et à l’oxygène
Exemple concret : L’itraconazole (antifongique à faible solubilité) est commercialisé sous forme de complexe avec la 2-hydroxypropyl-β-cyclodextrine (Sporanox® solution orale), ce qui permet d’améliorer drastiquement son absorption intestinale.
Limites et Contraintes des Cyclodextrines
Malgré leurs avantages, les cyclodextrines présentent plusieurs limitations :
- Sensibilité microbienne : les conservateurs risquent de former des complexes d’inclusion et de perdre leur efficacité
- Compétition moléculaire : les molécules hydrophobes endogènes (lipides, cholestérol) peuvent entrer en compétition avec le principe actif
- Les cyclodextrines naturelles ont une solubilité limitée et une toxicité orale non négligeable, ce qui a conduit à leur modification chimique (hydroxypropylation, méthylation)
- L’administration orale peut provoquer des irritations gastro-intestinales par extraction des lipides membranaires intestinaux
- Le coût de fabrication élevé limite le nombre de spécialités disponibles sur le marché
IV. Les Dispersions Solides : La Dispersion Moléculaire du Principe Actif
Définition et Concept
Une dispersion solide est une dispersion d’un ou plusieurs principes actifs dans un support inerte (véhicule) à l’état solide. Le but ultime est d’obtenir une dispersion à l’état moléculaire, maximisant ainsi la surface de contact entre le principe actif et le milieu de dissolution.
Il existe deux grandes familles :
- Les mélanges eutectiques : microcristaux des deux composants imbriqués, présentant un point de fusion unique inférieur à celui de chaque composant seul
- Les solutions solides : dispersion au niveau moléculaire du principe actif dans le vecteur solide (aussi appelées « cristaux mixtes »)
Comment Choisir le Bon Véhicule ?
Le choix du véhicule est déterminant pour l’efficacité de la dispersion solide. Il doit répondre à plusieurs exigences :
- Grande hydrosolubilité pour libérer rapidement le principe actif
- Innocuité physiologique totale
- Inertie chimique vis-à-vis du principe actif
- Stabilité thermique suffisante
- Point de fusion bas (inférieur à 200°C) pour éviter la dégradation thermique
Les véhicules les plus utilisés en pratique :
- Polymères : PVP, PEG, HPMC, HEC, Eudragit — les PEG 4000, 6000 et 20 000 sont les transporteurs les plus populaires
- Sucres : dextrose, sorbitol, maltose, xylose
- Acides organiques : acide citrique, acide succinique
- Surfactifs : Tweens, Spans, stéarate de PEG
Les Méthodes de Préparation des Dispersions Solides
La Méthode Hot Melt (Fusion à Chaud)
Le principe actif et le vecteur sont fondus ensemble à une température supérieure à celle de l’eutectique, puis le mélange est refroidi brusquement, pulvérisé et tamisé.
Avantage principal : Procédé simple, sans solvant, économique.
Limites :
- Nécessite une miscibilité parfaite des deux composants à l’état liquide
- Inapplicable si l’un des composants est thermosensible
La Méthode du Solvant (Coprécipitation)
Le principe actif et le vecteur sont co-dissous dans un solvant organique commun (éthanol, acétone, chloroforme), puis le solvant est éliminé par évaporation. Le résidu solide est ensuite pulvérisé et tamisé.
Avantages :
- Applicable aux molécules thermolabiles (procédé entre 23 et 65°C)
- Permet l’utilisation de polymères à point de fusion élevé
- Dispersion moléculaire de qualité supérieure
Limitations importantes :
- Nécessité d’éliminer totalement le solvant résiduel avant administration
- Problèmes environnementaux liés à l’utilisation de solvants organiques toxiques
- Difficulté de contrôle de la complète élimination du solvant
La Méthode Mixte
Combinaison des deux approches précédentes pour tirer parti des avantages de chacune.
Mécanisme d’Action des Dispersions Solides
Lorsqu’une dispersion solide est mise en contact avec un milieu aqueux (fluides digestifs) :
- Pour les mélanges eutectiques : le vecteur se dissout rapidement, libérant de très fins cristaux de principe actif à grande surface spécifique
- Pour les solutions solides : le vecteur se solubilise et le principe actif se disperse à l’échelle moléculaire dans la solution, maximisant sa biodisponibilité
Résultat concret : Des études ont démontré qu’une dispersion solide peut multiplier par 2 à 3 fois la vitesse de dissolution et la solubilité apparente d’un principe actif par rapport à sa forme cristalline pure.
Limites des Dispersions Solides
- Difficultés de transposition à l’échelle industrielle (passage du laboratoire à la production)
- Instabilité physique lors de la fabrication et du stockage (recristallisation du principe actif, phénomènes de vieillissement)
- Nécessité de contrôles analytiques rigoureux pour garantir l’homogénéité de la dispersion
V. Tableau Comparatif des Trois Approches
| Critère | Solutions Micellaires | Cyclodextrines | Dispersions Solides |
|---|---|---|---|
| Mécanisme | Encapsulation dans micelles | Complexe d’inclusion | Dispersion moléculaire |
| Forme finale | Liquide | Solide / Liquide | Solide |
| Coût | Faible | Élevé | Moyen |
| Biodisponibilité | Variable | Bonne | Très bonne |
| Stabilité | Modérée | Bonne | Délicate |
| Administration | Orale / Parentérale | Orale / Topique | Orale |
Conclusion : Choisir la Bonne Stratégie pour Optimiser la Solubilité
L’amélioration de la solubilité des principes actifs hydrophobes est un enjeu central du développement pharmaceutique moderne. Chaque approche — micellaire, cyclodextrine ou dispersion solide — présente un profil avantages/inconvénients spécifique qui oriente le choix du formulateur.
Points clés à retenir :
- Les solutions micellaires sont simples à mettre en œuvre mais peuvent modifier la biodisponibilité du principe actif
- Les cyclodextrines offrent de nombreux avantages (stabilité, masquage du goût, biodisponibilité) mais leur coût reste élevé
- Les dispersions solides constituent l’approche la plus puissante pour la libération orale, mais nécessitent une maîtrise rigoureuse du procédé de fabrication et du stockage
Le choix de la stratégie dépendra des propriétés physicochimiques du principe actif, de la voie d’administration visée, des contraintes réglementaires et économiques, et des objectifs thérapeutiques fixés.