Antalgiques du Troisième Palier : Tout Comprendre sur les Opioïdes Forts en Pharmacologie
La douleur intense est l’une des expériences les plus invalidantes pour un être humain. Lorsque les antalgiques classiques ne suffisent plus, les médecins ont recours aux molécules les plus puissantes de leur arsenal thérapeutique : les antalgiques du troisième palier, encore appelés opioïdes forts.
En France, près de 12 millions de personnes se sont vu prescrire des antalgiques opioïdes en 2024, et la douleur chronique touche entre 20 et 30 % de la population totale. Face à ces chiffres, comprendre le mécanisme, la chimie et les enjeux de ces médicaments est devenu une nécessité pour tout professionnel de santé.
Dans cet article, nous explorons en détail les bases pharmacologiques, la structure chimique, les principaux représentants et les risques associés aux antalgiques du palier III.

1. La Douleur et sa Classification : les Bases
Qu’est-ce que la douleur ?
Selon l’Association Internationale pour l’Étude de la Douleur (IASP), la douleur est définie comme une expérience sensorielle et émotionnelle désagréable, liée à des lésions tissulaires réelles ou potentielles (1979).
Cette définition met en avant deux dimensions essentielles :
- Sensorielle : la douleur est un signal d’alarme biologique.
- Émotionnelle : elle retentit sur la psychologie du patient et sa qualité de vie.
Les deux grands types de douleur
Il existe deux catégories principales :
- La douleur par excès de nociception : provoquée par une stimulation excessive des récepteurs périphériques (traumatisme, cancer, chirurgie). C’est la forme la plus fréquente.
- La douleur psychogène : sans lésion organique détectable. Elle est liée au psychisme et nécessite une prise en charge spécifique.
La nociception, système d’alarme du corps
La nociception désigne l’ensemble des processus biologiques permettant à l’organisme de détecter, transmettre et interpréter un stimulus douloureux. Les nocirécepteurs (musculaires, articulaires ou cutanés) captent le message et l’acheminent vers le cerveau via les fibres nerveuses. Ce signal n’est transmis que si l’intensité de la stimulation dépasse un certain seuil.
2. La Classification OMS des Antalgiques : L’Échelle en Trois Paliers
En 1984, l’Organisation Mondiale de la Santé (OMS) a établi un protocole en trois paliers pour guider la prescription des antalgiques selon l’intensité de la douleur.

| Palier | Classe | Indication |
|---|---|---|
| I | Antalgiques périphériques (paracétamol, AINS, aspirine) | Douleur légère à modérée |
| II | Antalgiques centraux faibles (tramadol, codéine) | Douleur modérée à sévère |
| III | Antalgiques centraux forts (morphine, fentanyl, méthadone) | Douleur très sévère, rebelle |
Ce guide est d’une importance capitale en pratique clinique. Les antalgiques du palier III sont réservés aux douleurs qui résistent aux deux premiers paliers, notamment dans les contextes oncologiques, postopératoires lourds ou de soins palliatifs.
3. Histoire et Origine des Opioïdes : De l’Opium à la Morphine
L’opium, le plus ancien analgésique de l’humanité
L’utilisation médicinale de l’opium remonte à l’Antiquité. Il est extrait du latex de la capsule de pavot (Papaver somniferum), une plante cultivée depuis des millénaires en Asie centrale et en Méditerranée.

La composition chimique de l’opium
La caractérisation chimique de l’opium a révélé sa composition complexe :
- Morphine : principal alcaloïde (~50 % de la fraction alcaloïdique)
- Codéine
- Thébaïne : précurseur de nombreux dérivés hémisynthétiques
- Papavérine et Narcotine : alcaloïdes aux propriétés distinctes
La paille de pavot contient entre 1 et 6 % d’alcaloïdes totaux, dont environ la moitié est de la morphine.
Isolation de la morphine : une révolution en 1806
C’est en 1806 que le pharmacien allemand Friedrich Sertürner isola pour la première fois la morphine à partir de l’opium. Cette molécule devint rapidement la référence absolue parmi les analgésiques opioïdes, un statut qu’elle conserve encore aujourd’hui.
4. La Morphine : Structure, Chimie et Mécanisme d’Action
Structure chimique de la morphine
La morphine a pour formule brute C₁₇H₁₉NO₃ (établie en 1847) et sa structure définitive a été déterminée en 1925.
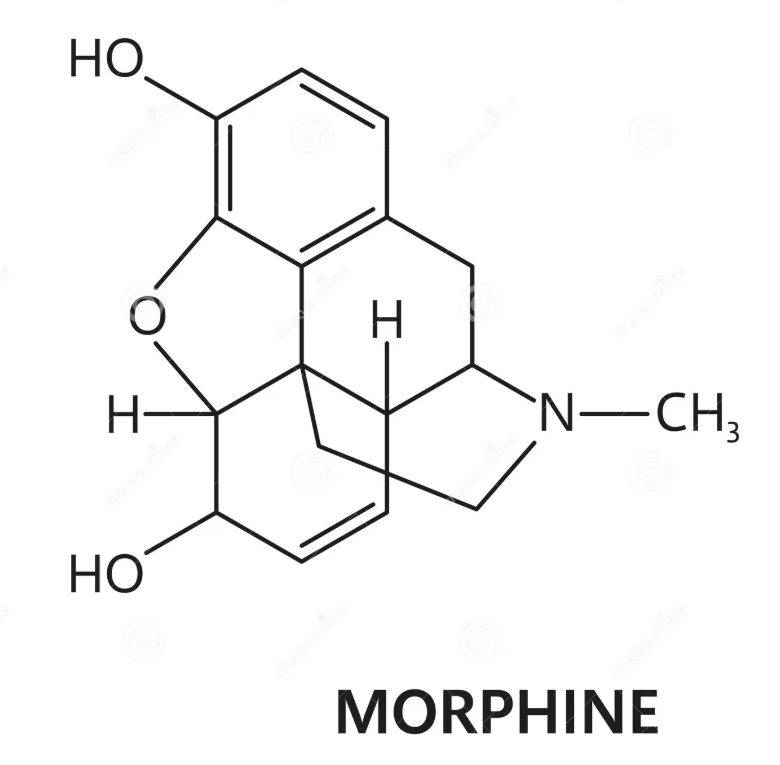
Son architecture est fondée sur le noyau morphinane, composé de cinq cycles :
- Cycle A : phényle, portant un groupement phénol en C3 (indispensable à l’activité)
- Cycle B : cyclohexane
- Cycle C : cyclohexène, portant une fonction alcool secondaire en C6
- Cycle D : pipéridine N-méthylée (cycle ponté)
- Cycle E : 2,3-dihydrofurane
Stéréochimie de la morphine
La morphine possède 5 centres chiraux (positions 5, 6, 9, 13 et 14). Cette configuration spatiale précise est essentielle à son activité pharmacologique. Seul l’énantiomère lévogyre (-) est biologiquement actif.
Propriétés physico-chimiques
- Poudre cristalline blanche, point de fusion à 230°C
- Amine tertiaire, monobasique → forme facilement des sels solubles (chlorhydrate, sulfate)
- Pouvoir rotatoire lévogyre : entre -107° et -115°
Identification chimique : réactions caractéristiques
Deux tests permettent d’identifier la morphine en laboratoire :
- Réaction au réactif sulfo-formaldéhyde → coloration pourpre virant au violet
- Réaction avec le perchlorure de fer → coloration bleue caractéristique (due au phénol en C3)
5. Les Récepteurs aux Opioïdes : Cibles Moléculaires
Trois familles de récepteurs
Les récepteurs aux opioïdes sont des récepteurs à 7 hélices transmembranaires, couplés à des protéines G hétérotrimériques (sous-unités α, β, γ). On distingue trois sous-types :
- Récepteurs μ (mu) : cibles principales de la morphine → analgésie, euphorie, dépendance, dépression respiratoire
- Récepteurs κ (kappa) → analgésie spinale, sédation
- Récepteurs δ (delta) → modulation de l’humeur, analgésie
Les ligands endogènes naturels
L’organisme produit ses propres molécules capables d’activer ces récepteurs :
- Endorphines → affinité principale pour les récepteurs μ
- Dynorphines → affinité principale pour les récepteurs κ
- Enképhalines → affinité principale pour les récepteurs δ
La morphine agit en se substituant à ces ligands endogènes, en particulier au niveau pré-synaptique, inhibant ainsi la libération de la substance P, médiateur clé de la transmission nociceptive.
6. Mécanisme d’Action et Classification des Opioïdes
Trois modes d’action sur les récepteurs
Selon leur interaction avec les récepteurs opioïdes, les molécules sont classées en trois catégories :
Agonistes purs (ex : morphine, fentanyl) Ils se lient directement aux récepteurs et reproduisent tous les effets de la morphine. L’augmentation des doses produit une augmentation proportionnelle de l’effet (pas d’effet plafond).
Agonistes partiels / agonistes-antagonistes (ex : buprénorphine, pentazocine) Leur efficacité maximale est limitée (effet plafond). Ils peuvent réduire l’effet d’un agoniste pur s’ils occupent la place sur le récepteur.
Antagonistes (ex : naloxone) Ils se fixent sur les récepteurs sans les activer, empêchant l’action des agonistes. La naloxone est l’antidote de référence en cas d’intoxication aux opioïdes.
7. Relation Structure-Activité (RSA) de la Morphine
Comprendre quels groupements chimiques sont responsables de l’activité permet de concevoir de meilleures molécules.
Groupements essentiels
- L’hydroxyle phénolique en C3 : indispensable à l’activité analgésique. Sa substitution (ex. codéine = méthylation) réduit fortement l’effet.
- Le cycle aromatique (A) : capital. Toute molécule en étant dépourvue est inactive.
- L’atome d’azote : déterminant. Sans azote, toute activité disparaît. Le groupement N-méthyle favorise le passage de la barrière hémato-encéphalique.
Groupements modulables
- La fonction alcool en C6 : non indispensable. Sa suppression ou masquage ne diminue pas l’activité.
- Le pont éther : non strictement nécessaire pour l’activité analgésique.
8. Effets Secondaires et Risques de la Morphine
Effets secondaires centraux
- Euphorie et sédation
- Dépression respiratoire (effet le plus dangereux en cas de surdosage)
- Hypotension orthostatique
- Myosis (rétrécissement de la pupille : signe clinique clé d’intoxication)
- Nausées et vomissements
Effets secondaires périphériques
- Constipation (effet quasi-constant, lié à l’action sur les récepteurs intestinaux)
- Spasme biliaire
- Libération d’histamine → vasodilatation et prurit
Risques à long terme
Lors d’une administration prolongée, deux phénomènes majeurs se développent :
- La dépendance physique et psychique : l’arrêt brutal entraîne un syndrome de sevrage (anxiété, douleurs musculaires, insomnie, diarrhée).
- La tolérance : diminution progressive de la réponse pharmacologique nécessitant l’augmentation des doses.
⚠️ En France, les hospitalisations liées aux opioïdes ont augmenté de 167 % entre 2000 et 2017 (ANSM). La vigilance est essentielle, même si la situation reste loin de la crise américaine.
9. Les Principaux Antalgiques du Palier III : Présentation
La Morphine : la référence
Indications principales :
- Douleurs postopératoires intenses
- Douleurs cancéreuses sévères et rebelles
- Soins palliatifs
Formes disponibles :
- Libération immédiate : 5–10 mg toutes les 4h (voie orale, IV, SC, péridurale)
- Libération prolongée : 30 mg toutes les 12h (voie orale)
La Péthidine (Mépéridine) : le premier synthétique
La péthidine est le premier opioïde entièrement de synthèse. Sa structure est celle d’un ester de pipéridine (chlorhydrate de 1-méthyl-4-phénylpipéridine-4-carboxylate d’éthyle).
Profil pharmacologique comparé à la morphine :
- Environ 10 fois moins puissante sur la douleur
- Beaucoup moins constipante
- Moins émétisante
- Mais même niveau de sédation et de dépression respiratoire
Elle possède également des propriétés spasmolytiques atropiniques, ce qui la rend utile dans certaines situations spécifiques. Elle est disponible en ampoules de 10 mg (voie IM et IV).
La Méthadone : l’opioïde de substitution
Structure : Chlorhydrate de (6RS)-6-(diméthylamino)-4,4-diphénylheptan-3-one
La méthadone possède un seul centre chirale :
- Énantiomère R : 2 fois plus actif que la morphine
- Énantiomère S : inactif
Avantages par rapport à la morphine :
- Moins de nausées et de constipation
- Syndrome de sevrage moins prononcé (demi-vie prolongée)
- Sédation et euphorie atténuées
Utilisation principale : traitement de substitution aux opiacés (pharmacodépendance), administrée par voie orale (sirop, gélules) à raison d’une prise par 24 heures.
La Pentazocine : l’agoniste-antagoniste mixte
La pentazocine est un agoniste κ / antagoniste partiel μ. Son profil original résulte de son substituant allylique sur l’azote (à l’origine de l’antagonisme μ).
- 30 mg de pentazocine ≈ 10 mg de morphine en termes d’analgésie
- Intéressante en cas de problème de toxicomanie avérée
- Utilisée dans les douleurs chroniques sévères
La Buprénorphine (Temgesic®) : une molécule hautement lipophile
La buprénorphine est un agoniste partiel à haute affinité des récepteurs μ et antagoniste des récepteurs κ et δ. Sa structure est dérivée de la thébaïne, avec plusieurs modifications clés :
- Méthylation de l’hydroxyle en C6
- Radical méthylcyclopropane sur l’azote (responsable de l’antagonisme κ/δ)
- Radical 3,3-diméthylbutan-2-ol en C7
- Pont éthylène entre C6 et C14
Caractéristiques pharmacologiques notables :
- Très liposoluble → excellente pénétration cérébrale → plus puissante que la morphine à faibles doses
- Très peu d’effets sur la respiration (avantage majeur de sécurité)
- Effet plafond (limite le risque de surdose)
Indications :
- Douleurs postopératoires et néoplasiques
- Traitement de substitution aux opiacés
Formes disponibles :
- Injectable (ampoules de 0,3 mg, voie SC/IM/IV)
- Sublinguale (comprimés à 0,2 mg) pour usage ambulatoire
Les Propionanilides : réservés à l’anesthésie
Les propionanilides (famille des 4-anilino-pipéridines, analogues structuraux de la péthidine) ont une demi-vie très courte, ce qui en fait des outils précieux en anesthésie générale. Ils permettent un réveil rapide après l’acte opératoire et réduisent le risque de dépression respiratoire post-opératoire.
10. Contexte Actuel : Opioïdes et Enjeux de Santé Publique
Une consommation en hausse en France
En 2024, les opioïdes représentent 22 % de la consommation totale d’antalgiques en France. Les ventes d’opioïdes forts (morphine, oxycodone) ont progressé de 59 % depuis 2010.
Malgré cela, seulement 37 % des Français souffrant de douleurs chroniques se déclarent satisfaits de leur prise en charge — ce qui souligne le besoin de trouver un meilleur équilibre thérapeutique.
La France n’est pas les États-Unis
La situation française reste éloignée de la crise nord-américaine, où plus de 800 000 décès par surdose ont été enregistrés en 25 ans. En France, la prescription est strictement encadrée, la publicité auprès du grand public est interdite, et la situation est activement surveillée par l’ANSM.
La Haute Autorité de Santé (HAS) a publié en 2022 de nouvelles recommandations sur le bon usage des opioïdes. Un nouveau plan national de lutte contre la douleur est réclamé par la communauté scientifique, le dernier remontant à 2006–2010.
Conclusion et Points Clés à Retenir
Les antalgiques du troisième palier sont des molécules pharmacologiquement complexes, indispensables dans la prise en charge des douleurs sévères. Leur compréhension nécessite de maîtriser à la fois leur chimie structurale, leur mécanisme d’action réceptoriel et leur profil de tolérance.
Ce qu’il faut retenir :
- La morphine est la molécule de référence des opioïdes forts, dont l’activité dépend de l’hydroxyle phénolique en C3, du cycle aromatique et de l’atome d’azote.
- Les opioïdes agissent sur trois types de récepteurs (μ, κ, δ), avec des profils d’action variables selon les molécules.
- Chaque dérivé (péthidine, méthadone, buprénorphine, pentazocine) présente un profil pharmacologique propre permettant d’adapter la thérapeutique.
- La dépendance et la tolérance sont des effets inhérents à l’usage prolongé de cette classe médicamenteuse.
- En France, l’usage des opioïdes est en hausse et requiert une vigilance accrue des prescripteurs comme des patients.
📌 Pour aller plus loin : consultez les recommandations de la HAS sur le bon usage des opioïdes (2022) et les travaux de la SFETD (Société Française d’Étude et de Traitement de la Douleur) pour une mise à jour régulière des pratiques cliniques.



