Spectrométrie RMN ¹H : Principes, Techniques et Applications en Pharmacie
La Résonance Magnétique Nucléaire (RMN) est aujourd’hui l’une des techniques analytiques les plus puissantes et les plus utilisées dans le monde scientifique. Que vous soyez étudiant en pharmacie, chercheur ou professionnel de l’industrie, comprendre les fondements de la RMN ¹H est essentiel pour maîtriser l’analyse structurale des molécules organiques.
Dans cet article, nous allons explorer pas à pas le principe de la RMN du proton, son appareillage, l’interprétation des spectres et ses applications concrètes dans le domaine pharmaceutique et médical.

I. Qu’est-ce que la RMN ? Une technique spectroscopique de référence
La Résonance Magnétique Nucléaire (RMN) est une technique spectroscopique qui exploite les propriétés magnétiques de certains noyaux atomiques. Elle repose sur la mesure de l’absorption d’un rayonnement radiofréquence par un noyau atomique placé dans un champ magnétique intense.
Elle constitue une méthode de référence pour la détermination structurale des molécules organiques et inorganiques, car elle donne accès à des informations précises sur l’environnement chimique de chaque atome dans une molécule.
💡 Le saviez-vous ? La spectroscopie RMN naît en 1946 grâce aux travaux de Felix Bloch et Edward Mills Purcell, qui reçurent le Prix Nobel de Physique en 1952 pour cette découverte fondamentale.
Quelques chiffres clés sur la RMN dans le monde
- Plus de 62 % des laboratoires pharmaceutiques mondiaux s’appuient sur des spectromètres RMN pour la validation de structures moléculaires et le profilage des impuretés.
- Environ 48 % des instituts de recherche en sciences de la vie ont augmenté leur adoption de systèmes RMN à haut champ.
- Le marché mondial de la spectroscopie moléculaire (dont la RMN est un segment majeur) était estimé à 2,87 milliards USD en 2024, avec un taux de croissance prévu de 3,72 % par an jusqu’en 2029.
II. La RMN dans les Pharmacopées : une reconnaissance officielle
La RMN est une méthode officiellement reconnue et encadrée par les grandes pharmacopées internationales. Elle est inscrite dans la Pharmacopée Européenne (10ème édition) sous la référence 2.2.33 — Spectrométrie de résonance magnétique nucléaire.
Les noyaux analysés de façon courante en pharmacie sont :
- ¹H (proton) — le plus utilisé
- ¹³C (carbone-13)
- ¹⁹F (fluor-19)
- ³¹P (phosphore-31)
Cette reconnaissance officielle confirme le statut incontournable de la RMN dans le contrôle qualité et l’identification des substances pharmaceutiques.
III. Principes Généraux de la RMN
Pour comprendre comment fonctionne la RMN, il faut d’abord s’intéresser aux propriétés des noyaux atomiques.
a) Le noyau atomique et ses propriétés magnétiques
Un noyau atomique est constitué de nucléons (protons et neutrons). Deux caractéristiques clés le définissent :
- A : le nombre de masse (protons + neutrons)
- Z : le nombre de charge (protons)
Certains noyaux se comportent comme de petits aimants. C’est le cas du proton ¹H : c’est une particule chargée qui tourne sur elle-même, ce qui lui confère un moment magnétique noté μ.
b) Le spin nucléaire « I » : clé d’entrée en RMN
Le spin nucléaire est le nombre quantique qui détermine si un noyau est actif en RMN. Il dépend de la composition du noyau :
| Noyau | Spin I | Actif en RMN ? |
|---|---|---|
| ¹H, ¹³C, ¹⁹F, ³¹P | 1/2 | ✅ Oui |
| ²H, ¹⁴N | 1 | ✅ Oui |
| ¹²C, ¹⁶O | 0 | ❌ Non |
Un noyau est actif en RMN uniquement si son spin est non nul. Les noyaux avec A et Z pairs (comme ¹²C ou ¹⁶O) ont un spin nul et sont donc invisibles en RMN.
c) L’interaction spin nucléaire / champ magnétique
En l’absence de champ magnétique externe, les moments magnétiques de spin sont orientés au hasard — c’est l’état dégénéré.
Lorsqu’on applique un champ magnétique statique H₀, les moments magnétiques s’alignent selon la direction du champ. Il en résulte deux états d’énergie distincts pour le proton (I = 1/2) :
- État α (parallèle à H₀) → basse énergie (favorable)
- État β (antiparallèle à H₀) → haute énergie (défavorable)
Chaque moment magnétique décrit alors un mouvement de précession autour de H₀ à la fréquence de Larmor : ν₀ = γH₀ / 2π
d) La radiofréquence et le phénomène de résonance
La résonance se produit lorsqu’on applique une onde radiofréquence (RF) dont la fréquence est exactement égale à la fréquence de Larmor du noyau. Cette onde provoque la transition du noyau de l’état α (basse énergie) vers l’état β (haute énergie).
Exemple concret : Pour le proton ¹H avec un champ H₀ de 1,4 Tesla, la fréquence de résonance est de 60 MHz — soit dans la gamme des ondes radio.
Après l’arrêt de l’impulsion RF, les noyaux excités reviennent à leur état d’équilibre : c’est le phénomène de relaxation, qui génère le signal RMN enregistré.
💡 En pratique : La relation fondamentale de la RMN est ν = γH₀ / 2π. Plus le champ magnétique H₀ est fort, plus la fréquence de résonance est élevée, et plus la résolution du spectre est grande.
IV. Réalisation d’une Analyse RMN ¹H : Mode Opératoire
Préparation de l’échantillon
Une analyse RMN du proton nécessite une préparation rigoureuse de l’échantillon :
- Dissoudre 10 à 50 mg de substance dans un solvant deutéré (sans protons actifs), comme :
- CDCl₃ (chloroforme deutéré) — le plus courant
- DMSO-d₆
- D₂O (eau deutérée)
- CD₃OD (méthanol deutéré)
- Ajouter une petite quantité de TMS (tétraméthylsilane) comme étalon interne.
- Placer l’échantillon dans un tube en verre fin (5 mm de diamètre standard).
- Mettre le tube en rotation au centre de la bobine magnétique.
Pourquoi des solvants deutérés ? Les solvants ordinaires contiennent des protons ¹H qui satururaient le spectre. En remplaçant les hydrogènes par du deutérium (²H, spin I = 1, différent du proton), le solvant devient “invisible” en RMN du proton.
Déroulement de l’analyse
- Le champ H₀ aligne les spins des protons de l’échantillon.
- La bobine de radiofréquences envoie une impulsion RF à la fréquence de résonance.
- Le signal de réponse (FID — Free Induction Decay) est enregistré et transformé par transformée de Fourier pour obtenir le spectre.
V. L’Appareillage RMN : du Cryostat au Spectromètre
Un spectromètre RMN moderne est composé de plusieurs éléments essentiels :
- Un aimant supraconducteur qui génère le champ magnétique H₀ (fort, homogène et stable)
- Une chaîne d’émission qui produit les impulsions radiofréquences
- Une bobine qui transmet les impulsions à l’échantillon et recueille le signal
- Une chaîne de réception qui amplifie le signal
- Un ordinateur qui gère l’ensemble et traite les données
L’aimant supraconducteur : cœur technologique de la RMN
L’aimant supraconducteur est la pièce centrale du spectromètre. Il est constitué de fils supraconducteurs en NbTi (Niobium-Titane) ou Nb₃Sn (Niobium-Étain), refroidis à des températures extrêmement basses grâce à un système cryogénique :
- Hélium liquide (-269°C / 4,2 K) : assure la supraconductivité (résistance électrique nulle, pas d’effet Joule)
- Azote liquide (-196°C) : réduit le gradient thermique et limite l’évaporation de l’hélium
💡 Évolution technologique : Aujourd’hui, environ 55 % des instruments RMN nouvellement installés intègrent des fonctionnalités d’automatisation avancées, réduisant les interventions manuelles et augmentant le débit d’échantillons.
VI. Lecture et Interprétation du Spectre RMN ¹H
Le spectre RMN ¹H représente l’intensité du signal en fonction du déplacement chimique (δ) en ppm. Son interprétation repose sur quatre paramètres fondamentaux.
1. Le Déplacement Chimique (δ) : identifier l’environnement des protons
Le déplacement chimique traduit l’effet des électrons voisins sur le proton :
- Les groupes électroattracteurs (F, Cl, OH, OR, CN…) réduisent la densité électronique autour du proton → déblindage → signal déplacé vers les grandes valeurs de δ (gauche du spectre)
- Les groupes électrodonneurs (alkyles, métaux) augmentent la densité électronique → blindage → signal déplacé vers les petites valeurs de δ (droite du spectre)
Exemple concret : Dans l’éthanoate de méthyle (CH₃–COO–CH₃) :
- Le CH₃ lié au carbone carbonyle résonne à 2,06 ppm
- Le CH₃ lié à l’oxygène de l’ester résonne à 3,6 ppm (plus déblindé car l’oxygène est plus électronégatif)
Le TMS : référence universelle du déplacement chimique
Le tétraméthylsilane Si(CH₃)₄ est utilisé comme référence interne (δ = 0 ppm) pour les raisons suivantes :
- Ses 12 protons sont tous équivalents → un seul signal intense
- Il résonne à champ fort → bien séparé des autres signaux
- Il est chimiquement inerte et très volatil (Teb = 20°C)
La formule du déplacement chimique est : δ (ppm) = (ν_échantillon – νₜMS) / νₛpectromètre × 10⁶
2. Les Protons Équivalents : un signal par groupe
Des protons sont dits équivalents s’ils partagent le même environnement chimique et électronique. Ils donnent alors un seul signal sur le spectre.
Le nombre de signaux dans un spectre = nombre de groupes de protons non équivalents dans la molécule.
Exemple : La propanone (acétone) CH₃–CO–CH₃ possède 6 protons, mais ils forment un seul groupe équivalent (les deux CH₃ sont symétriques) → 1 seul signal sur le spectre.
3. L’Intégration : compter les protons
L’aire sous la courbe d’un signal est proportionnelle au nombre de protons responsables de ce signal. L’intégration permet donc de déterminer combien de protons correspondent à chaque signal, et d’identifier la structure de la molécule.
4. La Multiplicité des Signaux : la règle des (n+1)-uplets
Un signal peut être dédoublé ou multiplié par les couplages spin-spin avec les protons voisins. La règle est simple :
Un proton ayant n voisins non équivalents apparaît sous la forme d’un multiplet de (n+1) pics.
| Nom du multiplet | Nombre de pics | n voisins |
|---|---|---|
| Singulet (s) | 1 | 0 |
| Doublet (d) | 2 | 1 |
| Triplet (t) | 3 | 2 |
| Quadruplet (q) | 4 | 3 |
| Quintuplet | 5 | 4 |
Important : Le couplage est stoppé par la présence d’un hétéroatome (différent de H et C). Deux protons sont dits voisins s’ils sont séparés par exactement 3 liaisons.
Récapitulatif : Comment interpréter un spectre RMN ¹H ?
- Compter les signaux → identifier le nombre de groupes de protons non équivalents
- Lire le déplacement chimique (δ) → déterminer la nature des groupes fonctionnels voisins
- Analyser l’intégration → compter le nombre de protons de chaque type
- Étudier la multiplicité → déterminer le nombre de protons voisins
VII. Exemple d’Étude Complète : Identification du C₇H₁₄O
Voici un exemple concret d’utilisation combinée de la spectroscopie IR et de la RMN ¹H pour identifier une molécule inconnue.
Données :
- Formule brute : C₇H₁₄O
- Le spectre IR montre une bande d’absorption caractéristique d’un groupement cétone (C=O)
Analyse du spectre RMN ¹H :
| Signal (δ ppm) | Hauteur intégration | Nombre de H | Interprétation |
|---|---|---|---|
| 0,9 ppm | 18 mm | 9H | 3 groupements –CH₃ équivalents (loin du C=O) |
| 2,1 ppm | 6 mm | 3H | 1 groupement –CH₃ voisin du C=O |
| 2,6 ppm | 4 mm | 2H | 1 groupement –CH₂ voisin du C=O |
Conclusion : La formule semi-développée est celle du 4,4-diméthylpentan-2-one :
(CH₃)₃C – CH₂ – CO – CH₃
VIII. Applications de la RMN ¹H : De la Pharmacie à la Médecine
Applications pharmaceutiques
La RMN est devenue indispensable dans l’industrie pharmaceutique. Elle est utilisée pour :
- La caractérisation structurale des matières premières et des produits finis
- La détection et l’identification des impuretés, même énantiomériques (à un taux supérieur à 10 %)
- L’établissement d’empreintes spectrales (fingerprinting) d’un mélange complexe
- Le couplage HPLC/RMN pour identifier les impuretés et les métabolites dans les fluides biologiques
💡 Application émergente : La technique RMN-DOSY (Diffusion Ordered SpectroscopY) permet d’analyser des médicaments complexes sans séparation préalable de leurs composants. Elle sert notamment à détecter les faux médicaments et les contrefaçons, en générant une véritable empreinte spectrale unique pour chaque formulation.
Environ 64 % des flux de travail de recherche pharmaceutique dépendent de la RMN pour le développement de médicaments et la vérification des composés, ce qui en fait une technologie stratégique pour l’ensemble de la chaîne du médicament.
Limites à connaître
- Nécessite une quantité de produit relativement importante (quelques milligrammes)
- L’appareillage est coûteux à l’achat et à la maintenance
- L’interprétation peut devenir complexe pour les grandes molécules avec de nombreux protons
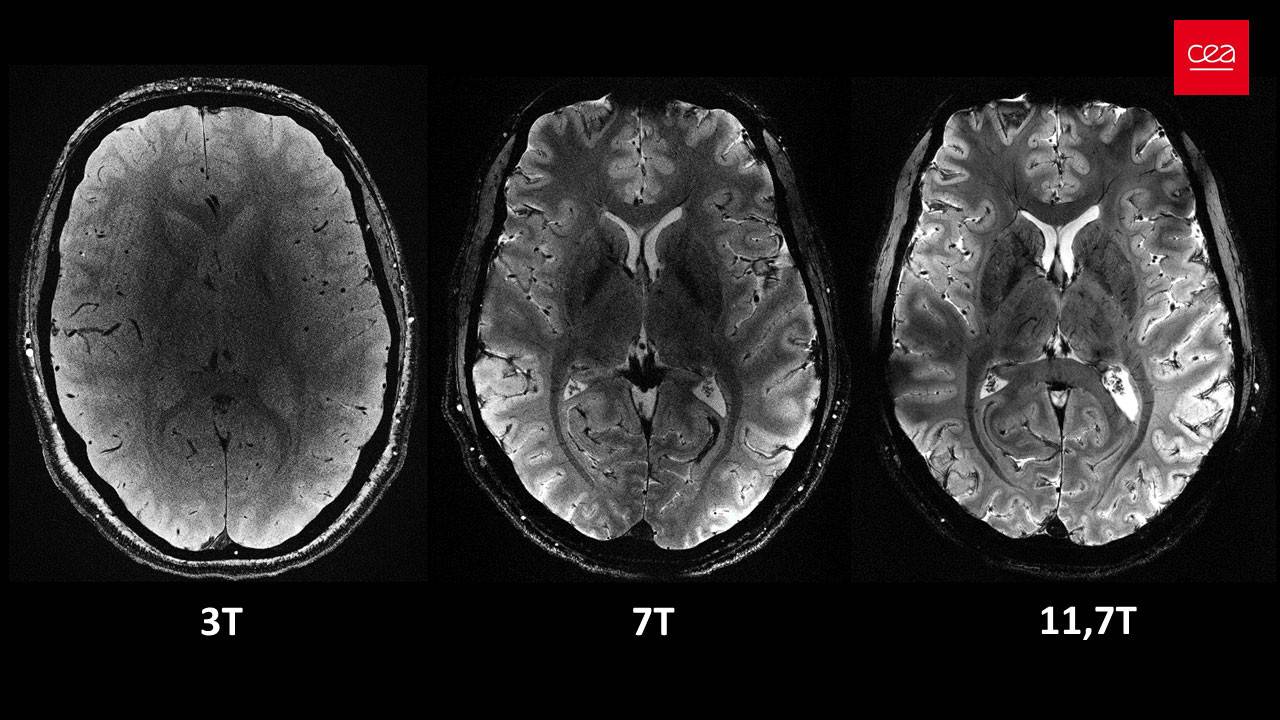
Applications médicales : l’IRM
L’application médicale la plus connue de la RMN est l’Imagerie par Résonance Magnétique (IRM). Ce procédé utilise les mêmes principes physiques que la RMN de laboratoire, mais appliqués au corps humain :
- Des gradients de champ magnétique sont appliqués dans les trois directions de l’espace.
- Les noyaux d’hydrogène de l’eau et des graisses des tissus résonnent à leurs fréquences caractéristiques.
- Les niveaux de gris de l’image représentent l’intensité du signal émis par chaque élément de volume (voxel).
L’IRM permet ainsi de visualiser les tissus mous (cerveau, muscles, articulations) sans irradiation ionisante, contrairement à la radiographie.
Conclusion : La RMN ¹H, un outil analytique incontournable
La Résonance Magnétique Nucléaire du proton (RMN ¹H) est bien plus qu’une simple technique de laboratoire. C’est un véritable outil de déchiffrage moléculaire, capable de révéler l’identité et la structure d’une molécule à partir de signaux aussi simples que des déplacements chimiques, des multiplicités et des intégrations.
En résumé, les 4 points clés à retenir :
- La RMN exploite les propriétés magnétiques des noyaux atomiques actifs (spin ≠ 0)
- Le déplacement chimique (δ, en ppm) renseigne sur l’environnement électronique du proton
- La multiplicité des signaux (règle n+1) révèle le nombre de protons voisins
- L’intégration des signaux permet de compter les protons de chaque groupe



