L’Appareil de Craig et la Séparation à Contre-Courant : Guide Complet
Introduction : Pourquoi la Séparation à Contre-Courant ?
En chimie analytique, séparer les constituants d’un mélange complexe est un défi quotidien. Parmi les nombreuses techniques disponibles — distillation, chromatographie, électrophorèse — la distribution à contre-courant (CCD) occupe une place historique et pédagogique irremplaçable.
Cette méthode repose sur un principe simple mais puissant : répartir une substance entre deux solvants non miscibles, de manière répétée et organisée. Le résultat ? Une séparation fine de molécules aux propriétés très proches.
Dans cet article, vous allez comprendre :
- Le principe fondamental de la technique
- Le fonctionnement détaillé de l’appareil de Craig
- Les bases mathématiques de la distribution binomiale
- Les applications concrètes en pharmacie et biochimie
I. Contexte et Place dans les Techniques de Séparation
Avant de plonger dans le cœur du sujet, rappelons que les méthodes de séparation se classent selon la nature du mélange à traiter :
Pour les mélanges homogènes liquides, on utilise principalement :
- L’extraction par solvant miscible ou non miscible
- La séparation à contre-courant
- La chromatographie et l’électrophorèse
Pour les mélanges hétérogènes, on fait appel à :
- La distillation ou la sublimation (changement d’état)
- La précipitation ou concentration (transfert de phase)
La séparation à contre-courant se positionne donc comme une technique intermédiaire entre l’extraction liquide-liquide simple (entonnoir séparateur) et la chromatographie moderne.

II. Historique : De Craig à la Biochimie Moderne
Lyman C. Craig, le père de la distribution à contre-courant
La distribution à contre-courant (CCD) est une technique de chimie analytique développée par Lyman C. Craig dans les années 1940. Craig a entrepris ses travaux pionniers en étudiant la distribution d’un médicament antipaludéen, la mépacrine (atabrine), entre deux couches d’un système biphasique de solvants.
L’idée est née des frustrations rencontrées lors d’études structurelles sur les alcaloïdes de l’ergot et de la vératrine à la fin des années 1930. En 1943, Craig mit au point un appareil capable de réaliser simultanément 20 extractions quantitatives en une seule étape.
Un rôle décisif pendant la Seconde Guerre mondiale
Avant même d’être largement appliqué aux alcaloïdes, cet appareil fut mobilisé pour répondre à une urgence militaire : prouver la pureté des nouveaux antipaludéens de synthèse avant les essais cliniques. L’appareil de Craig révéla systématiquement des impuretés dans des préparations considérées comme pures par toutes les autres méthodes de séparation alors disponibles.
Un héritage scientifique considérable
Dans le domaine hormonal, la technique a joué un rôle crucial dans l’isolement et l’étude de l’ocytocine, de la vasopressine, de l’ACTH, de l’hormone de croissance, et de nombreuses autres hormones. Elle a également été appliquée avec succès à l’étude de la structure du virus de la mosaïque du tabac et à l’angiotensine.
Jusqu’au développement des techniques chromatographiques modernes plus simples, la distribution à contre-courant était la seule procédure efficace pour l’isolement de nombreux antibiotiques, de l’insuline, d’autres hormones et de vitamines sous forme pure.
III. Principe Fondamental
La base : le coefficient de partage
La séparation à contre-courant est une méthode fondée sur la répartition d’une substance entre deux phases solvantes non miscibles.
Elle permet de séparer les constituants dissous dans une phase initiale en les rassemblant dans des fractions distinctes de solvants.
Règle d’or : La séparation n’est possible que si les substances à séparer ont des coefficients de partage différents dans le système de solvants choisi.
Coefficient de partage (D) — La clé de tout
Le coefficient de partage D est défini comme :
D = CM / CS
Où :
- CM = concentration dans la phase légère (mobile)
- CS = concentration dans la phase lourde (stationnaire)
Plus les coefficients de partage de deux substances sont éloignés l’un de l’autre, plus leur séparation sera facile et complète.
IV. L’Appareil de Craig : Description Détaillée
1. Structure générale
L’appareil de Craig est constitué de deux blocs principaux qui fonctionnent ensemble :
Le bloc inférieur (stationnaire) :
- Creusé de cavités équidistantes numérotées de 0 à 19
- Contient des tubes ouverts à leur extrémité supérieure et calibrés pour contenir le même volume
- Accueille la phase solvante lourde (stationnaire)
Le bloc supérieur (mobile) :
- Cavités numérotées en sens inverse (de 19 à 0)
- Tubes ouverts aux deux extrémités
- Contient la phase solvante légère (mobile)
Le couvercle : muni d’une poignée, il permet de saisir et d’agiter l’appareil pour assurer un mélange efficace.
Point clé : Chaque tube inférieur est en communication avec un tube supérieur. L’ensemble forme une colonne. Le bloc supérieur peut pivoter autour d’un axe vertical pour déplacer la phase légère d’une colonne à la suivante.

2. Préparation de l’appareil
La mise en route suit un protocole rigoureux en 4 étapes :
- Remplissage de tous les tubes du bloc inférieur avec le même volume VS de solvant lourd — sauf le tube 0 qui contient la solution à séparer
- Mise en place du bloc supérieur de façon à superposer les deux tubes N°0
- Introduction d’un volume VM de solvant léger pur dans tous les tubes supérieurs (sans les remplir totalement, pour permettre un mélange efficace)
- Adaptation du couvercle de l’appareil
3. Fonctionnement — Le cycle d’une opération
Chaque opération se déroule en trois temps :
Temps 1 — Agitation : L’appareil est retourné énergiquement. Les deux phases se mélangent et l’équilibre de partition s’établit.
Temps 2 — Repos : L’appareil est laissé au repos jusqu’à ce que les ménisques de séparation coïncident exactement avec le plan de rotation séparant les deux blocs.
Temps 3 — Rotation : Le bloc supérieur est tourné d’un cran vers la gauche (sans agitation). La phase légère avance d’une position, tandis que le bloc inférieur reste immobile.
Ces trois temps constituent une opération complète.
V. Étude Quantitative : La Distribution Binomiale
Notations et hypothèses de travail
Pour l’étude mathématique, on suppose que :
- La phase lourde contient une seule substance dissoute au départ
- Les agitations sont suffisamment énergiques pour atteindre l’équilibre
- Il n’y a aucune perte de solvant
Symboles utilisés :
- VM : volume du solvant léger (tubes supérieurs mobiles)
- VS : volume du solvant lourd (tubes inférieurs stables)
- Q : quantité totale de substance
- QM : quantité dans la phase légère après équilibre
- QS : quantité dans la phase lourde après équilibre
Calcul des fractions Z et Y
Après chaque agitation, la substance se répartit selon deux fractions complémentaires :
- Z = fraction dans la phase légère (mobile) = D·VM / (D·VM + VS)
- Y = fraction dans la phase lourde (stationnaire) = VS / (D·VM + VS)
- Z + Y = 1 (conservation de la matière)
Propriété fondamentale : Z et Y ne dépendent que de D, VM et VS — des constantes dans des conditions opératoires données. Elles sont donc invariables tout au long des opérations, ce qui simplifie considérablement les calculs.
Le développement binomial
Après n opérations, la répartition totale de la substance suit le développement du binôme (Z + Y)ⁿ.
| Nbre d’opérations | Répartition totale |
|---|---|
| 1 | (Z + Y)Q |
| 2 | (Z + Y)²Q |
| 3 | (Z + Y)³Q |
| n | (Z + Y)ⁿQ |
La quantité présente dans la colonne de rang p après n opérations est égale à Tp × Q, où Tp est le (p+1)ème terme du développement du binôme (Z+Y)ⁿ.
Exemple pratique : Après 3 opérations, la colonne n°1 contient une fraction égale à 3Z²Y de la quantité initiale Q.
Interprétation graphique et gaussienne
Deux observations essentielles :
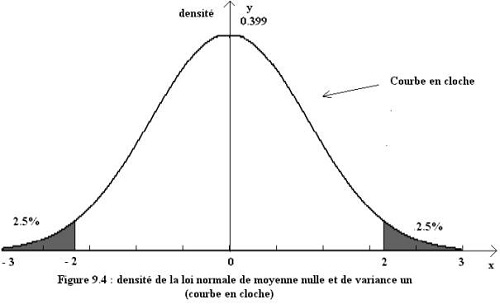
1. Évolution avec n : Lorsque n augmente, la distribution prend une allure gaussienne (courbe en cloche). Certains termes du binôme deviennent si faibles qu’ils ne correspondent plus à des quantités analytiquement détectables — ils sont dits logistiquement négligeables.
2. Influence du coefficient de partage : Pour un même nombre d’opérations (ex. : n=8), des substances ayant des coefficients K’ différents occupent des colonnes distinctes. Bien que quatre étapes ne suffisent pas toujours à séparer les analytes, il est clair qu’en augmentant le nombre de tubes, on finira par les séparer complètement.
VI. Applications Pratiques en Pharmacie et Biochimie
La séparation à contre-courant a permis des avancées majeures dans l’isolement de molécules biologiques complexes. Elle est notamment utilisée pour séparer et purifier :
En biochimie pharmaceutique :
- Vitamines (notamment vitamines liposolubles)
- Hormones : insuline, ocytocine, vasopressine, ACTH, hormone de croissance
- Antibiotiques : pénicilline et dérivés
En chimie des molécules naturelles :
- Polypeptides et protéines
- Acides nucléiques (ARN messager, ARN de transfert)
- Acides biliaires et composés polycycliques
La technique a également été utilisée pour la séparation du taxol, des hydrocarbures polycycliques et de divers acides nucléiques. Les composés aromatiques sont récupérés à partir de la fraction de paraffine des huiles de pétrole et les composés chimiques sont isolés de systèmes aqueux.
Cas concret : Les travaux de Sanger sur la structure de l’insuline — qui lui valurent le prix Nobel — ont bénéficié directement des résultats obtenus grâce à la distribution à contre-courant de Craig.
VII. Comparaison avec la Chromatographie Moderne
Il est légitime de se demander pourquoi l’on étudie encore cette technique alors que la chromatographie existe.
La distribution à contre-courant est instructive car elle introduit l’étudiant au concept fondamental d’équilibration entre phases mobile et stationnaire. Chaque tube correspond à un plateau théorique de la colonne chromatographique, où une équilibration complète a lieu.
Bien que les séparations à contre-courant ne soient plus courantes — les séparations chromatographiques étant bien plus efficaces en termes de résolution, de temps et de facilité d’utilisation — la théorie qui les sous-tend reste précieuse comme introduction à la théorie des séparations chromatographiques.
| Critère | Appareil de Craig | Chromatographie moderne |
|---|---|---|
| Principe | Distribution liquide-liquide | Affinité phase stationnaire |
| Efficacité | Limitée (≤ 1000 tubes) | Très élevée (milliers de plateaux) |
| Temps | Long | Rapide |
| Utilité pédagogique | Excellente | Moindre pour les bases |
Conclusion : Un Outil Fondamental, un Héritage Durable
L’appareil de Craig représente bien plus qu’un simple instrument de laboratoire. C’est un modèle conceptuel qui a posé les bases de la séparation chromatographique moderne.
À retenir :
- La séparation repose sur des coefficients de partage différents
- Les fractions Z et Y sont invariantes dans des conditions données
- La distribution suit un développement binomial qui tend vers une gaussienne
- Le nombre d’opérations et la différence de coefficients K’ déterminent la qualité de la séparation
Sur le principe du modèle original de Craig, plusieurs types d’appareils de distribution à contre-courant ont été construits pour une utilisation avec des solvants organiques et de l’eau. La conception la plus connue est la machine entièrement en verre de Craig et Post, dans laquelle le temps de chaque segment du cycle opératoire ainsi que le nombre de transferts peuvent être programmés.



