Anticorps Monoclonaux en Oncologie : La Révolution Thérapeutique du Cancer
En bref : Les anticorps monoclonaux (AcM) représentent aujourd’hui l’une des avancées les plus significatives dans le traitement du cancer. Précis, ciblés et de plus en plus efficaces, ils transforment la prise en charge oncologique à l’échelle mondiale.
Introduction : Quand le Système Immunitaire Devient une Arme Contre le Cancer
Pendant des décennies, les oncologues n’ont disposé que de trois armes contre le cancer : la chirurgie, la radiothérapie et la chimiothérapie. Ces traitements ont permis de prolonger la survie de nombreux patients, mais ils restent insuffisants face à certaines tumeurs, et leurs effets secondaires peuvent être lourds à supporter.
Aujourd’hui, une nouvelle génération de médicaments change la donne : les anticorps monoclonaux thérapeutiques. Ces molécules issues de la biotechnologie ciblent avec précision les cellules cancéreuses, épargnant ainsi les cellules saines et améliorant significativement la qualité de vie des patients.
Le marché mondial de ces thérapies atteignait déjà 263 milliards de dollars en 2024 et devrait frôler les 720 milliards de dollars d’ici 2032, signe de l’engouement scientifique et médical pour cette approche révolutionnaire.

Qu’est-ce qu’une Biothérapie ? Comprendre les Bases
Définition d’un médicament biologique
Un médicament biologique est toute substance active produite à partir d’une source biologique vivante (cellule, organisme). Sa fabrication et son contrôle qualité nécessitent une combinaison d’analyses physiques, chimiques et biologiques très poussées.
Les biothérapies regroupent une large famille de traitements :
- Les anticorps monoclonaux (AcM)
- Les cytokines (interférons, interleukines)
- Les thérapies cellulaires (cellules CAR-T)
- Les vaccins thérapeutiques contre le cancer
Pourquoi les biothérapies ont-elles révolutionné l’oncologie ?
Contrairement à la chimiothérapie, qui agit de façon non sélective sur toutes les cellules en division (cancéreuses ou saines), une biothérapie cible spécifiquement une molécule à la surface de la cellule tumorale.
Cette précision chirurgicale réduit les dommages aux tissus sains, diminue les effets indésirables et améliore l’efficacité du traitement.
Les Anticorps : Piliers du Système Immunitaire
Qu’est-ce qu’un anticorps ?
Les immunoglobulines (Ig) sont des glycoprotéines produites par le système immunitaire en réponse à la détection d’un corps étranger (l’antigène). Elles sont sécrétées par les plasmocytes lors de la réponse immunitaire adaptative.
Un anticorps possède deux propriétés fondamentales :
- Se lier spécifiquement à un antigène donné
- Activer des fonctions effectrices comme l’activation du complément ou l’opsonisation (marquage des cellules cibles pour leur destruction)
Structure en Y : une architecture précisément conçue
Un anticorps est constitué de 4 chaînes polypeptidiques formant une structure en Y :
- Deux chaînes lourdes (H) identiques
- Deux chaînes légères (L) identiques
- Le tout relié par des ponts disulfures qui assurent la flexibilité de la molécule
Chaque chaîne comporte une région variable (responsable de la reconnaissance de l’antigène) et une région constante (impliquée dans les fonctions effectrices immunitaires).
Les Anticorps Monoclonaux : Définition et Spécificité
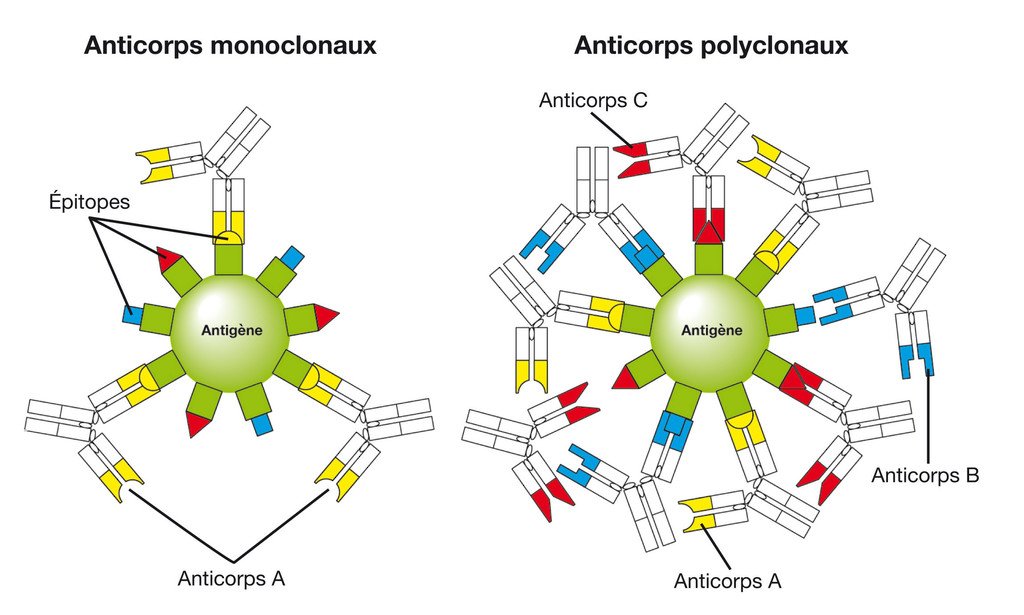
Un anticorps, un seul épitope
Un anticorps monoclonal (AcM) est un anticorps qui reconnaît un seul et unique épitope (site précis) sur un antigène donné. Il est produit par un seul clone de plasmocyte, d’où son nom “monoclonal”.
Contrairement aux anticorps polyclonaux (qui ciblent plusieurs épitopes du même antigène), les AcM offrent une spécificité absolue, ce qui en fait des outils thérapeutiques d’une grande précision.
Conditions pour qu’un AcM soit efficace en oncologie
Pour qu’un traitement par anticorps monoclonal fonctionne, l’antigène ciblé doit répondre à plusieurs critères :
- Être exprimé sur les cellules tumorales mais absent (ou peu présent) sur les cellules saines critiques
- Être surexprimé de façon significative dans la tumeur
- Être stable (non muté, non variant)
- Être indispensable à la survie ou à la croissance de la cellule tumorale
Histoire : De la Découverte au Prix Nobel
1975 : la naissance des hybridomes
Tout commence en 1975, quand deux scientifiques changent l’histoire de la médecine. Georges Köhler (immunologiste allemand) et César Milstein (biochimiste britannico-argentin) mettent au point la technologie des hybridomes.
Leur idée géniale : fusionner un lymphocyte B (capable de produire des anticorps spécifiques mais à durée de vie limitée) avec une cellule de myélome (cancéreuse, donc immortelle mais incapable de produire des anticorps). La cellule hybride résultante — l’hybridome — produit indéfiniment un anticorps monoclonal spécifique.
Cette découverte leur vaut le Prix Nobel de Médecine et Physiologie en 1984.
1997 : le premier anticorps approuvé en oncologie
En 1997, la FDA (États-Unis) approuve le premier anticorps monoclonal thérapeutique en oncologie : le rituximab (Rituxan), un anticorps chimérique anti-CD20, pour le traitement des lymphomes non hodgkiniens.
Depuis lors, le nombre de mAbs approuvés n’a cessé de croître, englobant de nombreux cancers (sein, côlon, poumon, rein, ORL, hémopathies).
Comment Fabrique-t-on un Anticorps Monoclonal ?
Étape 1 : L’immunisation de l’animal
L’antigène cible purifié est injecté à un animal (généralement une souris). Le système immunitaire de l’animal produit des lymphocytes B capables de reconnaître cet antigène. Ces cellules sont ensuite extraites de la rate.
Étape 2 : La fusion et la sélection (milieu HAT)
Les lymphocytes B sont fusionnés avec des cellules de myélome grâce au polyéthylène glycol. La sélection des hybridomes est réalisée dans un milieu de culture spécial (HAT : Hypoxanthine-Aminoptérine-Thymidine) :
- L’aminoptérine bloque la synthèse normale de nucléotides, forçant les cellules à utiliser la voie de sauvetage
- Seuls les hybridomes (cellules fusionnées) survivent, car ils combinent la voie de sauvetage du lymphocyte B et l’immortalité de la cellule myélomateuse
Étape 3 : Clonage et production
Les hybridomes producteurs de l’anticorps désiré sont identifiés (test ELISA), isolés, puis multipliés soit en culture cellulaire (in vitro), soit en cavité péritonéale de la souris (in vivo). Les anticorps sont ensuite purifiés et concentrés.
Un hybridome peut être conservé indéfiniment dans l’azote liquide, garantissant une production illimitée de l’anticorps spécifique.
Les 4 Générations d’Anticorps Monoclonaux Thérapeutiques
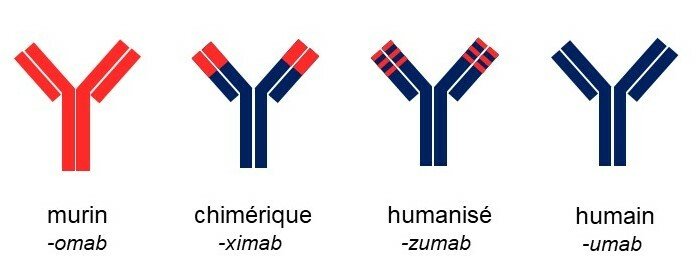
1. Les anticorps murins — suffixe -omab
Entièrement produits chez la souris. Leur grand défaut : ils provoquent la production d’anticorps humains anti-souris (HAMA) chez le patient, entraînant des réactions immunitaires et réduisant leur efficacité. Leur utilisation est aujourd’hui très limitée.
Exemple : Ibritumomab (utilisé en radio-immunothérapie)
2. Les anticorps chimériques — suffixe -ximab
Humains à 60 %. Les régions variables (VH et VL) de l’anticorps murin sont greffées sur des régions constantes humaines. Meilleure tolérance, mais risque d’immunogénicité résiduel.
Exemple : Rituximab, Cetuximab
3. Les anticorps humanisés — suffixe -zumab
Humains à 90 %. Seules les régions hypervariables (CDR) murines sont greffées sur un squelette d’immunoglobuline humain. Excellente tolérance et demi-vie prolongée dans l’organisme.
Exemple : Trastuzumab (Herceptin), Bevacizumab (Avastin)
4. Les anticorps humains — suffixe -umab
Humains à 100 %. Obtenus grâce aux souris transgéniques ou au phage display. Risque d’immunogénicité quasi nul et très bonne tolérance.
Exemple : Panitumumab, Ipilimumab
Les Mécanismes d’Action en Oncologie
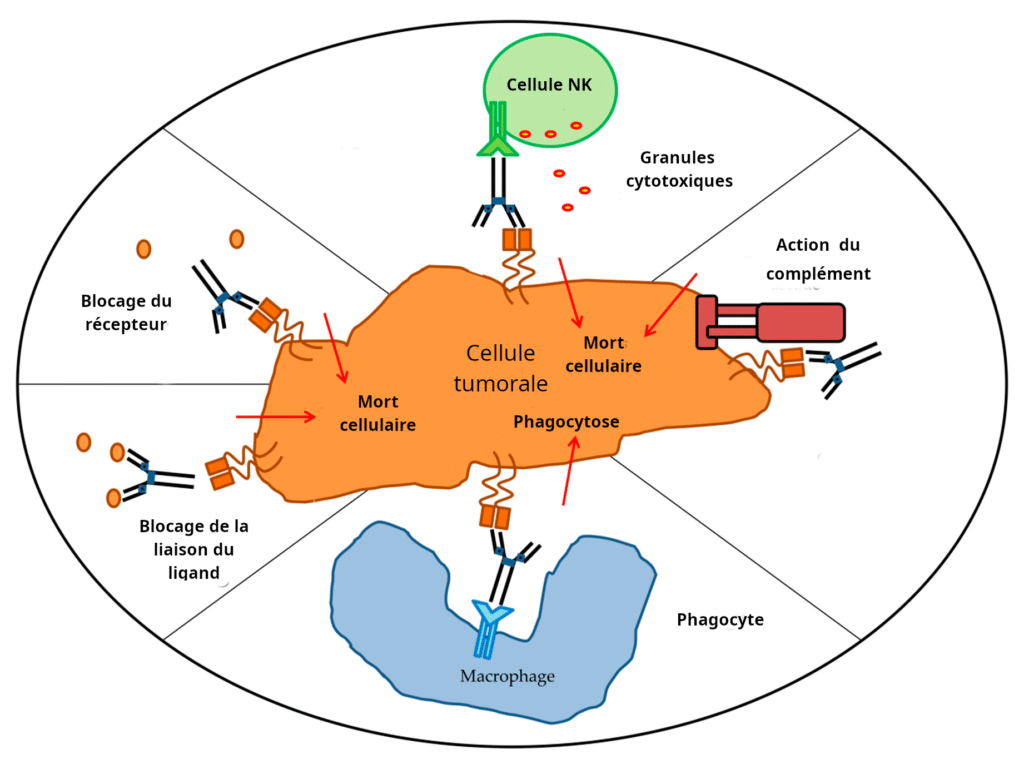
Les anticorps monoclonaux peuvent agir selon quatre grands mécanismes :
1. Destruction directe de la cellule cible
L’anticorps se lie à son récepteur cible sur la cellule tumorale et déclenche une réaction immunitaire conduisant à la mort de cette cellule. C’est le cas via :
- La cytotoxicité à médiation cellulaire dépendante des anticorps (ADCC) : des cellules NK (natural killer) détruisent la cellule marquée
- La lyse par le complément : activation de la cascade du complément aboutissant à la lyse cellulaire
- L’induction de l’apoptose : mort programmée de la cellule tumorale
2. Blocage des récepteurs membranaires
L’anticorps se fixe au récepteur et bloque la liaison avec son ligand naturel (facteur de croissance). La cascade de signaux favorisant la prolifération cellulaire est ainsi interrompue.
Exemple concret : Le cétuximab (anti-EGFR) bloque le récepteur au facteur de croissance épidermique dans le cancer colorectal, stoppant la division non contrôlée des cellules.
3. Neutralisation de molécules circulantes
La cible n’est plus le récepteur membranaire, mais une molécule circulante (comme un facteur de croissance). En se liant à elle, l’anticorps l’empêche de rejoindre son récepteur.
Exemple concret : Le bévacizumab (anti-VEGF) capture le facteur de croissance vasculaire (VEGF), privant ainsi la tumeur de nouveaux vaisseaux sanguins (anti-angiogenèse).
4. Rôle de vecteur : les anticorps conjugués (ADC)
Une stratégie innovante consiste à coupler chimiquement un anticorps monoclonal à une molécule cytotoxique (chimiothérapie ou toxine). L’anticorps sert de “missile guidé” qui délivre l’agent toxique directement aux cellules tumorales, sans toucher les cellules saines.
Avantage majeur : Efficacité accrue de la chimiothérapie + effets secondaires considérablement réduits.
Les Principaux Anticorps Monoclonaux Utilisés en Oncologie
Le Rituximab — Anti-CD20 (lymphomes)
Premier mAb approuvé en oncologie (1997), le rituximab cible la protéine CD20 présente à la surface des lymphocytes B. Il agit via trois mécanismes combinés : induction de l’apoptose, lyse par le complément et ADCC.
Indications principales :
- Lymphomes non hodgkiniens (folliculaires, agressifs)
- Leucémie lymphoïde chronique (LLC) : taux de réponse globale de 51 à 90 % en monothérapie de première ligne
- Polyarthrite rhumatoïde (hors oncologie)
Le Cetuximab — Anti-EGFR (côlon, ORL)
Le cetuximab cible la partie extracellulaire du récepteur EGFR (Epidermal Growth Factor Receptor), bloquant la liaison de son ligand par encombrement stérique.
Indications :
- Cancer colorectal métastatique (CCRm)
- Carcinomes épidermoïdes de la tête et du cou
Le Bevacizumab — Anti-VEGF (anti-angiogenèse)
Le bevacizumab (IgG1) neutralise le VEGF (Vascular Endothelial Growth Factor), empêchant la création de nouveaux vaisseaux sanguins qui alimentent la tumeur.
Indications :
- Cancer colorectal, du poumon, du rein, du col de l’utérus
- Glioblastome
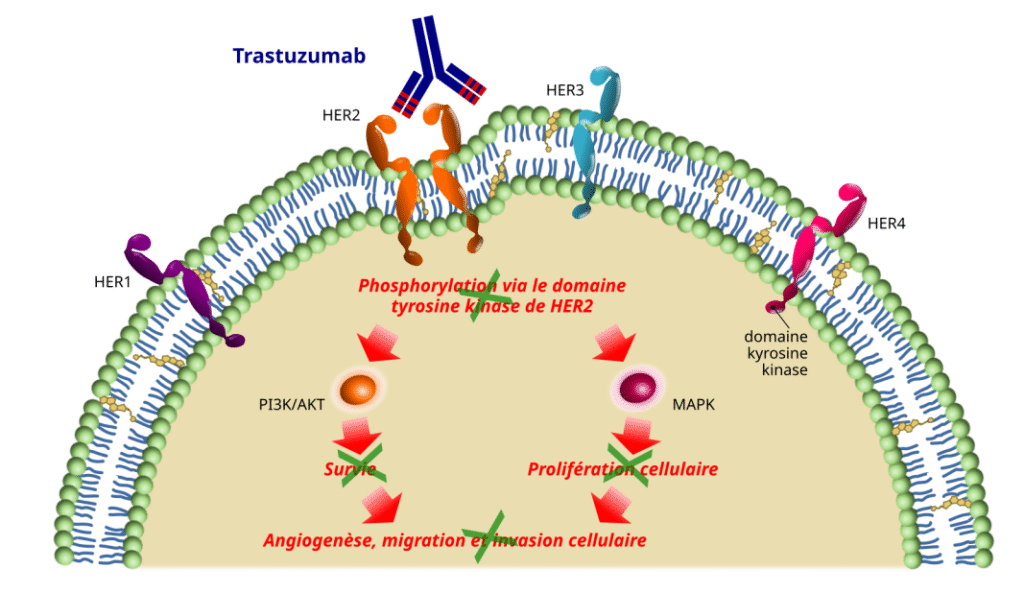
Le Trastuzumab — Anti-HER2 (cancer du sein)
Le trastuzumab (Herceptin) est un anticorps humanisé ciblant le domaine extracellulaire de HER2 (Human Epidermal growth factor Receptor 2). Environ 20 % des cancers du sein présentent une surexpression de HER2, associée à un pronostic plus défavorable.
Le trastuzumab agit en combinant plusieurs mécanismes : ADCC, blocage de la signalisation et inhibition de l’excrétion de HER2. Il représente une avancée majeure dans le traitement du cancer du sein HER2-positif, améliorant significativement la survie globale.
Les Anticorps Conjugués : la Précision Ultime
Les ADC (Antibody-Drug Conjugates) représentent la prochaine génération de thérapies ciblées. Ils associent chimiquement un anticorps monoclonal à un agent cytotoxique puissant via un “linker” (bras de liaison) clivable.
Le Brentuximab védotine
Le brentuximab cible le marqueur CD30 (présent sur les cellules de Hodgkin et les lymphomes T). Il est couplé à la monométhylauristatine E (MMAE), un agent anti-microtubulaire très puissant. Une fois lié aux cellules CD30+, le linker est clivé et libère la MMAE directement dans la cellule tumorale, la détruisant de l’intérieur.
Les Anticorps Bispécifiques : Rapprocher Immune et Tumeur
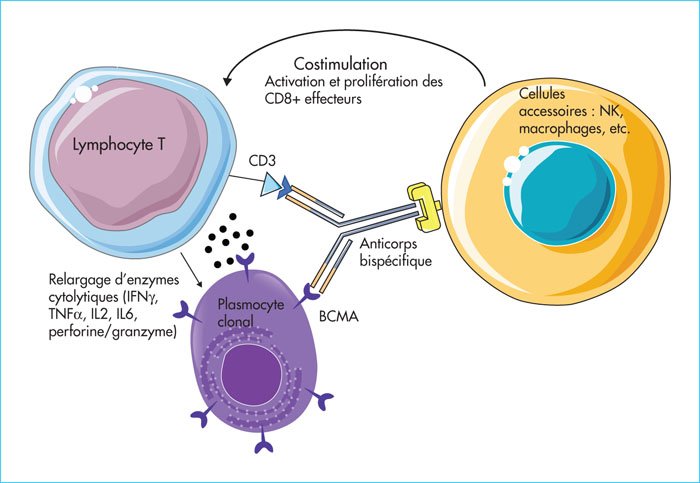
Les anticorps bispécifiques sont capables de reconnaître simultanément deux épitopes différents grâce à deux paratopes distincts. Leur rôle : rapprocher physiquement une cellule tumorale d’une cellule immunitaire (lymphocyte T ou cellule NK) pour activer la destruction.
Le Blinatumomab
Le blinatumomab est un anticorps bispécifique qui se lie simultanément :
- Au CD19 sur les cellules B malignes (leucémies lymphoblastiques aiguës B)
- Au CD3 sur les lymphocytes T cytotoxiques
En rapprochant ces deux cellules, il active les lymphocytes T endogènes du patient pour qu’ils détruisent les cellules leucémiques. Un concept simple mais d’une efficacité remarquable.
Chimiothérapie vs Biothérapie : Quelle Différence ?
| Critère | Chimiothérapie | Biothérapie (AcM) |
|---|---|---|
| Mode d’action | Agit sur toutes les cellules en division | Cible un antigène spécifique |
| Sélectivité | Faible (cellules saines touchées) | Élevée (cellules tumorales visées) |
| Effets secondaires | Souvent importants (nausées, chute des cheveux…) | Généralement mieux tolérée |
| Administration | Orale ou IV | Principalement IV |
| Résistance | Fréquente | Possible (mutation de la cible) |
La chimiothérapie détruit les cellules cancéreuses en agissant sur les mécanismes de division cellulaire, mais elle affecte aussi les cellules saines à fort renouvellement.
La biothérapie cible au contraire spécifiquement une molécule présente à la surface de la cellule tumorale, limitant les dommages collatéraux.
Les Anticorps Monoclonaux : Un Marché en Pleine Explosion
Les chiffres parlent d’eux-mêmes :
- 263 milliards USD : valeur du marché mondial des AcM en 2024
- 720 milliards USD : valeur projetée d’ici 2032 (TCAC de +13,4 %)
- 62 % des ventes mondiales de mAbs concernent le traitement du cancer
- 80 % des plans de traitement avancés en oncologie incluent désormais un anticorps monoclonal
- 15 nouveaux mAbs approuvés par l’EMA (Europe) en 2024 seulement
- 100 000 $/an : coût moyen d’un traitement par AcM aux États-Unis — un enjeu majeur d’accès aux soins
Ces chiffres reflètent à la fois l’efficacité prouvée de ces thérapies et les immenses efforts de recherche déployés par l’industrie pharmaceutique mondiale.
Perspectives et Innovations : Que Prépare la Recherche ?
La recherche sur les anticorps monoclonaux évolue à grande vitesse. Parmi les axes les plus prometteurs :
- Les ADC de nouvelle génération (Antibody-Drug Conjugates), avec des linkers plus stables et des agents cytotoxiques encore plus puissants
- Les anticorps bispécifiques et trifonctionnels, capables d’engager plusieurs types cellulaires immunitaires simultanément
- Les biosimilaires, qui permettent de réduire les coûts et d’élargir l’accès aux traitements : plus de 60 biosimilaires approuvés par la FDA en 2024
- L’intelligence artificielle pour accélérer la conception et la sélection de nouveaux anticorps thérapeutiques
- Les essais de phase III pour de nouvelles molécules comme le RGX-202 (Roche, 2025) ciblant le cancer gastrique HER2-positif
Conclusion : Les Anticorps Monoclonaux, Piliers de l’Oncologie Moderne
Les anticorps monoclonaux thérapeutiques ont profondément transformé la prise en charge du cancer en moins de 30 ans. Depuis le rituximab en 1997, plus d’une dizaine de ces molécules sont devenues des traitements de référence, améliorant la survie et la qualité de vie de millions de patients à travers le monde.
Leur précision, leur efficacité et leur polyvalence (tumeurs solides, hémopathies malignes, cancers métastatiques) en font des acteurs incontournables de l’arsenal thérapeutique oncologique moderne.
Alors que la recherche continue de repousser les frontières — avec les anticorps bispécifiques, les ADC et l’IA — une chose est certaine : la révolution des biothérapies n’en est qu’à ses débuts.
Points clés à retenir
- Les AcM sont des protéines produites en laboratoire qui ciblent avec précision les cellules cancéreuses
- Ils agissent selon 4 mécanismes principaux : destruction cellulaire, blocage des récepteurs, neutralisation de molécules circulantes, et vecteur de médicament
- On distingue 4 types selon leur degré d’humanisation : murins, chimériques, humanisés et humains
- Les AcM les plus utilisés en oncologie incluent le rituximab, le trastuzumab, le bevacizumab et le cetuximab
- Le marché mondial des AcM devrait dépasser 700 milliards de dollars d’ici 2032
- La recherche s’oriente vers les ADC, les anticorps bispécifiques et l’IA pour concevoir les traitements de demain
Mots-clés : anticorps monoclonaux, oncologie, biothérapie, cancer, immunothérapie, trastuzumab, rituximab, bevacizumab, thérapies ciblées, AcM thérapeutiques, hybridomes