La Spectrométrie de Masse : Principe, Fonctionnement et Applications en Pharmacie
Introduction : Pourquoi la spectrométrie de masse révolutionne l’analyse chimique ?
Imaginez une balance capable de peser une seule molécule avec une précision de l’ordre du milliardième de gramme. C’est exactement ce que fait la spectrométrie de masse (SM), une technique analytique incontournable dans les laboratoires de chimie, de pharmacologie et de biologie.
Depuis ses premières applications au début du XXᵉ siècle, cette méthode n’a cessé d’évoluer. Aujourd’hui, le marché mondial de la spectrométrie de masse est évalué à plus de 6,7 milliards USD en 2024, avec une croissance annuelle soutenue de plus de 7 %. Dans cet article, nous vous expliquons tout : son principe de fonctionnement, ses composants, ses types d’analyseurs, et ses applications concrètes, notamment dans l’industrie pharmaceutique.

I. Qu’est-ce que la spectrométrie de masse ?
Définition et principe fondamental
La spectrométrie de masse est une méthode analytique qui permet de caractériser les molécules en déterminant leur masse atomique ou moléculaire. L’unité utilisée est le dalton (Da), aussi appelé unité de masse atomique (uma) :
1 Da = 1,66054 × 10⁻²⁷ kg
Pour être analysée, une molécule doit d’abord être transformée en ion chargé. Le spectromètre “pèse” ensuite ces ions en les séparant selon leur rapport masse/charge (m/z), grâce à des champs électriques et magnétiques.
Les 5 étapes clés du processus
- Vaporisation : les molécules passent de l’état condensé à l’état gazeux pour être isolées les unes des autres.
- Ionisation : les molécules sont transformées en ions dans la source de l’appareil. Cette étape génère un mélange statistique d’ions de fragmentation.
- Accélération : les ions formés sont extraits, focalisés et accélérés par des lentilles électroniques pour augmenter leur énergie cinétique.
- Séparation : les ions sont “filtrés” par l’analyseur selon leur rapport m/z.
- Détection : les ions séparés frappent un capteur qui génère un signal électrique proportionnel à leur nombre.
💡 Résumé : Ionisation → Séparation par m/z → Analyse qualitative et quantitative.
II. Les composants d’un spectromètre de masse
Un spectromètre de masse est composé de quatre blocs fonctionnels essentiels :
- La chambre d’introduction : permet d’introduire l’échantillon
- La source d’ionisation : transforme les molécules en ions
- L’analyseur (séparateur) : sépare les ions selon leur rapport m/z
- Le détecteur / enregistreur : mesure et enregistre les signaux
Tous ces modules fonctionnent sous un vide poussé (entre 10⁻⁴ et 10⁻⁷ Torr), condition indispensable pour éviter les collisions entre les ions et les molécules de gaz.
III. Les sources d’ionisation : comment ionise-t-on une molécule ?
L’ionisation est l’étape critique de la spectrométrie de masse. Il existe deux grandes familles : l’ionisation dure et l’ionisation douce.
Ionisation dure : l’Impact Électronique (IE)
C’est la méthode la plus ancienne et la plus répandue. Un faisceau d’électrons bombarde les molécules, arrachant un électron pour former un ion radical cation M⁺•.
- ✅ Avantage : fragmentation intense, spectres très riches en informations (véritable “empreinte digitale” de la molécule)
- ❌ Inconvénient : le pic moléculaire est souvent très faible ou absent
Exemple : Pour le butane (CH₃-CH₂-CH₂-CH₃, M = 58 Da), l’IE génère de nombreux fragments caractéristiques, dont la perte d’un groupement méthyle (M-15).
Ionisation Chimique (CI)
Dans cette méthode, un gaz réactif (méthane, ammoniac ou isobutane) est d’abord ionisé par bombardement électronique. Les ions ainsi formés transfèrent ensuite leur charge à la molécule à analyser.
Le résultat est la formation d’un ion [M+H]⁺, appelé pseudo-ion moléculaire. Ce mode est plus doux que l’IE et préserve mieux le pic moléculaire.
Exemple : Pour la benzophénone (M = 182,2 g/mol), le pic [M+H]⁺ apparaît à m/z = 183,2.
Ionisation MALDI (Matrix-Assisted Laser Desorption Ionization)
La technique MALDI est idéale pour l’analyse de grosses biomolécules (protéines, polysaccharides, ADN) dont la masse moléculaire peut dépasser 200 kDa.
Le protocole se déroule en trois étapes :
- L’analyte est mélangé à une matrice organique solide (ex. : acide dihydroxybenzoïque) sur une plaque métallique.
- Un laser pulsé vaporise et ionise les molécules de matrice.
- Les molécules de matrice ionisées transfèrent un proton à l’analyte : XH⁺ + M → MH⁺ + X.
Cette technique est très peu fragmentante, ce qui la rend parfaite pour déterminer la masse intacte de biomacromolécules.
Ionisation par Électronébullisation (ESI)
L’ESI est aujourd’hui l’une des sources d’ionisation les plus utilisées en biologie et en pharmacie. Elle permet d’analyser des molécules en solution directement, ce qui facilite le couplage avec la chromatographie liquide (HPLC-MS).
L’ESI détenait la plus grande part de marché des modes d’ionisation, à 42,5 % en 2023, grâce à sa sensibilité élevée, sa polyvalence et sa compatibilité avec une large gamme d’analytes.
Ionisation par Plasma d’Argon (ICP)
Utilisée principalement en couplage ICP/MS, cette technique est réservée à l’identification et au dosage des métaux et métalloïdes (plomb, mercure, arsenic…) dans des matrices liquides. Elle est très utilisée en toxicologie et en contrôle environnemental.

IV. Les analyseurs de masse : séparer les ions avec précision
L’analyseur est le “cœur” du spectromètre. Il sépare les ions selon leur rapport m/z. Ses performances sont caractérisées par plusieurs paramètres :
- La gamme de masse : plage de m/z analysable (exprimée en uma)
- La résolution : R = M/ΔM — capacité à distinguer deux ions de masse voisine
- La sensibilité : quantité minimale d’analyte détectable
- La vitesse de balayage : nombre de balayages par seconde
- La précision de masse : exprimée en % ou en ppm
L’analyseur Quadripolaire (Q)
Composé de quatre barres métalliques parallèles, le quadripôle filtre les ions grâce à des potentiels électriques alternatifs.
- Gamme de masse : 30 à 2 000 uma
- Résolution : basse à moyenne
- Avantage : robuste, rapide, peu coûteux → idéal pour les analyses de routine
L’analyseur à Temps de Vol (TOF)
Le principe est simple : tous les ions reçoivent la même énergie cinétique à leur sortie de la source. Les ions légers vont plus vite que les ions lourds, et donc atteignent le détecteur en premier.
- Compatible avec MALDI pour l’analyse de très grosses molécules
- Haute résolution et grande gamme de masse
- Excellente précision de masse
L’analyseur à Secteur Magnétique
Les ions sont déviés par un champ magnétique. Seuls ceux dont le rayon de courbure correspond à la géométrie de l’analyseur atteignent le détecteur.
- Gamme de masse : jusqu’à 3 500 uma
- Pouvoir de résolution : de 10 000 à 150 000 → haute résolution
- Utilisé pour la détermination exacte de formules moléculaires
Autres analyseurs
- Trappe à ions (Ion Trap) : piège et stocke les ions pour des analyses MS/MS
- FT-ICR (Fourier Transform Ion Cyclotron Resonance) : résolution ultra-haute, utilisé en recherche fondamentale
V. Les détecteurs : transformer les ions en signal mesurable
Après séparation, les ions frappent un détecteur qui convertit leur énergie en signal électrique. Les principaux détecteurs sont :
- Faraday Cup : simple et robuste, pour les ions abondants
- Channeltron : très sensible, capable de détecter un ion unique
- Daly Detector : haute sensibilité, utilisé en secteur magnétique
- Electron Multiplier Tube (EMT) : amplification du signal par cascade d’électrons
- Microchannel Plate (MCP) : détecteur bidimensionnel pour les analyses TOF
VI. La spectrométrie de masse en tandem (MS/MS)
La MS/MS combine deux analyseurs séparés par une chambre de collision. Cette configuration permet une analyse à deux niveaux :
- Le premier analyseur sélectionne un ion précurseur d’intérêt.
- L’ion est fragmenté dans la chambre de collision.
- Le second analyseur analyse les fragments produits.
La configuration la plus courante est le triple quadripôle (QqQ), où le quadripôle central (q) joue le rôle de chambre de collision.
Cette approche est extrêmement puissante pour l’analyse de molécules dans des matrices complexes (plasma sanguin, urine, extraits végétaux), avec une sensibilité et une sélectivité inégalées.
💡 Exemple concret : En pharmacocinétique, le QqQ est utilisé pour doser un médicament et ses métabolites simultanément dans le plasma d’un patient, à des concentrations de l’ordre du ng/mL.
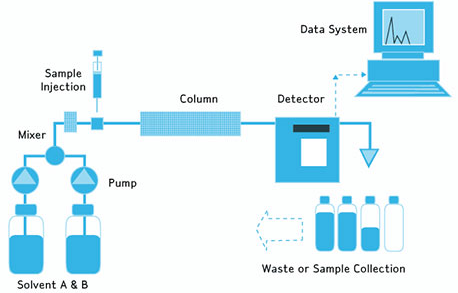
VII. Le couplage Chromatographie / Spectrométrie de masse
L’une des forces majeures de la spectrométrie de masse est sa compatibilité avec les techniques chromatographiques. Ce couplage permet de séparer les constituants d’un mélange complexe avant de les analyser.
Couplage GC/MS (Chromatographie en Phase Gazeuse)
- Adapté aux molécules volatiles et thermostables
- Utilise principalement l’ionisation par impact électronique (IE)
- Applications : drogues, résidus de pesticides, arômes alimentaires, polluants atmosphériques
Couplage HPLC/MS et HPLC/MS/MS
- Adapté aux molécules polaires, ioniques ou thermolabiles
- Utilise l’ionisation ESI ou APCI
- Applications : médicaments et leurs métabolites, protéines, acides nucléiques, résidus de médicaments vétérinaires
VIII. Applications de la spectrométrie de masse
A. Identification des molécules
Dans des conditions opératoires identiques, le spectre de masse d’une molécule inconnue est comparé à des bases de données de référence contenant des milliers de spectres connus.
Si Spectre (molécule X) = Spectre (molécule Y) → Molécule X = Molécule Y
La base de données Wiley de spectres de masse des drogues de synthèse contient plus de 36 360 spectres de 27 500 composés chimiques uniques, dont les nouvelles substances psychoactives, constituant une ressource essentielle pour les laboratoires de toxicologie et de médecine légale.
B. Détermination de la masse moléculaire
Le pic moléculaire (M⁺) correspond au cation formé par perte d’un seul électron. Sa position en m/z donne directement la masse molaire de la molécule.
Exemple : Dans le spectre du méthanol (CH₃OH, M = 32 g/mol), le pic moléculaire apparaît à m/z = 32, et le pic de base (le plus intense) est à m/z = 31, correspondant à la perte d’un atome d’hydrogène.
C. Détermination de la structure moléculaire
L’interprétation des fragments permet de reconstituer la structure d’une molécule inconnue. Chaque pic correspond à un fragment produit par la rupture d’une liaison spécifique.
Quelques règles générales :
- La fragmentation se produit préférentiellement au niveau des liaisons les plus faibles.
- La présence d’hétéroatomes (O, N, S) dirige l’ionisation vers les doublets libres.
- Les réarrangements (ex. : réarrangement de McLafferty) donnent des fragments caractéristiques.
D. Analyse quantitative
La SM permet de doser précisément des analytes à des concentrations très faibles grâce à deux méthodes d’étalonnage :
- Étalonnage externe : courbe de calibration avec des standards de concentration connue.
- Étalonnage interne : utilisation d’un standard interne (souvent un analogue deutéré) pour corriger les variations analytiques. C’est la méthode de référence en pharmacologie et en toxicologie clinique.
E. Applications dans l’industrie pharmaceutique
Dans l’industrie pharmaceutique, la spectrométrie de masse est utilisée pour vérifier la pureté des médicaments en détectant et quantifiant les impuretés et les sous-produits de synthèse. Elle permet également de caractériser les principes actifs (API), d’étudier leur métabolisme et de valider leur stabilité.
Les sociétés pharmaceutiques représentaient environ 50 % de la part de marché des applications en spectrométrie de masse en 2023, ce qui confirme le rôle central de cette technique dans le développement du médicament.
Parmi les applications concrètes :
- Contrôle qualité des médicaments : détection d’impuretés en dessous du seuil réglementaire (ICH Q3A/Q3B)
- Études pharmacocinétiques : suivi des concentrations plasmatiques et des métabolites
- Protéomique et biothérapeutiques : caractérisation des anticorps monoclonaux et des protéines recombinantes
- Néonatalogie : dépistage néonatal de maladies métaboliques héréditaires par LC-MS/MS
F. Applications environnementales et alimentaires
La spectrométrie de masse est appliquée à l’analyse d’échantillons environnementaux comme l’eau, l’air et le sol, pour la détection de polluants tels que les pesticides, les herbicides et les composés organiques volatils (COV).
Dans l’industrie alimentaire, elle est utilisée pour :
- Détecter les résidus de pesticides dans les fruits et légumes
- Identifier les adulterants et les fraudes alimentaires
- Contrôler la qualité des huiles, des arômes et des additifs
IX. Les tendances actuelles et l’avenir de la spectrométrie de masse
La spectrométrie de masse est en pleine transformation. Plusieurs tendances majeures se dégagent pour les prochaines années :
L’intégration de l’Intelligence Artificielle
L’application de l’IA à l’interprétation des données spectroscopiques évolue rapidement, permettant d’extraire des informations précieuses à partir d’ensembles de données complexes. Les algorithmes de machine learning optimisent les conditions expérimentales et accélèrent l’identification des molécules.
La miniaturisation des instruments
Des spectromètres de masse portables sont désormais disponibles pour des analyses sur le terrain : contrôle de sécurité aux frontières, surveillance environnementale en temps réel, diagnostic au point de soin.
Les systèmes hybrides haute performance
Le marché de la spectrométrie de masse hybride détenait plus de 60 % des revenus en 2022, offrant une sensibilité, une sélectivité et des capacités de quantification accrues par rapport aux autres technologies.
Conclusion : La spectrométrie de masse, un outil analytique universel
La spectrométrie de masse est bien plus qu’une simple technique de pesée moléculaire. C’est un outil polyvalent, précis et sensible qui couvre un spectre d’applications extrêmement large : de la caractérisation structurale de nouveaux médicaments au dépistage de contaminants environnementaux, en passant par le diagnostic clinique et la recherche en protéomique.
Le marché mondial de la spectrométrie de masse devrait croître à un TCAC de 7,42 % jusqu’en 2033, porté par les avancées technologiques et la demande croissante dans les secteurs pharmaceutique, alimentaire et environnemental.