Physiopathologie de la Douleur : Comprendre les Mécanismes pour Mieux Traiter
Introduction : La Douleur, un Signal d’Alarme Universel
La douleur est l’expérience la plus commune et la plus redoutée de l’être humain. Selon l’IASP (Association Internationale pour l’Étude de la Douleur), elle se définit comme “une expérience sensorielle et émotionnelle désagréable, associée à une lésion tissulaire réelle ou potentielle”.
Loin d’être un simple inconfort, la douleur constitue le premier motif de consultation aussi bien aux urgences que chez le médecin généraliste. En France, les données les plus récentes (Observatoire Français de la Douleur et des Antalgiques, 2025) révèlent que plus de 40 % de la population adulte souffre de douleur chronique, soit environ 23 millions de personnes. Pourtant, moins de 3 % d’entre elles bénéficient d’une prise en charge spécialisée.
Comprendre comment naît, se transmet et se module la douleur est indispensable pour mieux la traiter. Cet article vous propose un tour complet des mécanismes physiopathologiques de la douleur, des nocicepteurs jusqu’au cerveau.

1. Pourquoi la Douleur Existe-t-elle ? Son Rôle Physiologique
La douleur est avant tout un mécanisme de protection non spécifique. Elle signale à l’organisme qu’un tissu est en danger et déclenche des comportements de défense (retrait du membre, mise au repos, consultation médicale).
Un exemple simple : poser la main sur une plaque brûlante provoque une douleur immédiate qui force le retrait du bras avant même que le cerveau ait eu le temps de “décider” consciemment. Ce réflexe protecteur est rendu possible par la vitesse de conduction des fibres nerveuses de la douleur.
Cependant, lorsque la douleur persiste au-delà de 3 mois, elle perd sa fonction d’alarme et devient elle-même une maladie : la douleur chronique. Elle entraîne alors :
- Des troubles du sommeil, de l’anxiété et de la dépression (chez 70 % des patients douloureux chroniques)
- Une perte de productivité (arrêts de travail 5 fois plus fréquents que dans la population générale)
- Un coût économique estimé à plus de 30 000 € par patient et par an

2. Les Trois Étapes de la Transmission Douloureuse
La nociception — c’est-à-dire la détection et la transmission des stimuli douloureux — se déroule en trois grandes étapes impliquant des mécanismes électrophysiologiques et neurochimiques précis.
Étape 1 — La Détection Périphérique : le Rôle des Nocicepteurs
Les nocicepteurs sont des récepteurs sensoriels spécialisés, présents dans la peau, les muscles, les articulations et les viscères. Ils constituent la “porte d’entrée” du signal douloureux.
Il en existe deux grandes catégories :
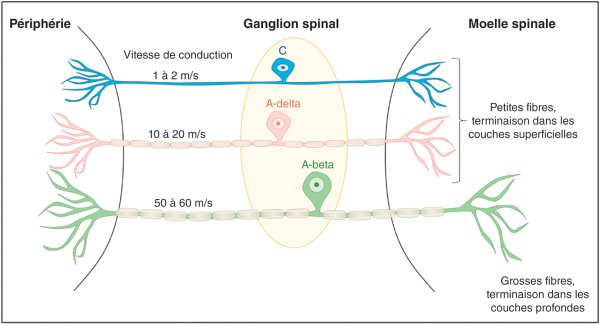
Les fibres Aδ (A-delta)
- Myélinisées, donc rapides (vitesse de conduction : 5 à 30 m/s)
- Transmettent une douleur vive, aiguë et bien localisée (exemple : la piqûre d’une aiguille)
- Répondent principalement aux stimuli mécaniques et thermiques intenses
Les fibres C
- Non myélinisées, donc lentes (vitesse : 0,5 à 2 m/s)
- Transmettent une douleur diffuse, sourde et mal localisée (exemple : la brûlure qui “couve” après un coup de soleil)
- Répondent aux stimuli mécaniques, thermiques ET chimiques (polymodales)
💡 À retenir : C’est pourquoi après une blessure, on ressent d’abord une douleur aiguë et précise (fibres Aδ), suivie d’une douleur plus profonde et persistante (fibres C).
Étape 2 — Le Relais Médullaire : la Corne Dorsale de la Moelle Épinière
Une fois le signal capté par les nocicepteurs, il remonte via le 1er neurone (protoneurone) jusqu’à la corne dorsale de la moelle épinière. C’est ici que s’effectue un relais crucial, où l’information est à la fois transmise et modulée.
Deux types de neurones assurent ce relais :
- Neurones nociceptifs spécifiques : reçoivent exclusivement les signaux des fibres Aδ et C — ils ne traitent que la douleur
- Neurones nociceptifs non spécifiques (ou convergents) : reçoivent des signaux de toutes les fibres sensorielles — ils expliquent notamment les douleurs référées (une crise cardiaque ressentie dans le bras gauche, par exemple)
Le Rôle Clé des Récepteurs Glutamatergiques
Au niveau de la synapse entre le 1er et le 2ème neurone, deux types de récepteurs au glutamate jouent un rôle déterminant :
- Récepteur AMPA : assure une transmission excitatrice rapide et de courte durée (la douleur aiguë ordinaire)
- Récepteur NMDA : responsable de modifications neuronales à long terme, notamment une hyperexcitabilité auto-entretenue — c’est le mécanisme clé de la sensibilisation centrale dans la douleur chronique
Ce phénomène de sensibilisation centrale explique pourquoi un patient souffrant de fibromyalgie ressent une douleur intense même à un simple effleurement.
Étape 3 — L’Intégration Cérébrale : de l’Influx à la Sensation
Le 2ème neurone (spino-thalamique) monte vers le thalamus via deux voies ascendantes principales :
Le faisceau néo-spinothalamique
- Rejoint le thalamus latéral puis le cortex sensitif somatique
- Assure la discrimination de la douleur : localisation précise, intensité, qualité (brûlure, piqûre…)
Le faisceau paléo-spinothalamique
- Rejoint le thalamus médian, puis les structures limbiques, l’hypothalamus et le cortex frontal
- Gère la composante affective et émotionnelle de la douleur : la souffrance, l’angoisse, la mémorisation
💡 C’est pourquoi la douleur est une expérience à la fois sensorielle ET émotionnelle. L’imagerie cérébrale (IRM fonctionnelle) confirme que les mêmes zones cérébrales traitent la douleur physique et la souffrance psychologique.
Le 3ème neurone (thalamo-cortical) finalise l’intégration en transformant l’influx nerveux en sensation douloureuse consciente, colorée par le vécu, la culture et le contexte psychologique de l’individu.

3. La Modulation de la Douleur : le Système Peut Amplifier ou Atténuer
La transmission de la douleur n’est pas un processus passif. L’organisme dispose de puissants mécanismes de modulation, capables d’amplifier ou de réduire la perception douloureuse.
3.1 L’Amplification : Quand la Douleur s’Emballe
Un excès de stimulation nociceptive peut provoquer une sensibilisation du système, se manifestant par :
L’hyperalgésie primaire
- Localisée au niveau de la lésion elle-même
- Le seuil de douleur est abaissé : un stimulus normalement peu douloureux devient intense
- Médiée par l’inflammation locale (libération de prostaglandines, bradykinine, substance P)
L’hyperalgésie secondaire
- S’étend autour et à distance de la lésion
- Résulte de la sensibilisation centrale via les récepteurs NMDA
- Exemple clinique : après une brûlure, la peau saine autour de la brûlure devient également hypersensible
Ce phénomène explique l’allodynie : une douleur déclenchée par un stimulus normalement non douloureux, comme le simple contact d’un vêtement chez un patient atteint de zona ou de neuropathie diabétique.
3.2 Le Contrôle Porte (Gate Control Theory)
Proposée par Melzack et Wall en 1965, la théorie du contrôle de la porte reste une référence fondamentale. Elle postule qu’une “porte” synaptique au niveau médullaire peut être ouverte ou fermée selon les signaux reçus :
- Les fibres A-bêta (grosses fibres sensitives non nociceptives) ferment la porte et inhibent le signal douloureux — c’est pourquoi frotter une zone blessée soulage temporairement
- Les fibres Aδ et C ouvrent la porte et facilitent la transmission
Cette théorie est à la base des techniques de neuromodulation comme la stimulation médullaire ou la TENS (Transcutaneous Electrical Nerve Stimulation).
3.3 Les Contrôles Descendants Inhibiteurs
Le cerveau exerce également un contrôle descendant sur la transmission de la douleur, via des voies inhibitrices issues du tronc cérébral. Ces voies libèrent des neurotransmetteurs comme :
- Les endorphines et enképhalines (opioïdes endogènes)
- La sérotonine et la noradrénaline
Ces systèmes expliquent pourquoi la douleur perçue varie selon l’état émotionnel : un soldat blessé au combat peut ne ressentir aucune douleur sur le moment (analgésie de stress), tandis qu’un patient anxieux percevra une douleur amplifiée.
💡 C’est aussi sur ces voies que agissent les antidépresseurs (inhibiteurs de recapture de la sérotonine-noradrénaline) utilisés dans le traitement de la douleur neuropathique.
4. Les Grandes Classifications de la Douleur
Comprendre la physiopathologie permet de classer les douleurs et d’adapter le traitement :
| Type de douleur | Mécanisme | Exemples |
|---|---|---|
| Nociceptive | Activation normale des nocicepteurs | Douleur post-opératoire, arthrose |
| Neuropathique | Lésion du système nerveux | Zona, neuropathie diabétique, sciatique |
| Nociplastique | Dysfonction des systèmes de modulation | Fibromyalgie, colon irritable |
| Mixte | Combinaison de mécanismes | Lombalgies chroniques, cancer |
5. De la Physiopathologie à la Thérapeutique
La connaissance des mécanismes de la douleur permet de cibler précisément les traitements :
- Anti-inflammatoires (AINS, corticoïdes) → agissent sur la sensibilisation périphérique
- Morphine et opioïdes → agissent sur les récepteurs µ au niveau médullaire et supraspinal
- Antiépileptiques (gabapentine, prégabaline) → stabilisent les membranes neuronales hyperexcitables
- Antidépresseurs (duloxétine, amitriptyline) → renforcent les contrôles descendants inhibiteurs
- Anesthésiques locaux (lidocaïne, bupivacaïne) → bloquent la conduction dans les fibres nociceptives
- Kétamine → antagoniste des récepteurs NMDA, prévient la sensibilisation centrale
Conclusion : Vers une Prise en Charge Globale et Multidisciplinaire
La physiopathologie de la douleur est un processus complexe, multi-étagé, qui dépasse largement la simple “transmission d’un signal”. Elle implique des interactions entre le système nerveux périphérique, la moelle épinière, le cerveau et les systèmes émotionnels.
Cette compréhension est la clé d’une prise en charge efficace et personnalisée. Face à une douleur chronique, une approche biopsychosociale — associant traitements médicamenteux, kinésithérapie, psychothérapie et éducation thérapeutique — s’impose comme le gold standard actuel.
Points clés à retenir :
- La nociception se déroule en 3 étapes : détection → relais médullaire → intégration cérébrale
- Les fibres Aδ transmettent la douleur aiguë ; les fibres C, la douleur diffuse et persistante
- Les récepteurs NMDA sont au cœur de la sensibilisation centrale et de la chronicisation
- Le système peut amplifier (hyperalgésie) ou inhiber (contrôles descendants) la douleur
- Chaque mécanisme physiopathologique correspond à une ou plusieurs cibles thérapeutiques



