Phosphorylation Oxydative et Chaîne Respiratoire Mitochondriale : Le Moteur Énergétique de la Cellule
La chaîne respiratoire mitochondriale est l’un des mécanismes les plus fascinants du vivant. Elle transforme l’énergie chimique des aliments en ATP, la monnaie énergétique universelle de la cellule. Comprendre son fonctionnement est essentiel en biochimie, en médecine et dans la recherche sur les maladies métaboliques.
I. Introduction : La Mitochondrie, Centrale Énergétique Cellulaire
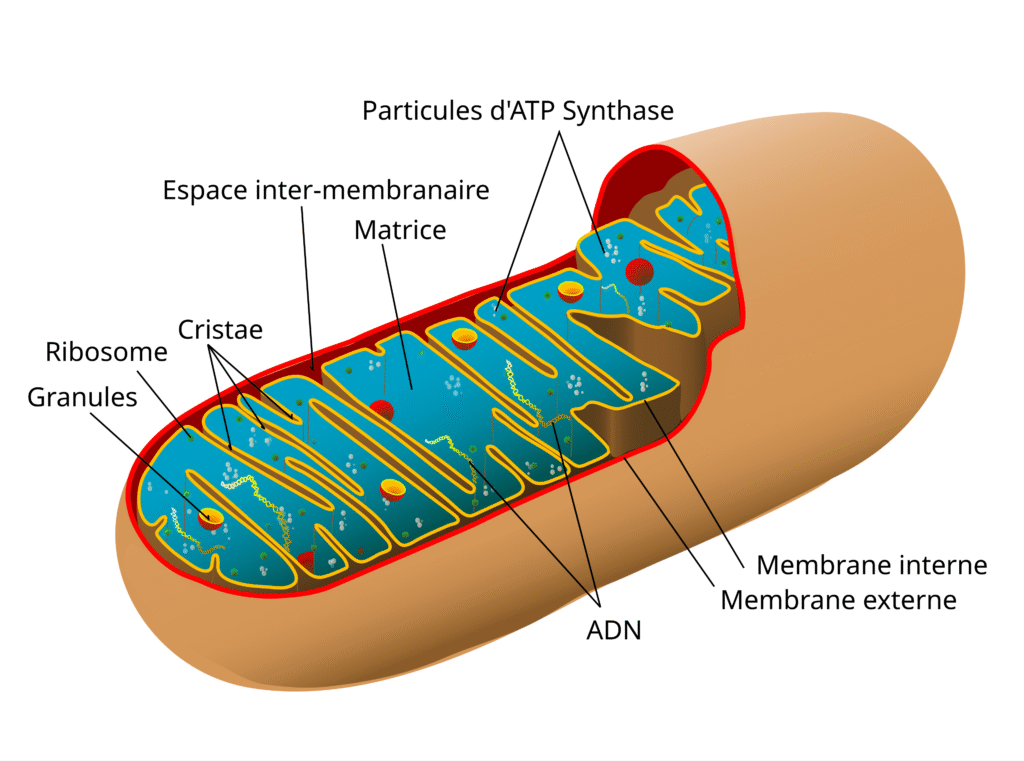
La mitochondrie est souvent appelée “la centrale énergétique de la cellule”, et pour cause : elle produit environ 90 % de l’ATP nécessaire au fonctionnement des cellules eucaryotes. Au cœur de cette production se trouve la chaîne respiratoire mitochondriale (CRM), un système de transport d’électrons localisé dans la membrane interne mitochondriale.
Cette membrane interne est fortement repliée en structures appelées crêtes mitochondriales, ce qui augmente considérablement sa surface et donc sa capacité à produire de l’ATP. Chez l’homme adulte, le corps synthétise et consomme environ 40 kg d’ATP par jour au repos — un chiffre qui illustre l’importance capitale de ce système.
Qu’est-ce que la chaîne respiratoire mitochondriale ?
La CRM est un ensemble de complexes protéiques enchâssés dans la membrane interne de la mitochondrie. Elle constitue la voie finale de l’oxydation des coenzymes réduits (NADH et FADH₂) issus du catabolisme : glycolyse, cycle de Krebs, bêta-oxydation des acides gras.
Le processus global peut être résumé ainsi :
- Les coenzymes réduits (NADH, FADH₂) cèdent leurs électrons à la chaîne de transporteurs.
- Ces électrons passent par une cascade de réactions d’oxydoréduction, libérant de l’énergie à chaque étape.
- L’accepteur final des électrons est l’oxygène moléculaire (O₂), réduit en eau (H₂O).
- L’énergie libérée est couplée à la synthèse d’ATP à partir d’ADP et de phosphate inorganique.
II. Les Acteurs Moléculaires : 5 Complexes Protéiques
La CRM est constituée de 5 complexes protéiques principaux et de deux transporteurs mobiles. Voici leur rôle détaillé.
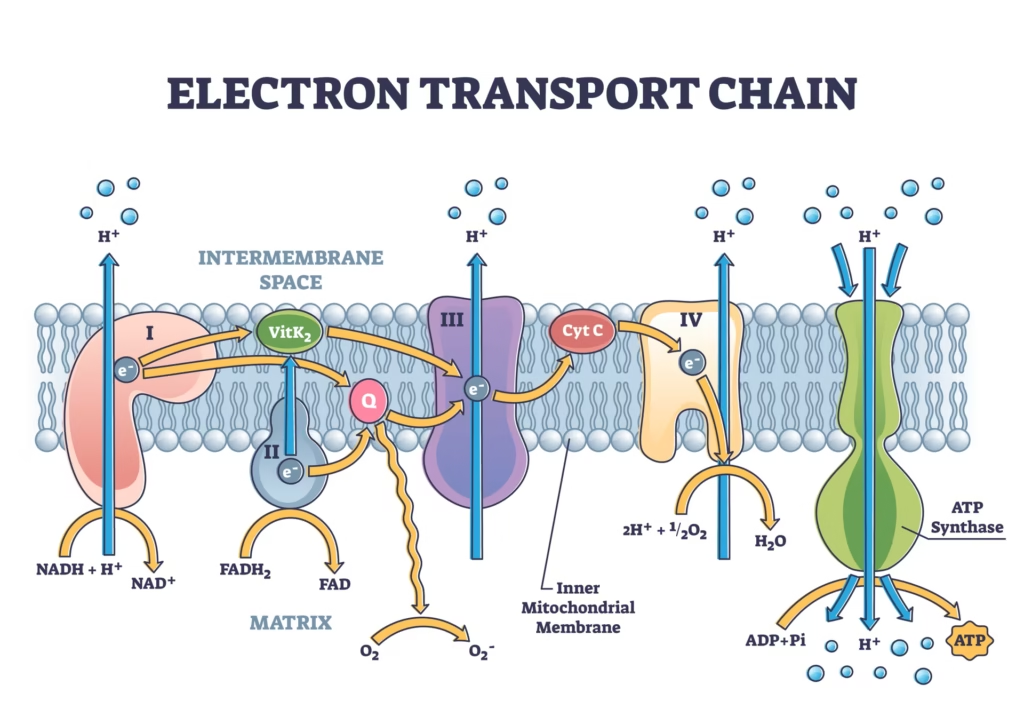
Complexe I : NADH-CoQ Oxydoréductase (NADH Déshydrogénase)
Le Complexe I est le premier et le plus grand complexe de la CRM. Il joue un rôle de pompe à protons.
- Il oxyde le NADH en NAD⁺, récupérant ainsi 2 électrons.
- Ces électrons sont transférés au CoQ (Coenzyme Q ou ubiquinone), présent dans les lipides membranaires.
- Simultanément, il pompe 4 ions H⁺ de la matrice vers l’espace intermembranaire.
- Il est aussi appelé NADH déshydrogénase et contient des groupements fer-soufre (Fe-S).
Point clé : Le Complexe I est l’entrée des électrons provenant du NADH dans la chaîne respiratoire.
Complexe IV : Succinate-CoQ Réductase (Complexe II)
Contrairement aux autres complexes, le Complexe IV ne pompe pas de protons. Son rôle est plus discret mais indispensable.
- Il oxyde le succinate (issu du cycle de Krebs) en fumarate via la succinate déshydrogénase.
- Le FADH₂ formé transfère ses électrons au CoQ, qui devient ubiquinol (QH₂).
- Le FADH₂ ne quitte jamais le complexe : ses électrons sont directement transmis.
Pourquoi moins d’ATP ? Parce que l’absence de pompage de H⁺ signifie que moins d’énergie libre est dégagée. Par conséquent, l’oxydation du FADH₂ produit environ 1,5 ATP contre 2,5 ATP pour le NADH (selon les valeurs actuelles de la P/O ratio).
Complexe II : CoQ-Cytochrome C Oxydoréductase (Complexe III)
C’est la deuxième pompe à protons de la CRM. Il contient 2 types de cytochrome (b et c1) ainsi qu’une protéine Fe-S.
- Il transfère les électrons de QH₂ au cytochrome C, un petit transporteur protéique mobile.
- En même temps, il pompe des H⁺ de la matrice vers l’espace intermembranaire.
- Le mécanisme “cycle Q” permet d’optimiser ce transfert en recyclant les électrons entre ubiquinol et semi-quinone.
Les cytochromes sont des protéines héminiques (contenant du fer) qui changent d’état d’oxydation (Fe²⁺ ↔ Fe³⁺) pour assurer le transport des électrons.
Complexe III : Cytochrome C Oxydase (Complexe IV)
C’est le dernier complexe enzymatique de pompage et la porte de sortie des électrons.
- Il reçoit les électrons du cytochrome C réduit.
- Ces électrons réduisent l’O₂ moléculaire en eau selon la réaction :
4 Cyt C (Fe²⁺) + 4 H⁺ + O₂ → 4 Cyt C (Fe³⁺) + 2 H₂O
- Il pompe simultanément des H⁺ vers l’espace intermembranaire.
- Il contient 2 noyaux hèmes identiques (a et a3), chacun associé à un cuivre.
Ce complexe est inhibé par le cyanure (CN⁻) et le monoxyde de carbone (CO), deux poisons respiratoires mortels qui bloquent la réduction de l’oxygène.
Complexe V : ATP Synthase Mitochondriale (F₁F₀-ATPase)
Le Complexe V est l’enzyme finale, celle qui fabrique réellement l’ATP.
- Il est constitué de deux parties : une portion F₀ enchâssée dans la membrane interne, et une tête F₁ (corpuscule de Green) qui fait saillie dans la matrice.
- Contrairement aux complexes I, II, III, il fonctionne à l’inverse : il laisse revenir les H⁺ de l’espace intermembranaire vers la matrice.
- Ce flux de protons entraîne la rotation mécanique de la F₀, qui actionne la synthèse d’ATP par la F₁.
- La réaction de phosphorylation est endergonique (ΔG°’ = +7,3 kcal/mole) et nécessite du magnésium (Mg²⁺).
III. Les Transporteurs Mobiles : CoQ et Cytochrome C
Deux molécules mobiles assurent le relais entre les complexes fixes :
Le Coenzyme Q (ubiquinone / CoQ) est une petite molécule liposoluble qui diffuse librement dans la bicouche lipidique de la membrane interne. Il collecte les électrons des complexes I et IV (succinate-CoQ réductase) et les cède au Complexe II (bc1). Il peut accepter 1 ou 2 électrons (ubiquinone → semi-quinone → ubiquinol).
Le Cytochrome C est une petite protéine hydrosoluble périphérique à la membrane interne. Il transporte les électrons du Complexe II vers le Complexe III (cytochrome c oxydase), un électron à la fois grâce au couple Fe²⁺/Fe³⁺.
IV. Potentiel Redox et Énergie Libre : Les Fondements Thermodynamiques
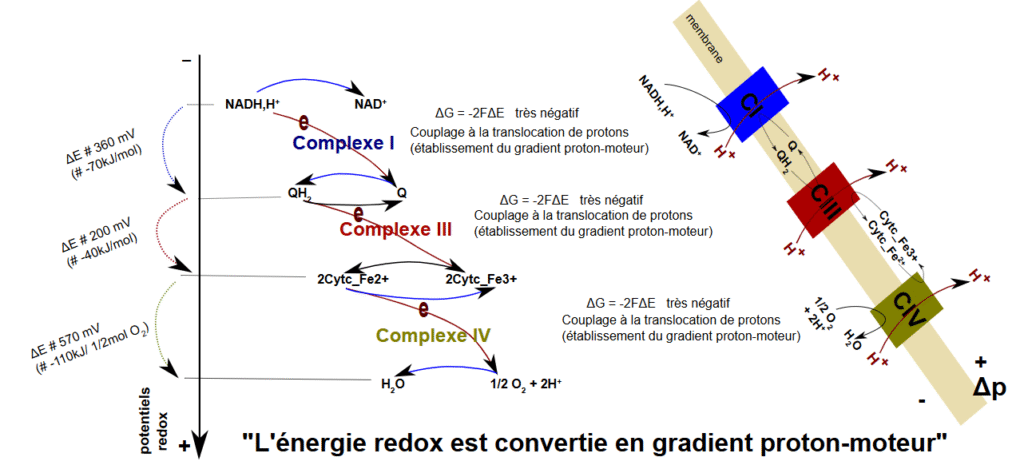
Le concept de potentiel redox (ΔE°’)
Le potentiel redox mesure l’affinité d’une substance pour les électrons :
- Un potentiel négatif → affinité faible pour les électrons (bons donneurs d’électrons)
- Un potentiel positif → affinité élevée pour les électrons (bons accepteurs d’électrons)
Les électrons circulent toujours des potentiels les plus négatifs (NADH : -0,32 V) vers les potentiels les plus positifs (O₂/H₂O : +0,82 V), selon le gradient de potentiel redox.
La relation ΔG°’ = – n F ΔE°’
La variation d’énergie libre est directement reliée à la variation de potentiel redox :
ΔG°' = - n × F × ΔE°'
Où :
- n = nombre d’électrons transférés
- F = constante de Faraday = 23,06 kcal/V·mol
- ΔE°’ = différence de potentiel redox (en Volts)
Exemple : Réduction du pyruvate par le NADH
- Potentiel du couple (NAD⁺/NADH) = -0,32 V
- Potentiel du couple (Pyruvate/Lactate) = -0,19 V
- ΔE°’ = (-0,19) – (-0,32) = +0,13 V
- ΔG°’ = -(2) × (23,06) × (0,13) = -6 kcal/mole → réaction exergonique
Bilan global : NADH → O₂
Le flux d’électrons du NADH vers l’oxygène libère une quantité considérable d’énergie :
NADH + H⁺ + ½ O₂ → NAD⁺ + H₂O
ΔE°' = +1,14 V
ΔG°' = -52,6 kcal/mole
Cette énergie est fractionnée en 3 sauts énergétiques correspondant chacun à la synthèse d’1 ATP :
| Réaction | E°’ (V) | ΔE°’ | ATP |
|---|---|---|---|
| NAD/NADH → FP flavoprotéine | -0,32 → -0,12 | +0,20 | 1 ATP |
| Cyt c Fe³⁺/Fe²⁺ | +0,08 → +0,25 | +0,17 | 1 ATP |
| ½ O₂ / H₂O | +0,29 → +0,82 | +0,53 | 1 ATP |
V. La Théorie Chimiosmotique de Peter Mitchell (1961)
En 1961, le biochimiste britannique Peter Mitchell propose sa révolutionnaire hypothèse chimiosmotique, pour laquelle il reçut le Prix Nobel de Chimie en 1978.
Le principe fondamental
Mitchell propose que le transfert d’électrons et la synthèse d’ATP ne sont pas couplés par un intermédiaire covalent de haute énergie (comme le 1,3-BPG dans la glycolyse), mais par un gradient électrochimique de protons à travers la membrane interne.
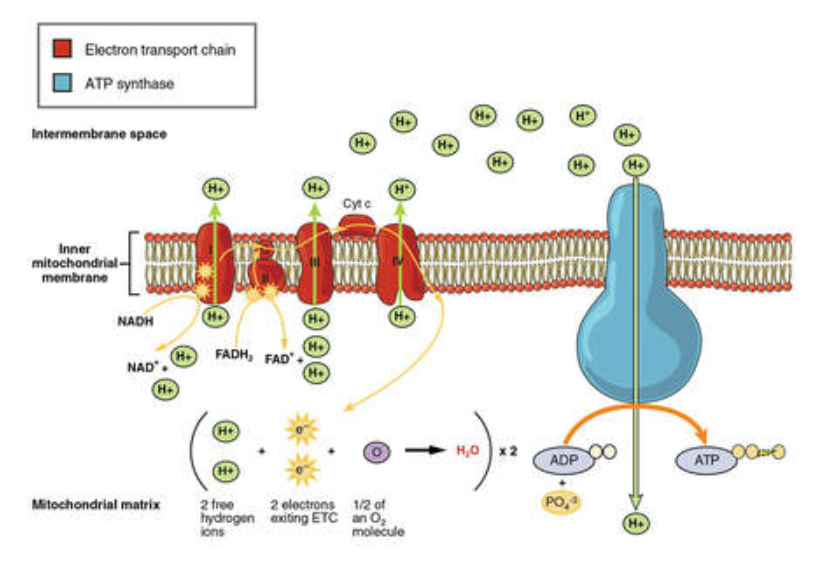
Le mécanisme se déroule en deux temps :
Phase 1 — Création du gradient : Les complexes I, II et III pompent des H⁺ de la matrice vers l’espace intermembranaire. La membrane interne étant imperméable aux protons, il s’établit un gradient de pH (l’espace intermembranaire est plus acide) et un gradient électrique (l’espace intermembranaire est chargé positivement). Ensemble, ils forment la force protomotrice.
Phase 2 — Utilisation du gradient : Le Complexe V (ATP synthase) laisse refluer les H⁺ de l’espace intermembranaire vers la matrice. Ce flux de protons à travers le canal F₀ entraîne la rotation du rotor de l’ATP synthase, couplée mécaniquement à la synthèse d’ATP par la tête F₁.
Analogie : La force protomotrice fonctionne comme l’eau d’un barrage : l’énergie accumulée en pompant les protons “en amont” est libérée quand ils “redescendent” à travers l’ATP synthase.
Le rôle de l’ATP-Translocase et de la Porine
Une fois l’ATP synthétisé dans la matrice, il doit être exporté vers le cytoplasme. Deux protéines assurent ce transport :
- L’ATP-Translocase (ou ANT) : échange 1 ATP⁴⁻ de la matrice contre 1 ADP³⁻ du cytoplasme à travers la membrane interne.
- La Porine (VDAC) : canal non sélectif dans la membrane externe permettant le passage de l’ATP/ADP.
VI. Fonctionnement Global de la CRM : Vue d’Ensemble
Voici la séquence fonctionnelle complète de la chaîne respiratoire :
Complexe I (NADH-CoQ réductase) :
- Oxyde le NADH en NAD⁺
- Réduit le CoQ en QH₂
- Pompe 4 H⁺ de la matrice vers l’EIM
Complexe IV (Succinate-CoQ réductase) :
- Oxyde le succinate en fumarate
- Réduit le CoQ en QH₂ (via FADH₂)
- Ne pompe pas de H⁺
Complexe II (QH₂-Cytochrome c réductase) :
- Oxyde le QH₂ en CoQ
- Réduit le cytochrome C ferrique (Fe³⁺) en ferreux (Fe²⁺)
- Pompe des H⁺ de la matrice vers l’EIM
Complexe III (Cytochrome c oxydase) :
- Oxyde le cytochrome C ferreux en ferrique
- Réduit l’O₂ en H₂O
- Pompe des H⁺ de la matrice vers l’EIM
Complexe V (ATP Synthase) :
- Laisse revenir les H⁺ de l’EIM vers la matrice
- Utilise cette énergie pour phosphoryler l’ADP en ATP
L’activité combinée des complexes I, II et III crée une grande différence de concentration en H⁺ et un gradient électrique à travers la membrane interne, qui est exploité par le Complexe V pour produire l’ATP.
VII. Inhibiteurs et Découplants : Applications Cliniques
Inhibiteurs spécifiques
La CRM est sensible à plusieurs toxiques qui bloquent des complexes spécifiques :
- Roténone (insecticide) : inhibe le Complexe I → ↓ oxydation du NADH
- Antimycine A : inhibe le Complexe II → ↓ transfert QH₂ → Cyt C
- Cyanure (CN⁻), CO, Azide (N₃⁻) : inhibent le Complexe III → ↓ réduction de l’O₂
- Oligomycine : inhibe le Complexe V (bloque le canal F₀) → ↓ synthèse ATP
Découplants (protonophores)
Les découplants permettent aux protons de traverser la membrane interne sans passer par l’ATP synthase. Ils dissipent le gradient de protons sous forme de chaleur sans synthèse d’ATP.
- 2,4-Dinitrophénol (DNP) : autrefois utilisé comme “brûleur de graisse”, il peut être mortel.
- Thermogénine (UCP1) : découplant physiologique présent dans le tissu adipeux brun des nouveau-nés et animaux hibernants, responsable de la thermogenèse.
VIII. Maladies Mitochondriales : Quand la CRM Dysfonctionne
Les dysfonctionnements de la chaîne respiratoire sont à l’origine de nombreuses maladies mitochondriales, souvent sévères et à transmission maternelle (car l’ADN mitochondrial est d’origine maternelle).
Parmi les plus connues :
- Syndrome de Leigh : encéphalomyopathie progressive liée à des mutations des complexes I, III, IV ou V.
- MELAS (Myopathie mitochondriale, Encéphalopathie, Acidose Lactique, Stroke-like episodes) : mutation de l’ARNt mitochondrial.
- Neuropathie optique de Leber (NOHL) : mutation du Complexe I, entraînant une perte de vision.
La recherche actuelle explore des thérapies géniques et des supplémentations en cofacteurs (CoQ10, riboflavine, L-carnitine) pour traiter ces maladies.
Conclusion : La CRM, Chef-d’Œuvre de l’Évolution Biochimique
La chaîne respiratoire mitochondriale est un chef-d’œuvre d’efficacité moléculaire. En couplant le flux d’électrons à la création d’un gradient de protons, puis en utilisant ce gradient pour synthétiser l’ATP, la cellule extrait le maximum d’énergie des nutriments.
À retenir :
- La CRM est localisée dans la membrane interne mitochondriale.
- Elle comprend 5 complexes protéiques et 2 transporteurs mobiles (CoQ et Cyt C).
- Les électrons circulent du NADH/FADH₂ → CoQ → Cyt C → O₂.
- L’énergie libérée crée un gradient de protons (théorie chimiosmotique de Mitchell).
- L’ATP synthase utilise ce gradient pour synthétiser l’ATP.
- L’oxydation d’un NADH produit ~2,5 ATP ; celle d’un FADH₂ produit ~1,5 ATP.
La compréhension fine de ce mécanisme ouvre des perspectives thérapeutiques majeures pour le traitement des maladies métaboliques, neurodégénératives et du cancer.
Abréviations : M = Matrice | EIM = Espace IntерMembranaire | H⁺ = Proton | e⁻ = Électron | CRM = Chaîne Respiratoire Mitochondriale



