Les Gaz Nobles : Propriétés, Histoire et Applications Pharmaceutiques — Guide Complet pour Étudiants en Pharmacie
Les gaz nobles sont bien plus que de simples curiosités du tableau périodique. De l’hélium utilisé pour les plongées profondes au xénon employé comme anesthésique, ces éléments discrets jouent un rôle croissant en médecine et en pharmacie. Ce guide complet vous permettra de maîtriser l’essentiel du cours, du fondamental au clinique.

I. Généralités et Structure Électronique
1.1 Une couche de valence fermée : la clé de leur comportement
Les gaz nobles appartiennent au groupe 18 du tableau périodique (anciennement appelé groupe VIIIA ou groupe 0). Leur caractéristique fondamentale est de posséder une couche de valence complètement remplie :
- Hélium (He) : 2 électrons dans la couche 1s → configuration 1s²
- Tous les autres gaz nobles : réalisent l’octet, soit 8 électrons de valence dans les couches ns et np
Cette saturation électronique explique leur très faible réactivité chimique, qui a longtemps conduit les chimistes à les qualifier de « gaz inertes ».
💡 Point clé pour l’examen : La stabilité des gaz nobles est liée à la règle de l’octet (ou duet pour l’hélium). C’est cette même règle qui guide la formation des liaisons chimiques dans toute la chimie organique et minérale.
1.2 Classification et configurations électroniques
| n | Élément | Symbole | Configuration électronique | Étymologie |
|---|---|---|---|---|
| 1 | Hélium | He | 1s² | Du grec hélios = soleil (découvert par spectroscopie solaire, 1868) |
| 2 | Néon | Ne | [He] 2s² 2p⁶ | Du grec néos = nouveau (Ramsay et Travers, 1898) |
| 3 | Argon | Ar | [Ne] 3s² 3p⁶ | Du grec argos = paresseux/inactif (Rayleigh et Ramsay, 1894) |
| 4 | Krypton | Kr | [Ar] 4s² 3d¹⁰ 4p⁶ | Du grec kryptos = caché (Ramsay et Travers, 1898) |
| 5 | Xénon | Xe | [Kr] 5s² 4d¹⁰ 5p⁶ | Du grec xenos = étranger (Ramsay et Travers, 1898) |
| 6 | Radon | Rn | [Xe] 6s² 4f¹⁴ 5d¹⁰ 6p⁶ | Gaz radioactif (P. et M. Curie, 1899) |
| 7 | Oganesson | Og | [Rn] 7s² 5f¹⁴ 6d¹⁰ 7p⁶ | Découvert au début du XXIe siècle (2015) |
⚠️ Cas particulier — L’Oganesson (Og, Z=118) : Cet élément, découvert au début du XXIe siècle, prolonge le groupe 18. Toutefois, ses propriétés chimiques restent largement méconnues. Les effets relativistes d’un noyau atomique très chargé sur son cortège électronique pourraient en altérer suffisamment les propriétés pour qu’il soit probablement solide et non gazeux, et ne soit donc plus nécessairement un « gaz noble » au sens habituel.
II. Histoire de la Découverte des Gaz Nobles
2.1 Une découverte née d’une anomalie
Jusqu’à la fin du XIXe siècle, les scientifiques croyaient que l’air était exclusivement composé d’azote et d’oxygène. C’est en 1893 que le physicien anglais John William Strutt, lord Rayleigh (1842–1919) suspecta pour la première fois la présence d’un autre gaz dans un échantillon d’azote extrait de l’air.
Il remarqua que l’azote obtenu à partir de l’air était légèrement plus dense que l’azote obtenu par voie chimique — une différence infime mais reproductible, signe qu’un intrus se cachait dans ce gaz.
2.2 William Ramsay et l’isolement des gaz nobles
C’est au chimiste anglais William Ramsay (1852–1916) que l’on doit d’avoir isolé et identifié les gaz nobles. Sa démarche expérimentale est remarquable de rigueur :
En faisant réagir du calcium métallique avec un échantillon de diazote provenant de l’air, Ramsay observa qu’environ 1% du gaz (en volume) ne réagissait pas. Si le diazote avait été pur, il aurait réagi entièrement avec le calcium.
En raison de l’inertie totale de ce résidu, il lui donna le nom d’argon (du grec argos = paresseux). En poursuivant ses analyses, il découvrit que ce gaz résiduel était en réalité constitué de 5 composants distincts :
- L’argon — en proportion majoritaire
- L’hélium (hélios = soleil) — en très petite quantité
- Le néon (néos = nouveau) — en très petite quantité
- Le krypton (kryptos = caché) — en très petite quantité
- Le xénon (xenos = étranger) — en très petite quantité
2.3 La récompense Nobel
En 1904, ces découvertes majeures furent couronnées par les plus hautes distinctions scientifiques :
- Lord Rayleigh → Prix Nobel de Physique
- William Ramsay → Prix Nobel de Chimie
III. Présence à l’État Naturel
3.1 Abondance dans l’atmosphère
Comme Ramsay l’avait établi, les gaz nobles représentent près de 1% de l’atmosphère terrestre. Cependant, cette proportion est presque entièrement attribuable à l’argon. Les autres gaz nobles sont présents en quantités infimes, ce qui justifie pourquoi on les appelait autrefois « gaz rares » — une désignation aujourd’hui jugée inexacte pour l’argon.
| Gaz noble | Abondance dans l’air (% vol.) | État physique à 25°C |
|---|---|---|
| Hélium (He) | 0,000524 % | Gaz |
| Néon (Ne) | 0,001818 % | Gaz |
| Argon (Ar) | 0,934 % | Gaz |
| Krypton (Kr) | 0,000114 % | Gaz |
| Xénon (Xe) | 0,0000087 % | Gaz |
| Radon (Rn) | Traces (radioactif) | Gaz |
💡 Remarque terminologique : En raison de la relative abondance de l’argon (0,934% de l’atmosphère, soit plus que le CO₂), le terme « gaz rares » est inexact. Le terme officiel et recommandé est « gaz nobles ».
IV. Propriétés Physico-Chimiques
4.1 Propriétés physiques
Leur nature monoatomique et non polaire en fait des gaz quasi parfaits, ce qui justifie l’intérêt porté à leurs propriétés physiques. Ils obéissent de façon très précise à la loi des gaz parfaits (PV = nRT), ce qui en fait d’excellents étalons en physique.
Les points de fusion et d’ébullition sont extrêmement bas, en raison de la faiblesse des interactions de Van der Waals entre atomes isolés :
| He | Ne | Ar | Kr | Xe | Rn | |
|---|---|---|---|---|---|---|
| Tf (°C) | -272 | -249 | -189 | -157 | -112 | -71 |
| Teb (°C) | -269 | -246 | -186 | -153 | -107 | -65 |
💡 Tendance à retenir : Les températures de fusion et d’ébullition augmentent avec le numéro atomique. Cela s’explique par l’augmentation de la polarisabilité et donc des forces de London avec la taille de l’atome.
4.2 Propriétés chimiques et réactivité
Inertie chimique des éléments légers
- Hélium → totalement inerte chimiquement
- Néon → totalement inerte chimiquement
- Argon → inerte chimiquement ; la première molécule impliquant l’argon (HArF) a été synthétisée en 2000, à très basse température
- Radon → inerte ; aucun composé stable connu à ce jour, bien que des réactions avec le fluor soient théoriquement envisagées
La révolution de 1962 : la fin du mythe de l’inertie totale
Avant 1962, tous les manuels de chimie affirmaient catégoriquement que les gaz nobles ne formaient aucun composé chimique. Cette certitude fut ébranlée par une expérience décisive :
Neil Bartlett, alors à l’Université de Colombie-Britannique, travaillait avec un agent oxydant extrêmement puissant : l’hexafluorure de platine (PtF₆). En mélangeant du xénon et de PtF₆ dans une enceinte réactionnelle, il observa qu’une réaction bien définie se produisait, donnant un solide orangé. Cette découverte bouleversa la chimie des éléments et incita d’autres équipes à explorer la réactivité du xénon.
En moins d’un an, de nombreux composés du xénon furent synthétisés.
Les composés connus des gaz nobles
Le fluor, gaz corrosif jaune pâle et oxydant le plus puissant de la chimie, réagit avec le krypton et le xénon pour former des fluorures stables :
- KrF₂ (fluorure de krypton)
- XeF₂, XeF₄, XeF₆ (fluorures de xénon)
Le xénon forme également des composés avec l’oxygène :
- XeO₃, XeO₄ (oxydes de xénon)
- XeO₃F₂ (oxyfluorure)
- (XeO₆)⁴⁻ et (XeF₈)²⁻ (formes ioniques)
⚠️ Points importants à retenir :
- La liaison dans ces composés peut être rationalisée par la théorie des orbitales moléculaires
- Ces composés restent instables dans les conditions normales
- Seuls des composés du xénon ainsi qu’un fluorure du krypton ont été synthétisés à ce jour
- La non-réactivité est rigoureusement vraie uniquement jusqu’à l’argon
4.3 Préparation et obtention
- Hélium : essentiellement obtenu lors de la purification du gaz naturel de certains gisements géologiques. Il existe aujourd’hui une crise mondiale de production d’hélium en raison de la déplétion des réservoirs naturels et de la forte demande industrielle et médicale.
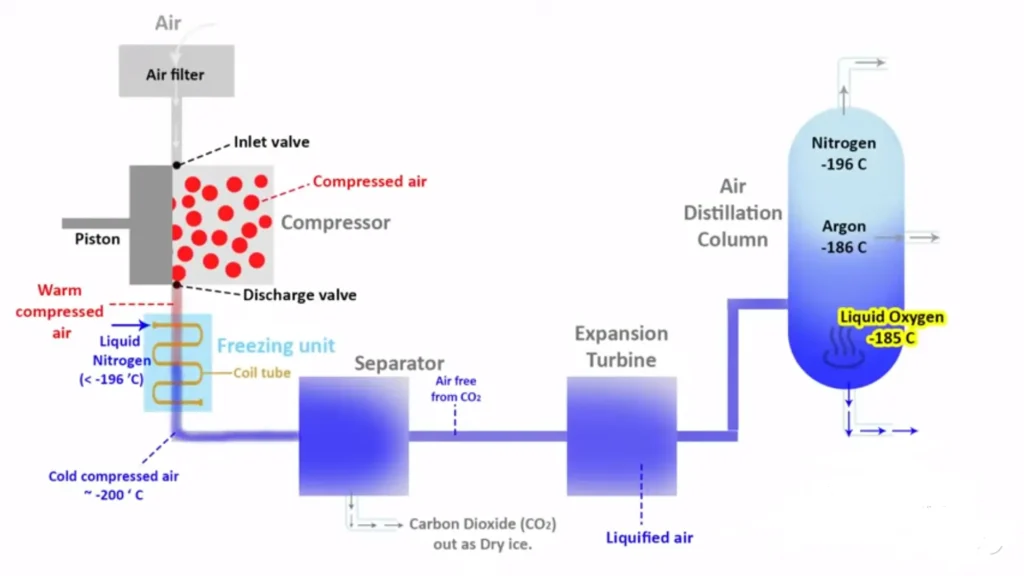
- Tous les autres gaz monoatomiques (sauf le radon) : obtenus par distillation fractionnée de l’air liquide. Cette technique industrielle repose sur les différences de points d’ébullition entre les constituants de l’air.
- Hélium : peut aussi être isolé en petite quantité comme produit de désintégration radioactive (particules alpha = noyaux d’hélium-4).
V. Usages Industriels
5.1 Hélium (He)
Après l’hydrogène, l’hélium est l’élément le plus abondant de l’univers (environ 24% de la masse de l’univers observable).
Ses principales applications industrielles :
- Ballons et dirigeables : sa faible masse volumique et son incombustibilité (contrairement à l’hydrogène) en font le gaz de remplissage idéal — un avantage de sécurité considérable
- Mélanges respiratoires pour plongeurs : sa faible solubilité dans les tissus humains permet de remplacer avantageusement l’azote dans les mélanges respiratoires, évitant ainsi l’accident de décompression (formation de bulles gazeuses dans les tissus) lors des plongées profondes
- Tubes luminescents : il produit une lumière blanche ivoire, pouvant être transformée en jaune doré par des verres filtrants jaunes
- IRM médicale : l’hélium liquide (à -269°C) est indispensable au refroidissement des aimants supraconducteurs des appareils d’IRM — une application médicale majeure et très gourmande en hélium
5.2 Néon (Ne)
Le néon est principalement utilisé dans les tubes luminescents, où il produit une lumière rouge caractéristique, virant au bleu intense en présence de vapeurs de mercure, ou au vert si le tube est réalisé en verre brun.
5.3 Argon (Ar)
L’argon est le plus polyvalent des gaz nobles industriels :
- Ampoules électriques à incandescence : il conduit mal la chaleur, permettant au filament de tungstène d’atteindre des températures de 2 500°C sans se consumer rapidement
- Tubes luminescents : la lumière émise est bleu rougeâtre
- Gaz de protection en soudure : son inertie chimique protège les métaux fondus de l’oxydation par l’air pendant la soudure (soudure TIG/MIG)
- Inertage pharmaceutique : utilisé pour protéger les médicaments sensibles à l’oxydation lors de leur conditionnement
5.4 Krypton (Kr)
Comme l’argon, il sert de gaz de remplissage des ampoules à incandescence, avec une efficacité encore supérieure. La lumière émise dans les tubes luminescents est verte-liliacée.
5.5 Xénon (Xe)
Utilisé sous pression élevée dans les lampes à arc électrique servant à éclairer les stades et les projecteurs de cinéma, le xénon assure l’isolation thermique d’un arc pouvant atteindre des températures de 6 000°C.
5.6 Radon (Rn)
Gaz radioactif issu de la désintégration naturelle du radium. Il se transmute en polonium solide et radioactif qui se dépose sur les surfaces et propage ainsi la radioactivité.
⚠️ Risque sanitaire : Le radon est reconnu comme la deuxième cause de cancer du poumon après le tabac. Sa présence dans les sous-sols et les habitations mal ventilées constitue un problème de santé publique important.
VI. Usages Thérapeutiques et Pharmaceutiques
C’est dans ce domaine que les gaz nobles prennent une dimension particulièrement importante pour le pharmacien. Les gaz à usage médical sont des produits de santé destinés à entrer en contact avec des patients, placés sous la responsabilité pharmaceutique.
Depuis 1992, en France, des gaz et des mélanges de gaz médicaux ont le statut de médicament ou de dispositif médical. Les gaz médicinaux font l’objet d’une autorisation de mise sur le marché (AMM). La fabrication et la distribution des gaz médicinaux sont réglementées par le Guide de Bonnes Pratiques de Fabrication (BPF) et le Guide de Bonnes Pratiques de Distribution (BPD). Les laboratoires pharmaceutiques de gaz médicaux sont régulièrement audités par l’ANSM.
6.1 Le Xénon comme agent anesthésique
Le xénon est un anesthésique par inhalation de la famille des gaz nobles, disposant d’une AMM en France (spécialité Xenon 100% v/v, gaz médicinal). Il provoque, selon la dose administrée, la perte réversible de :
- La conscience
- La sensibilité à la douleur
- Les réflexes végétatifs
- La fonction motrice
Il entraîne également une dépression respiratoire et une diminution des réponses circulatoires.
Mécanisme d’action
L’effet anesthésique et analgésique du xénon provient de l’inhibition non compétitive et sélective des récepteurs NMDA (N-méthyl-D-aspartate), essentiels à la mémoire et à la perception. Ce mécanisme est partagé avec d’autres agents comme la kétamine et le protoxyde d’azote.
Pharmacocinétique
Le coefficient de partage sang/gaz du xénon est le plus faible de tous les anesthésiques par inhalation. Par conséquent, l’induction anesthésique est très rapide (concentration de saturation cérébrale atteinte en quelques minutes), de même que son élimination à l’arrêt de l’anesthésie. La demi-vie maximale dans différents organes est d’environ 100 minutes.
Le xénon est éliminé sous forme inchangée dans l’air expiré, via les alvéoles pulmonaires — il n’est donc pas métabolisé par l’organisme.
Avantages cliniques du xénon
Le xénon est décrit comme un gaz ayant beaucoup des caractéristiques de l’agent anesthésique idéal : dépourvu de toxicité, neutre sur le plan hémodynamique, il possède une cinétique d’action qui autorise des réveils anesthésiques extrêmement rapides.
Ses atouts par rapport aux anesthésiques conventionnels :
- Début et fin d’action très rapides
- Neutralité hémodynamique : pas d’effet sur la pression artérielle ni sur le rythme cardiaque
- Non métabolisé par le foie ou les reins
- Absence d’effet tératogène documenté
- Propriétés neuroprotectrices potentielles (études en cours)
- Non inflammable, non explosif
- Non émetteur de gaz à effet de serre — avantage environnemental majeur par rapport au protoxyde d’azote ou aux éthers halogénés
Limites et précautions d’emploi
- Le xénon possède une concentration alvéolaire minimale (MAC) de 71%, ce qui en fait un anesthésiant 50% plus puissant que le protoxyde d’azote. Il ne semble cependant pas utilisable pour les patients fragiles sur le plan respiratoire parce qu’il n’a de propriétés anesthésiques qu’à des concentrations élevées (supérieures à 60%), ce qui limite à 40% l’apport en dioxygène.
- Risque élevé de nausées et vomissements postopératoires (jusqu’à 45%)
- Coût très élevé dû à la rareté du xénon dans l’atmosphère (0,0000087% de l’air)
- Contre-indiqué en présence de cavités gazeuses (pneumothorax, bulles)
💊 Note pour le pharmacien : Le xénon doit être utilisé exclusivement dans un mélange gazeux contenant au moins 30% d’oxygène, sous peine de risque d’asphyxie. Des systèmes de recyclage permettant de récupérer jusqu’à 80% du xénon consommé sont actuellement développés pour réduire son coût.
Nouvelles perspectives thérapeutiques du xénon
Le xénon fait l’objet de nombreux essais cliniques explorant ses utilisations pour le soulagement du stress avant la chirurgie (concentrations de 55-65%), le traitement du TOC (25% de xénon) et ses propriétés neuroprotectrices, réduisant potentiellement les dommages au cerveau lors de certaines procédures médicales.
6.2 L’Argon en thérapeutique
L’argon bénéficie d’un statut de dispositif médical pour certaines applications :
- Chirurgie par plasma argon (APC) : en endoscopie digestive et bronchique, le plasma d’argon est utilisé pour la coagulation des tissus hémorragiques, l’ablation de lésions superficielles et le traitement de certains cancers superficiels
- Médicament gazeux inhalable à base d’argon contre les déficiences ou défaillances d’organes périphériques : une composition gazeuse contenant une quantité efficace d’argon gazeux est utilisée par inhalation pour prévenir ou traiter une déficience ou défaillance d’au moins un organe périphérique chez un patient. Cette composition contient de préférence entre 15 et 80% en volume d’argon et au moins 21% d’oxygène. La déficience ou défaillance d’organe ainsi traitée peut être transitoire (de moins d’une heure à plusieurs semaines) ou définitive. Les organes concernés peuvent être le foie, les reins et les poumons.
6.3 Le Xénon-133 en médecine nucléaire et imagerie
Le xénon-133 (¹³³Xe), isotope radioactif de demi-vie de 5,245 jours, est utilisé en médecine nucléaire pour :
- Les études fonctionnelles du poumon (mesure de la ventilation pulmonaire)
- L’établissement de certains diagnostics respiratoires par scintigraphie
⚠️ Précaution de stockage : Le xénon se dissout rapidement dans la plupart des plastiques et caoutchoucs. Il doit donc être stocké dans des containers en verre ou en métal scellés.
VII. Réglementation des Gaz Médicaux — Ce que le Pharmacien Doit Savoir
Les gaz à usage médical comprennent les gaz médicinaux (oxygène, protoxyde d’azote, xénon) qui disposent d’une AMM, et les gaz dispositifs médicaux (argon pour chirurgie laser, CO₂ pour cœlioscopie) soumis au marquage CE.
Points réglementaires essentiels :
- Les gaz médicinaux sont soumis aux Pharmacopées européenne, américaine et japonaise
- Leur fabrication respecte les BPF (Bonnes Pratiques de Fabrication) et BPD (Bonnes Pratiques de Distribution)
- Chaque lot est tracé par un numéro de lot et livré avec un certificat d’analyse
- L’étiquetage doit comporter un code couleur normalisé (norme NF EN 1089-3) et les pictogrammes de risque
VIII. Résumé — Tableau Récapitulatif des Usages
| Gaz | Usages industriels | Usages médicaux / pharmaceutiques |
|---|---|---|
| He | Ballons, plongée, IRM (refroidissement) | Mélanges respiratoires plongeurs, support IRM |
| Ne | Tubes luminescents (rouge) | — |
| Ar | Ampoules, soudure, inertage | Chirurgie par plasma (APC), inhalation organes |
| Kr | Ampoules | — |
| Xe | Lampes à arc, projecteurs | Anesthésique inhalé (AMM), imagerie pulmonaire (¹³³Xe), neuroprotection (essais cliniques) |
| Rn | — | Risque sanitaire (cancer du poumon) |

Points Clés à Retenir pour l’Examen
- Les gaz nobles ont une couche de valence saturée (duet pour He, octet pour les autres), ce qui explique leur faible réactivité.
- L’appellation correcte est « gaz nobles » (et non « gaz rares » ou « gaz inertes »).
- Ramsay a isolé les gaz nobles → Prix Nobel de Chimie 1904 ; Rayleigh → Prix Nobel de Physique 1904.
- La réactivité chimique des gaz nobles n’est possible qu’à partir du krypton et surtout du xénon (avec F₂ et O₂ principalement).
- La découverte de Bartlett en 1962 (XePtF₆) a renversé le dogme de l’inertie absolue.
- Le xénon est le seul gaz noble avec une AMM en tant qu’anesthésique général par inhalation en France.
- Son mécanisme anesthésique repose sur l’inhibition des récepteurs NMDA.
- L’argon est utilisé en chirurgie sous forme de plasma (dispositif médical) et comme gaz inhalable pour défaillances d’organes.