Groupe VA — Les Pnictogènes : Propriétés, Chimie et Applications Pharmaceutiques
Cours de Chimie Minérale Pharmaceutique | Niveau : 2ème année Pharmacie Temps de lecture estimé : 20 minutes
Introduction : Qu’est-ce que les Pnictogènes ?
Les pnictogènes (du grec pnigein : étouffer) forment la famille des éléments de la 15ème colonne du tableau périodique (anciennement appelée 5ème colonne principale dans la nomenclature classique).
Ce groupe comprend cinq éléments fondamentaux :
- Azote (N) — gaz essentiel à la vie
- Phosphore (P) — indispensable au métabolisme énergétique
- Arsenic (As) — métalloïde aux propriétés toxiques bien connues
- Antimoine (Sb) — utilisé en médecine tropicale
- Bismuth (Bi) — métal aux applications pharmaceutiques variées

💡 Point clé pour l’étudiant en pharmacie : L’azote et le phosphore sont des éléments biologiquement essentiels, présents dans les acides aminés, les protéines, l’ADN et les molécules énergétiques comme l’ATP.
I. Présentation Générale du Groupe VA
Tableau récapitulatif des pnictogènes
| Élément | Symbole | État physique | Configuration électronique | États d’oxydation |
|---|---|---|---|---|
| Azote | N | Gaz (Éb = −196 °C) | [He] 2s²2p³ | −3, 0, +1, +2, +3, +4, +5 |
| Phosphore | P | Solide polymorphe | [Ne] 3s²3p³ | −3, +3, +5 |
| Arsenic | As | Solide foncé | [Ar] 3d¹⁰4s²4p³ | +3, +5 |
| Antimoine | Sb | Solide, éclat métallique, cassant | [Kr] 4d¹⁰5s²5p³ | +3, +5 |
| Bismuth | Bi | Solide, éclat métallique, cassant | [Xe] 4f¹⁴5d¹⁰6s²6p³ | +3, +5 |
Structure électronique commune
Tous les éléments du groupe VA partagent la même configuration externe : ns²np³, soit 5 électrons de valence.
Cette configuration explique :
- Un état d’oxydation maximal de +5 (utilisation de tous les électrons de valence)
- La tendance à la trivalence pour les éléments lourds (inertie du doublet s)
- Des liaisons majoritairement covalentes
II. État Naturel et Préparation Industrielle
L’azote
L’azote est relativement peu abondant dans la croûte terrestre (17ème rang, 0,03 % en masse). En revanche, il représente 75 % en masse de l’atmosphère sous forme de diazote N₂ — ce qui en fait le corps pur simple le plus abondant accessible sur Terre.
Production industrielle : distillation fractionnée de l’air liquide.
Au laboratoire, on peut obtenir N₂ par décomposition thermique :
NH₄NO₂ → N₂↑ + 2 H₂O
2 NaN₃ → 2 Na + 3 N₂↑
⚠️ Attention : La décomposition de l’azoture de sodium (NaN₃) est utilisée dans les airbags automobiles — réaction explosive très rapide.
Le phosphore
Le phosphore représente 0,12 % en masse de l’écorce terrestre (12ème rang). Il s’y trouve essentiellement sous forme d’apatites : Ca₅X(PO₄)₃ (où X = F⁻, Cl⁻ ou OH⁻).
Préparation industrielle au four électrique vers 1500 °C :
2 Ca₃(PO₄)₂(s) + 10 C(s) + 6 SiO₂(s) → 6 CaSiO₃(l) + 10 CO(g) + P₄(g)
Le phosphore vaporisé est ensuite condensé dans l’eau.
💊 Lien pharmacie : Les apatites sont aussi la forme naturelle du minéral osseux. C’est pourquoi les phosphates de calcium sont utilisés comme recalcifiants.
Arsenic, antimoine et bismuth
Ces trois éléments sont des sous-produits de la métallurgie, obtenus par réduction de leurs oxydes au carbone :
2 As₂O₃ + 6 C → As₄ + 6 CO
Sb₂O₃ + 3 C → 2 Sb + 3 CO
Bi₂O₃ + 3 C → 2 Bi + 3 CO
III. Propriétés Physiques et Chimiques Générales

Du non-métal au métal : une évolution progressive
À l’intérieur du groupe, le caractère métallique augmente de haut en bas :
- N et P : non-métaux
- As et Sb : métalloïdes (propriétés intermédiaires)
- Bi : véritable métal
Cette évolution se traduit directement sur la nature des oxydes :
| Élément | Nature de l’oxyde | Exemple |
|---|---|---|
| N, P | Fortement acide | HNO₃, H₃PO₄ |
| As, Sb | Amphotère | As₂O₃, Sb₂O₃ |
| Bi | Basique | Bi₂O₃ |
Types de liaisons
- Les potentiels d’ionisation élevés empêchent la formation d’ions très chargés
- Sauf avec F, les liaisons sont majoritairement covalentes
- Sb et Bi peuvent perdre des électrons → ions M³⁺ (rapidement hydrolysés en SbO⁺ et BiO⁺)
- Seul l’azote peut capter 3 électrons → ion N³⁻ (nitrure)
IV. Principales Familles de Composés
Les hydrures MH₃
Tous les pnictogènes forment des hydrures volatils de formule MH₃ :
| Composé | Nom | Caractère basique | Stabilité |
|---|---|---|---|
| NH₃ | Ammoniac | Faible base (pKa = 9,25) | Très stable |
| PH₃ | Phosphine | Très faiblement basique | Stable |
| AsH₃ | Arsine | Très faiblement basique | Modérée |
| SbH₃ | Stibine | Négligeable | Faible |
| BiH₃ | Bismuthine | Négligeable | Très instable |
Règle générale : la stabilité, la basicité et la capacité à former des liaisons hydrogène diminuent de NH₃ à BiH₃.
💡 L’azote se distingue par sa capacité à former des hydrures à différents degrés d’oxydation : NH₃ (−3), N₂H₄ hydrazine (−2) et NH₂OH hydroxylamine (−1).
Les oxydes
Les valences +3 et +5 donnent des oxydes aux propriétés bien distinctes :
- N₂O₃ et P₂O₃ : anhydrides acides
- Sb(OH)₃ : amphotère
- Bi₂O₃ : alcalin
- Les oxydes à l’état +5 sont plus acides que ceux à l’état +3
- La force acide décroît de l’azote au bismuth (HNO₃ = acide fort ; H₃PO₄ = acide moyen ; les suivants sont faibles)
Les halogénures
- Formation de tri- et penta-halogénures (sauf NBr₃ et NI₃)
- Liaisons covalentes (sauf BiF₃, ionique)
- Hydrolyse facile, notamment pour Sb et Bi :
SbCl₃ + H₂O → SbOCl + 2 HCl
Les sulfures
- Sulfures d’arsenic, antimoine et bismuth : obtenus par action de H₂S sur leurs sels en milieu acide
- Produits colorés et stables :
2 As + 3 H₂S → 3 H₂ + As₂S₃ (jaune)
Les combinaisons métalliques (nitrures, phosphures, arséniures…)
Les éléments du groupe VA forment des combinaisons métalliques avec les éléments trivalents :
| Composé | Nom |
|---|---|
| Li₃N | Nitrure de lithium |
| Ca₃P₂ | Phosphure de calcium |
| AlAs | Arséniure d’aluminium |
| Mg₃Sb₂ | Antimoniure de magnésium |
Hydrolyse par l’eau :
2 Li₃N + 6 H₂O → 2 NH₃ + 6 LiOH
Ca₃P₂ + 6 H₂O → 2 PH₃ + 3 Ca(OH)₂
2 AlAs + 6 H₂O → 2 AsH₃ + 2 Al(OH)₃
Mg₃Sb₂ + 6 H₂O → 2 SbH₃ + 3 Mg(OH)₂
V. Étude Approfondie de l’Azote et de ses Composés
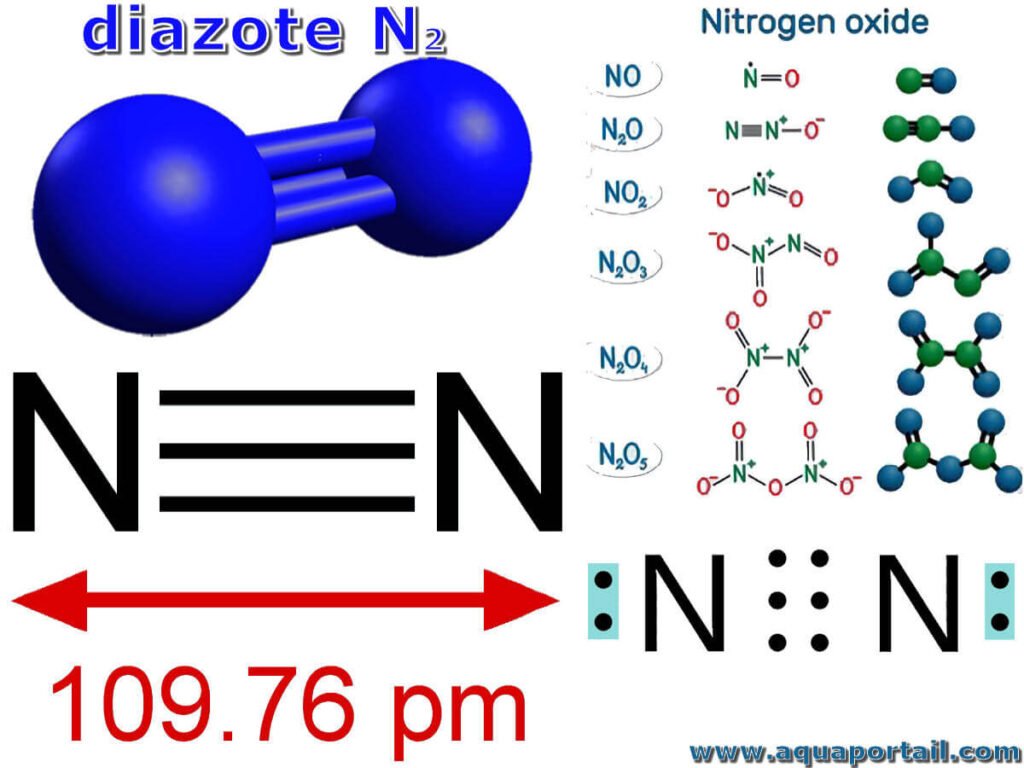
L’azote élémentaire N₂
- Isolé par Rutherford en 1772 ; nommé par Lavoisier (azote = privé de vie en grec)
- Gaz incolore, inodore, dans les conditions normales
- La triple liaison N≡N (énergie de liaison = 945 kJ/mol) rend N₂ très peu réactif
- Multiples degrés d’oxydation : −3, −2, −1, 0, +1, +2, +3, +4, +5
VI. L’Ammoniac NH₃ — Molécule Clé du Groupe VA
Préparation
a) À partir de la cyanamide calcique :
CaC₂ + N₂ → C + CN₂Ca
CN₂Ca + 3 H₂O → 2 NH₃ + CaCO₃ (chaleur + pression)
b) Procédé Haber-Bosch (synthèse industrielle) :
N₂ + 3 H₂ ⇌ 2 NH₃ (catalyseur Fe ou Mo, T = 550 °C, P = 200 atm)
💡 À savoir : Le procédé Haber-Bosch est l’une des inventions les plus importantes du XXe siècle. Il produit environ 150 millions de tonnes d’ammoniac par an dans le monde, servant de base aux engrais azotés qui nourrissent la moitié de l’humanité.
c) Au laboratoire :
NH₄Cl + NaOH → NH₃ + NaCl + H₂O
Propriétés physiques de l’ammoniac
- Gaz incolore à odeur caractéristique suffocante, plus léger que l’air (d = 0,6)
- Très soluble dans l’eau (la solution s’appelle ammoniaque)
- Liaisons hydrogène → constantes physiques élevées : Tf = −77,7 °C, Teb = −33,35 °C
- Structure en pyramide trigonale (N hybridé sp³, doublet libre en position apicale)
- Utilisé comme fluide frigorigène dans l’industrie du froid
Propriétés chimiques de l’ammoniac
NH₃ possède trois comportements chimiques essentiels :
1. NH₃ réducteur
Combustion sans catalyseur :
4 NH₃ + 3 O₂ → 2 N₂ + 6 H₂O
Oxydation catalytique (Pt, 800 °C) → base du procédé Ostwald :
4 NH₃ + 5 O₂ → 4 NO + 6 H₂O
Avec les halogènes :
8 NH₃ + 3 Br₂ → N₂ + 6 NH₄Br
Avec les oxydants forts :
2 NH₃ + NaClO → N₂H₂ + NaCl + H₂O
2. NH₃ base de Lewis
NH₃ possède un doublet libre sur l’azote → base de Lewis.
Réaction avec CO₂ (industriellement : 180 bar, 140 °C) → urée.
En solution aqueuse :
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻ (Kb = 1,8 × 10⁻⁵)
3. NH₃ acide
Dans des conditions spécifiques, NH₃ peut céder un proton et former les anions amidure (NH₂⁻), imidure (NH²⁻) et nitrure (N³⁻) :
2 NH₃(g) + 2 Na(s) → 2 NaNH₂ + H₂
Les oxydes d’azote NOx
| Composé | Formule | Degré d’oxydation de N | Remarque |
|---|---|---|---|
| Protoxyde d’azote | N₂O | +1 | Gaz anesthésique |
| Monoxyde d’azote | NO | +2 | Vasodilatateur médical |
| Dioxyde d’azote | NO₂ | +4 | Polluant atmosphérique |
| Trioxyde de diazote | N₂O₃ | +3 | Anhydride de HNO₂ |
| Tétroxyde de diazote | N₂O₄ | +4 | Forme dimère de NO₂ |
| Pentoxyde de diazote | N₂O₅ | +5 | Anhydride de HNO₃ |
VII. L’Acide Nitrique HNO₃
Préparation
Au laboratoire :
NaNO₃ + H₂SO₄ → HNO₃ + NaHSO₄
Procédé industriel d’Ostwald :
- Synthèse de NH₃ (Haber-Bosch)
- Oxydation catalytique : 2 NH₃ + 5/2 O₂ → 2 NO + 3 H₂O
- Oxydation : 2 NO + O₂ ⇌ 2 NO₂ ⇌ N₂O₄
- Dismutation : N₂O₄ + H₂O ⇌ HNO₂ + HNO₃
- HNO₂ instable : 3 HNO₂ → HNO₃ + 2 NO + H₂O
Bilan global :
2 NO + 3/2 O₂ + H₂O → 2 HNO₃
Propriétés physiques
- Molécule plane, N hybridé sp²
- Liquide incolore ; densité maximale 1,513 pour l’acide pur (acide nitrique fumant)
- Teb = 86 °C
- Libère des fumées rouges à température ambiante (décomposition partielle sous lumière en NO₂)
- Acide commercial : 58-70 %, densité 1,31–1,42, Teb 116–121 °C
Propriétés chimiques
Acide fort de Brønsted :
HNO₃ → H⁺ + NO₃⁻
Réagit avec toutes les bases → sels nitrates très solubles dans l’eau.
Agent oxydant puissant : HNO₃ est capable d’attaquer des métaux comme Cu, Sn et de dissoudre les sulfures peu solubles (NiS, CuS, CoS…).
VIII. Le Phosphore : Oxydes et Oxyacides
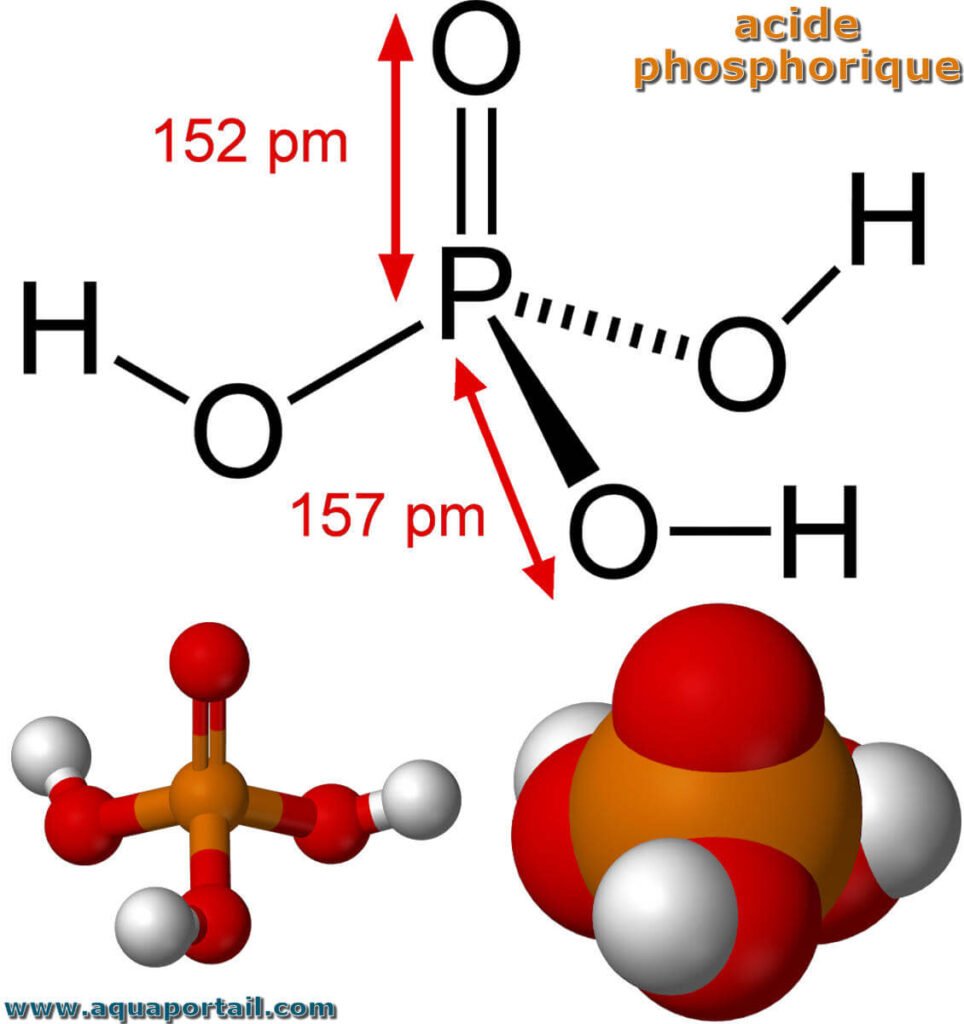
Les oxydes du phosphore
- La molécule PO existe dans les nuages interstellaires
- Les composés significatifs impliquent le phosphore aux degrés +III et +V
- P₄O₁₀ (noté improprement P₂O₅ ou anhydride phosphorique) : agent dessicant très puissant
Les oxyacides du phosphore
| Acide | Formule | Degré d’oxydation P | Nombre de H ionisables | pKa |
|---|---|---|---|---|
| Acide orthophosphorique | H₃PO₄ | +5 | 3 | pKa₁ = 2,1 ; pKa₂ = 7,2 ; pKa₃ = 12,4 |
| Acide phosphoreux | H₃PO₃ | +4 | 2 (1 H lié à P non ionisable) | — |
| Acide hypophosphoreux | H₃PO₂ | +3 | 1 | — |
💊 Application clinique : Aux pH physiologiques (ex. 7,4 dans le sang), l’acide phosphorique se trouve sous forme d’un mélange d’ions H₂PO₄⁻ et HPO₄²⁻ — constituants essentiels du système tampon sanguin.
Les polyphosphates
La présence de groupes P–OH permet des réactions de condensation :
- H₄P₂O₇ (acide diphosphorique/pyrophosphorique) : dimérisation de H₃PO₄
- H₅P₃O₁₀ : acide triphosphorique
- Acides polyphosphoriques : formule générale Hₙ₊₂PₙO₃ₙ₊₁
- Cyclophosphates (métaphosphates) : formule (HPO₃)ₙ
- Ultraphosphates : structures tridimensionnelles ramifiées (hydrolyse facile de la liaison P–O–P)
IX. L’Azote et le Phosphore en Biologie
Rôle de l’azote
L’azote est un constituant fondamental des tissus animaux et végétaux, via les 20 acides aminés naturels de formule NH₂–CHR–CO₂H.
- Le plus simple est la glycine : NH₂–CH₂–CO₂H
- 12 acides aminés sont synthétisés par l’organisme
- 8 acides aminés essentiels doivent être apportés par l’alimentation
L’enchaînement de ces acides aminés par condensation conduit aux polypeptides et aux protéines.
Rôle du phosphore
Le phosphore est présent :
- Dans les os et les dents sous forme d’apatite
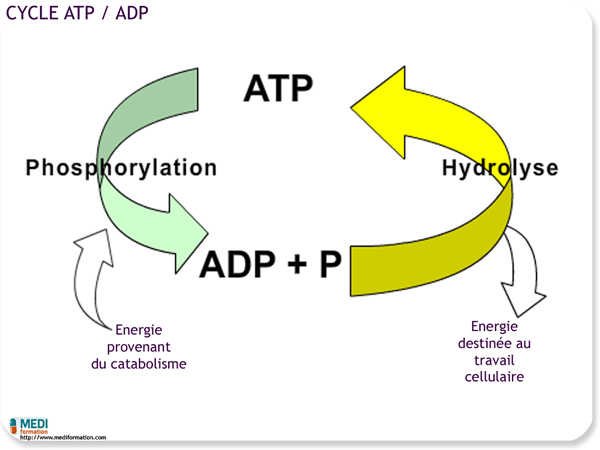
- Dans les molécules énergétiques ADP et ATP (adénosine di- et triphosphate)
- Via des liaisons ester phosphate P–O–R largement utilisées en biochimie
💡 L’ATP est la principale « monnaie énergétique » de la cellule. L’hydrolyse d’une liaison phosphate anhydride libère environ 30 kJ/mol d’énergie libre.
La phosphorylation (ajout d’un groupement phosphate par des enzymes spécialisées) est une voie majeure d’activation sélective des molécules biologiques.
X. Applications Pharmaceutiques des Pnictogènes
A. L’azote et ses composés
1. L’ammoniaque (NH₄OH)
La pharmacopée décrit deux solutions ammoniacales :
| Solution | Concentration en NH₃ | Usage |
|---|---|---|
| Ammoniaque officinale (liste 2) | ~20 % | Sert à préparer la solution diluée |
| Ammoniaque officinale diluée (liste 2) | ~10 % | Usage thérapeutique courant |
Voies d’utilisation de la solution diluée :
- Voie orale : stimulant (ex. potion ammoniacale)
- Inhalation : utilisation historique dans les syncopes (prudemment)
- Usage externe : révulsif
Conservation : flacons à bouchon en verre ou plastique chimique, bien bouchés (éviter la volatilisation du NH₃ et le contact avec le liège/caoutchouc).
2. L’acide nitrique HNO₃ (liste 2)
- Acide fort, se décompose à la lumière → vapeurs nitreuses
- Fume à l’air
- Caustique → usage externe pour traiter les verrues
Conservation : flacons bien bouchés pour éviter le dégagement de vapeurs nitreuses.
3. Les nitrates NO₃⁻
Sels de l’acide nitrique, très solubles dans l’eau.
| Composé | Formule | Usage pharmaceutique |
|---|---|---|
| Nitrate d’argent | AgNO₃ | Usage externe : verrues, plaies bourgeonnantes (très caustique) |
| Nitrate de potassium (salpêtre) | KNO₃ | Voie orale : diurétique |
4. Les nitrites NO₂⁻
Sels de l’acide nitreux HNO₂.
⚠️ Danger : Les nitrites sont méthémoglobinisants — ils transforment l’hémoglobine en méthémoglobine, incapable de transporter l’O₂ → asphyxie cellulaire.
Composés utilisés :
| Composé | Formule | Propriétés et indications |
|---|---|---|
| Nitrite de sodium | NaNO₂ | Vasodilatateur : artériosclérose, HTA, angor, asthme, claudication intermittente |
| Nitrite d’amyle | C₅H₁₁NO₂ | Vasodilatateur puissant ; conservé en ampoules scellées sous azote, à l’abri de la lumière |
5. Le protoxyde d’azote N₂O (« gaz hilarant »)
- Gaz anesthésique
- Effet antalgique et potentialise les anesthésiques administrés simultanément
- Utilisé en anesthésie générale (mélange MEOPA = 50 % N₂O + 50 % O₂ pour analgésie)
6. Le monoxyde d’azote NO
- Premier gaz à usage médical
- Vasodilatateur artériel et veineux sélectif de la circulation pulmonaire
- Utilisé dans les cas de détresse respiratoire aiguë (hypertension artérielle pulmonaire)
💡 Pharmacologie avancée : Le NO endogène est synthétisé par les cellules endothéliales via les enzymes NO-synthases (NOS). C’est le mécanisme d’action des dérivés nitrés utilisés en cardiologie (trinitrine, isosorbide).
B. Le phosphore et ses dérivés
1. L’acide phosphorique H₃PO₄ (triacide)
Solutions inscrites à la Pharmacopée :
| Solution | Concentration | Usage |
|---|---|---|
| Solution officinale | 50 % | Fabrication de la solution diluée |
| Solution diluée | 10 % | Usage thérapeutique |
Indications de la solution diluée :
- Traitement du rachitisme
- Reconstituant général
- Acidifiant urinaire
2. Les hydrogénophosphates HPO₄²⁻
| Composé | Usage selon la dose |
|---|---|
| Hydrogénophosphate de sodium (Na₂HPO₄) | Faible dose : stimulant sécrétions gastriques ; Dose moyenne : modérateur ; Forte dose : purgatif ; Dissolvant de l’acide urique → traitement de la goutte |
| Hydrogénophosphate de calcium (CaHPO₄) | Recalcifiant et reconstituant |
3. Les phosphates PO₄³⁻
| Composé | Usage |
|---|---|
| Phosphate de calcium Ca₃(PO₄)₂ | Recalcifiant et reconstituant osseux |
| Phosphate d’aluminium AlPO₄ | Antiacide gastrique |
C. L’antimoine
Les sels d’antimoine sont utilisés dans le traitement de la leishmaniose (maladie parasitaire tropicale).
Exemple : l’antimoniate de méglumine (Glucantime®) — médicament de référence contre les leishmanioses viscérales et cutanées.
💊 Contexte épidémiologique : La leishmaniose affecte environ 1 million de personnes par an dans le monde, principalement dans les régions tropicales et subtropicales.
D. Le bismuth
Le bismuth est très toxique sous forme soluble → utilisé exclusivement sous forme de composés insolubles dans l’eau.
Propriétés :
- Antiacide
- Antiseptique
Applications :
| Domaine | Composé | Usage |
|---|---|---|
| Thérapeutique digestive | Sous-citrate de bismuth | Traitement de l’ulcère gastrique (H. pylori) |
| Cosmétologie | BiOCl ou BiO(NO₃) | Brillance nacrée dans les rouges à lèvres et vernis à ongles |
| Citrate de bismuth | — | Lotions de pigmentation des cheveux |
💡 À savoir : Le bismuth est également utilisé dans les préparations anti-diarrhéiques (ex. Pepto-Bismol dans les pays anglo-saxons) grâce à ses propriétés astringentes et antiseptiques.

Conclusion : Ce qu’il Faut Retenir
Les pnictogènes forment un groupe d’éléments chimiquement diversifiés, allant du non-métal gazeux (azote) au métal lourd (bismuth). En pharmacie, leur intérêt est multiple :
Points clés à mémoriser :
- L’azote et le phosphore sont essentiels à la vie (acides aminés, ADN, ATP, tissu osseux)
- L’ammoniac et l’acide nitrique ont des usages pharmaceutiques directs (liste 2)
- Les nitrites sont vasodilatateurs mais méthémoglobinisants — attention à la toxicité
- Le N₂O est un gaz anesthésique ; le NO est vasodilatateur pulmonaire sélectif
- Les phosphates sont recalcifiants, antiacides ou purgatifs selon leur nature
- L’antimoine traite la leishmaniose ; le bismuth soigne les troubles digestifs
Ressources complémentaires : Pharmacopée Européenne (11ème édition) | Cours de Biochimie — Métabolisme énergétique | Pharmacologie des médicaments cardiovasculaires



