Bioénergétique : Comprendre l’Énergie du Vivant
Introduction : Pourquoi les cellules ont-elles besoin d’énergie ?
Chaque cellule vivante — qu’il s’agisse d’un neurone, d’un entérocyte ou d’une cellule hépatique — est une usine chimique en fonctionnement permanent. Pour survivre, se diviser et accomplir ses fonctions spécifiques, tout organisme vivant doit effectuer trois grandes catégories de travail :
1. Le travail osmotique Il correspond au transport actif de molécules ou d’ions à travers une membrane biologique, contre un gradient de concentration. Par exemple, la pompe Na⁺/K⁺-ATPase maintient un gradient ionique indispensable à la conduction nerveuse — elle consomme à elle seule environ 20 à 40 % de l’ATP produit par une cellule animale.
2. Le travail mécanique Il regroupe toutes les formes de mouvement cellulaire : contraction musculaire (myosine/actine), transport vésiculaire, division cellulaire. La contraction du cœur, par exemple, repose entièrement sur une hydrolyse continue d’ATP par les ATPases musculaires.
3. Le travail chimique Il désigne la biosynthèse de molécules complexes indispensables à la vie : protéines, acides nucléiques, lipides membranaires, hormones, médiateurs chimiques, etc.
D’où vient l’énergie dans le monde du vivant ?
L’énergie nécessaire à ces travaux provient de deux grandes sources :
- Radiation solaire : captée par les organismes autotrophes (végétaux chlorophylliens) via la photosynthèse, elle est convertie en énergie chimique stockée dans les glucides, lipides et protéines.
- Énergie chimique des aliments : utilisée par les organismes hétérotrophes (dont l’être humain) qui dégradent ces composés organiques pour en extraire l’énergie.
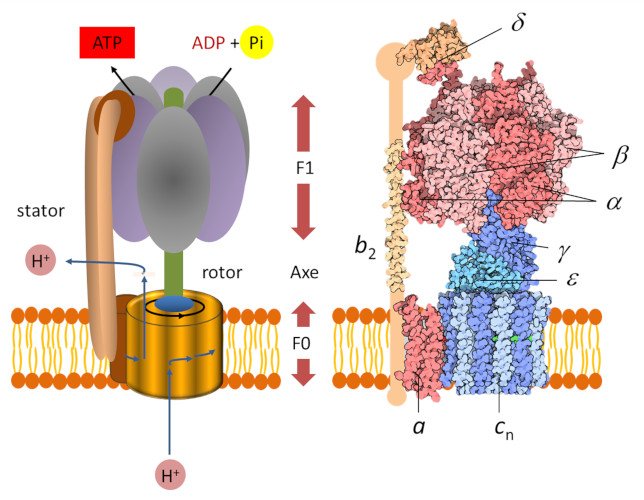
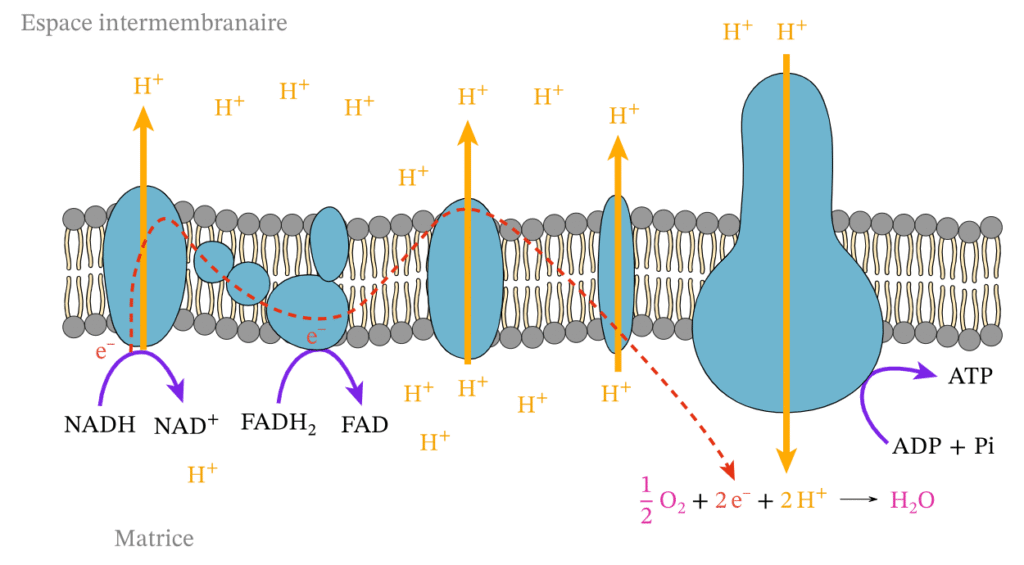
L’énergie chimique contenue dans les aliments est libérée par des oxydoréductions progressives au cours de la respiration cellulaire, par étapes successives contrôlées enzymatiquement. L’énergie ainsi dégagée est mise en réserve sous forme de composés phosphorylés riches en énergie, dont le principal est l’ATP (adénosine triphosphate).
Chez les organismes anaérobies, c’est au cours de la fermentation (sans O₂) que se produit la synthèse d’ATP. Ce mécanisme est cliniquement important : certaines bactéries pathogènes (Clostridium, Streptococcus) survivent et prolifèrent dans des conditions anaérobies.
I. Le Concept d’Énergie Libre
Les deux principes fondamentaux de la thermodynamique
Le transfert d’énergie dans les systèmes biologiques obéit aux lois de la thermodynamique. Ces lois s’appliquent à toute réaction chimique dans la cellule, qu’il s’agisse d’une phosphorylation, d’une réaction enzymatique ou d’un transport membranaire.
1er Principe — Conservation de l’énergie
L’énergie totale d’un système et de son environnement reste constante.
L’énergie ne se crée pas, elle se transforme. Dans la cellule, l’énergie chimique des nutriments se convertit en chaleur, en travail mécanique ou en énergie de liaison chimique (ATP), mais la somme totale reste invariable.
2ème Principe — Augmentation de l’entropie
Au cours de toute réaction chimique, l’entropie du système et de son environnement augmente jusqu’à atteindre l’équilibre.
À l’équilibre, l’entropie est à son maximum. Toute réaction spontanée va dans le sens d’une augmentation du désordre global.
Les trois grandeurs thermodynamiques essentielles
| Grandeur | Symbole | Définition |
|---|---|---|
| Entropie | S | Reflet du désordre moléculaire. Une réaction augmentant le désordre est favorisée. |
| Enthalpie | H | Énergie interne totale du système à pression constante. Mesurée par calorimétrie. |
| Énergie libre (de Gibbs) | G | Fraction de l’énergie utilisable pour fournir un travail. C’est la grandeur centrale en biochimie. |
La relation fondamentale de Gibbs
$\boxed{G = H – TS}
(où T est la température absolue en Kelvin)
Cette équation signifie que l’énergie libre disponible pour effectuer un travail dépend à la fois du contenu énergétique total (H) et de la part “perdue” en désordre (TS).
La variation d’énergie libre (ΔG) : critère de spontanéité
Pour une transformation de A vers B :
Δ G = GB – Gₐ = Δ H – T Δ S
Interprétation biochimique :
- Si ΔG < 0 (négatif) → La réaction est spontanée : elle libère de l’énergie libre. On parle de réaction exergonique. Exemple : l’hydrolyse de l’ATP.
- Si ΔG > 0 (positif) → La réaction nécessite un apport d’énergie : elle n’est pas spontanée. On parle de réaction endergonique. Exemple : la synthèse du glycogène à partir du glucose.
⚠️ Point clé pour l’examen : Le signe de ΔG indique la direction de la réaction dans les conditions réelles. Il ne préjuge pas de la vitesse de la réaction (qui dépend des enzymes et des énergies d’activation).
II. Relation entre ΔG et la Constante d’Équilibre
La formule centrale
Pour une réaction réversible A ⇌ B, la constante d’équilibre est :
Kₑq = [B][A]
La relation entre ΔG et les concentrations réelles est :
Δ G = Δ G° + RT × ln [B][A]
Définitions :
- ΔG° : variation d’énergie libre standard (conditions de référence : concentrations à 1 mol/L, pH = 7, T = 25 °C, P = 1 atm)
- R : constante des gaz parfaits (R = 1,987 cal/mol·K)
- T : température absolue (en Kelvin)
À l’équilibre (ΔG = 0)
Δ G° = -RT ln Kₑq
| Kₑq | ΔG° (cal/mol) | Signification |
|---|---|---|
| > 1 | Négatif | Réaction favorable (produits favorisés) |
| = 1 | 0 | Équilibre parfait |
| < 1 | Positif | Réaction défavorable (réactifs favorisés) |
💡 À retenir : C’est le signe de ΔG (et non de ΔG°) qui détermine si une réaction se produit spontanément dans les conditions cellulaires réelles. Les concentrations intracellulaires sont très différentes des concentrations standard.
III. Les Réactions Couplées : Le Moteur du Métabolisme
Principe du couplage énergétique
Les variations d’énergie libre sont additives. Ce principe fondamental permet à la cellule d’utiliser une réaction fortement exergonique pour “tirer” une réaction endergonique, via un intermédiaire commun.
C’est le mécanisme universel du métabolisme cellulaire : sans ce couplage, aucune biosynthèse ne serait possible.
Exemple classique : La phosphorylation du glucose en Glucose-6-Phosphate (G6P)
C’est la première réaction de la glycolyse, catalysée par l’hexokinase.
Réaction 1 — Endergonique (défavorable seule) : Glucose + Pᵢ → G6P + H₂O \quad Δ G° = +3,300 cal/mol
Réaction 2 — Exergonique (hydrolyse de l’ATP) : ATP + H₂O → ADP + Pᵢ \quad Δ G° = -7,300 cal/mol
Bilan du couplage : Glucose + ATP → G6P + ADP \quad Δ G° = -4,000 cal/mol$
Le bilan global est exergonique (ΔG° < 0) : la réaction est thermodynamiquement favorable grâce au couplage avec l’hydrolyse de l’ATP.
Application pharmaceutique : Ce mécanisme de couplage est la cible de nombreux médicaments. La metformine (antidiabétique) agit en inhibant partiellement le complexe I de la chaîne respiratoire, modifiant le rapport ATP/ADP et activant l’AMPK, un capteur énergétique cellulaire.
IV. Les Composés Riches en Énergie
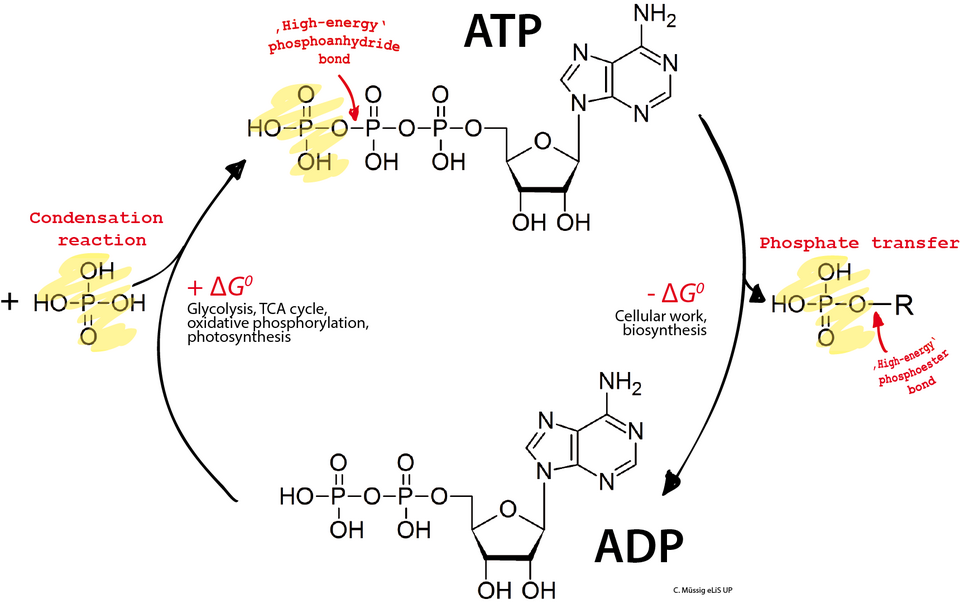
Notion de liaison phosphorique riche en énergie
L’énergie métabolique est principalement stockée et transférée via des liaisons phosphoanhydrides à haute énergie. Ces liaisons sont dites “riches en énergie” car leur hydrolyse libère une grande quantité d’énergie libre.
Hiérarchie des composés phosphorylés
La cellule maintient une hiérarchie précise de potentiel énergétique :
| Composé | ΔG° d’hydrolyse (cal/mol) | Localisation/Rôle |
|---|---|---|
| PEP (Phosphoénolpyruvate) | −14 800 | Glycolyse (étape finale) |
| 1,3-bisPG (1,3-bisphosphoglycérate) | −11 800 | Glycolyse |
| Phosphocréatine | −10 800 | Réserve rapide en muscle et cerveau |
| Carbamyl-phosphate | −10 100 | Cycle de l’urée |
| ATP → ADP + Pi | −7 300 | Monnaie universelle d’énergie |
| G1P (Glucose-1-Phosphate) | −5 000 | Glycogénolyse |
| G6P (Glucose-6-Phosphate) | −3 300 | Carrefour métabolique |
Le rôle pivot de l’ATP
L’ATP occupe une position intermédiaire dans cette hiérarchie — c’est précisément pour cette raison qu’il est la “monnaie énergétique universelle” de la cellule.
- Il est régénéré à partir de l’ADP grâce aux composés plus riches (PEP, 1,3-bisPG, phosphocréatine).
- Il cède son énergie à des composés moins énergétiques (G6P, G1P) pour les activer.
Ce système de transfert en cascade permet à la cellule de coupler efficacement les réactions cataboliques (productrices d’énergie) aux réactions anaboliques (consommatrices d’énergie).
Intérêt clinique — La phosphocréatine : Dans le muscle squelettique et le cerveau, la phosphocréatine constitue une réserve d’énergie immédiatement mobilisable. En cas d’effort intense, elle régénère l’ATP en quelques secondes, bien avant que la glycolyse ne prenne le relais. C’est pourquoi la créatinine (produit de dégradation de la créatine) est un marqueur de la masse musculaire et de la fonction rénale.
Résumé et Points Clés à Retenir
Tableau récapitulatif des concepts fondamentaux
| Concept | Définition | Application |
|---|---|---|
| ΔG < 0 | Réaction exergonique, spontanée | Hydrolyse de l’ATP, respiration |
| ΔG > 0 | Réaction endergonique, non spontanée | Biosynthèses, pompes ioniques |
| Couplage énergétique | ΔG additifs via intermédiaire commun | Toutes les réactions biosynthétiques |
| ATP | Intermédiaire universel de transfert d’énergie | Moteur de toute activité cellulaire |
Les 5 notions essentielles
- Toute forme de travail cellulaire (osmotique, mécanique, chimique) nécessite de l’énergie sous forme d’ATP.
- La spontanéité d’une réaction est déterminée par le signe de ΔG (et non ΔG°) dans les conditions cellulaires réelles.
- L’énergie libre de Gibbs (G) est la fraction d’énergie exploitable pour un travail biologique.
- Le couplage de réactions permet à la cellule de réaliser des synthèses thermodynamiquement défavorables grâce à l’énergie libérée par des réactions exergoniques.
- L’ATP est le pivot de tous les transferts énergétiques : sa position intermédiaire dans la hiérarchie des composés phosphorylés lui confère son rôle universel.
Pour Aller Plus Loin
Questions de révision
- Quelle est la différence entre ΔG et ΔG° ? Dans quel cas utilise-t-on l’un ou l’autre ?
- Comment expliquer que la phosphocréatine peut régénérer l’ATP, mais pas le G6P ?
- Citez deux exemples de réactions couplées impliquant l’ATP dans le métabolisme glucidique.
- Quelle est la signification biologique d’un ΔG° très négatif pour une réaction enzymatique ?
Mots-clés pour la recherche documentaire
bioénergétique | énergie libre de Gibbs | ATP | couplage énergétique | thermodynamique biochimique | phosphorylation oxydative | métabolisme énergétique



