Etude descriptive des oses d’intérêt biologique
Etude descriptive des oses d’intérêt biologique :
Monosaccharides :
Trioses :
Deux aldotrioes : D et l- glycéraldéhyde.
Un cétotriose : Dihydroxyacétone.
Existent sous forme d’esters phosphoriques, ce sont des éléments essentiels dans le métabolisme des glucides.
Tétroses :
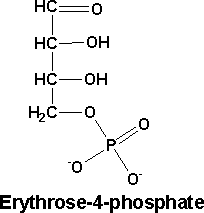
Erythroses : sous forme d’ester phosphorique (Erythrose 4 phosphate), c’est un intermédiaire de la voie des pentoses phosphate.
Pentoses :
Sont d’une grande importance biologique
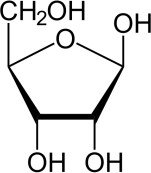
D-Ribose : Composant fondamental des nucléosides, nucléotides, ARN, et de nombreux coenzymes.
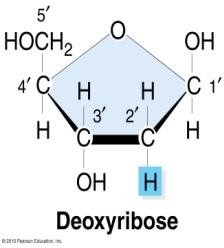
D-Désoxyribose : Composant fondamental de l’ADN.
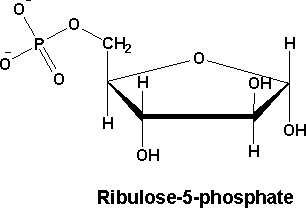
D-Ribulose : sous forme d’esters phosphorique, c’et un intermédiaire de la voie des pentoses phosphate.
Et de la photosynthèse.
L-Arabinose : très répandu dans la nature, non métabolisé par l’homme.
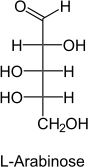
Après consommation de fruits riches en arabinose (cerises, prunes), on retrouve dans l’urine du L-arabinose pentosurie alimentaire à ne pas confondre avec un état pathologique.
Hexoses :
D-Glucose : très répandu dans la nature sous forme libre ou sous forme combinée, aussi bien dans le règne animal que végétal.
Son taux sanguin est constant (0.70 -1.10 g/l), il peut être mis en réserve dans les cellules animales sous forme de glycogène.
C’est le substrat énergétique de choix pour les cellules. [∝]20°𝐶 = + 52,2°.
𝐷
D-Galactose : constituant du lactose (sucre de lait), c’est le sucre le plus répandu après le glucose, sa dégradation rejoint la voie métabolique du glucose. [∝]20°𝐶 = 80°5.
𝐷
D-Mannose : constituant des glycoprotéines et polyosides [∝]20°𝐶 = +14,6°
𝐷
D-Fructose : très abondant dans les plantes et les fruits, miel ; chez l’homme on le retrouve surtout dans les sécrétions séminales où il sert d’aliment glucidiques aux spermatozoïdes. [∝]20°𝐶 = −93°.
𝐷
Heptoses :
Sedoheptulose : intermédiaire de la voie des pentoses phosphate.
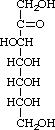
Osamines : résultent de la substitution d’un groupement OH par un groupement NH2. Exemple : D-glucosamine :
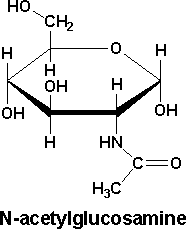
Les osamines sont rarement à l’état libre mais sous forme de N-acetylés :
Ex :N-acétyl glucosamine

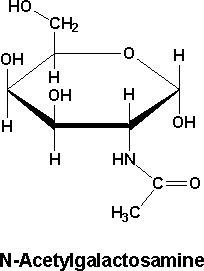
N-acétyl galactosamine
Acide N-acétyl muramique : résulte de l’association d’une molécule d’acide lactique avec une molécule de N-acétylglucosamine , retrouve au niveau des parois bactériennes
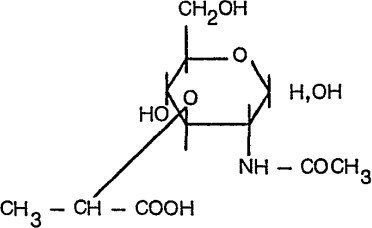
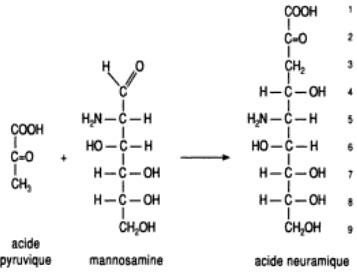
Ac Neuraminique : Ac sialique : cétose à 9 atomes de carbones
Résulte de la condensation de l’acide pyruvique avec D-mannosamine.
Il existe sous forme combinée (N-acétyl ; N-glycosyl ; O-acétyl ou O-glycosyl).
Les acides sialiques ont un très grand intérêt biologique.
Ils entrent dans la constitution des glycolipides, des glycoprotéines des membranes cellulaires.
Ils jouent un rôle fondamental dans la fixation de la pénétration des virus dans les cellules.
Le vibrion cholérique, le virus de la grippe et des orillons possèdent une enzyme spécifique : neuramidase ou sialidase.
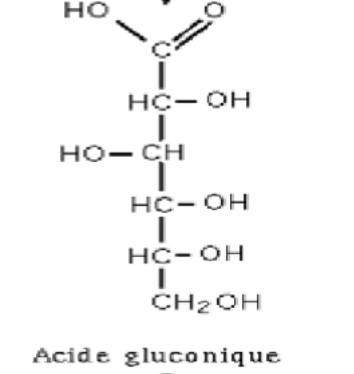
Les acides uroniques :
Obtenus par l’oxydation de la seule fonction OH primaire.
Ex : Ac D-glucuronique : joue un rôle dans la détoxification hépatique.
f.
Vitamine C (acide ascorbique) :
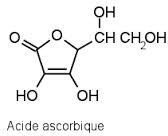
Présente dans les fruits et légumes frais, c’est un agent réducteur dans plusieurs réactions d’hydroxylation.
Les oligosides :
Ils résultent de la condensation de 2 à 10 résidus glucidiques reliés entre eux par une
liaison osidique.
La liaison osidique est très stable en milieu alcalin mais elle est facilement rompue par hydrolyse acide ou enzymatique.
Disaccharides (diholosides) :
Subdivisés en :
Disaccharides non réducteurs ;
Disaccharides réducteurs.
NB : un sucre est dit réducteur s’il est capable de réduire ou être oxydé par des oxydants doux Cu2+ ou Fe3+ ; le carbone du carbonyle est oxydé en acide carboxylique et le Cu2+ est réduit en Cu+.
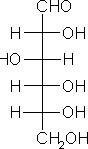
Glucose
Cette propriété est à la base de la réaction de Fehling : Formation de précipité rouge CuO2.
2 Cu2+
2 Cu+
L’extrémité réductrice d’un ose est celle qui contient un groupement carbonylique libre (OH sur le carbone anomère libre).
Un disaccharide est formé de deux monosaccharides unis par une liaison O-glycosidique, formée lorsqu’une fonction OH d’un sucre réagit avec le carbone anomérique d’un autre sucre.
Il y a donc formation d’un acétal à partir d’un hémiacétal et OH.
Un oligoside est dit réducteur lorsqu’il possède un OH aomèrique libre (non engagé dans un liaison osidique).
Disaccharides non réducteurs :
Saccharose : c’est le sucre de table, non réducteur, abondant chez les végétaux (bétrave).
[∝]20°C =+52°
D Glc
[∝]20°C =−93°
D 𝐅ruc
D Sach
⇒ [∝]20°C = +66° → Sucre interverti
Les enzymes qui dégradent le saccharose : invertase = mélange de glucosidase + fructosidase.
Utilisé pour son pouvoir sucrant.
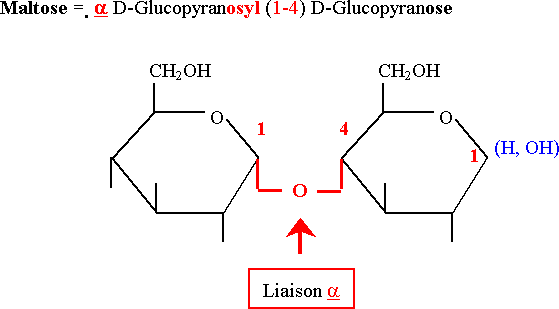
Tréhalose
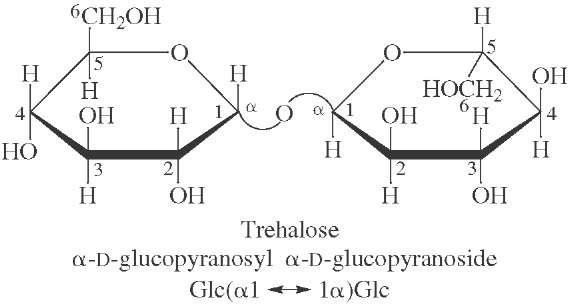
Diholosides réducteurs : a- Maltose :
Résulte de la dégradation de l’amidon par l’amylase.
Amidon
maltose + isomaltose
.
Isomaltose :
Deux résidus glucose unis par une liaison (16) glycosidique.
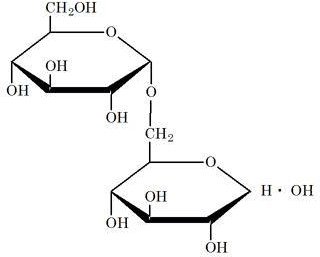
glucopyranosyl 16.
D. glucopyranose
Lactose
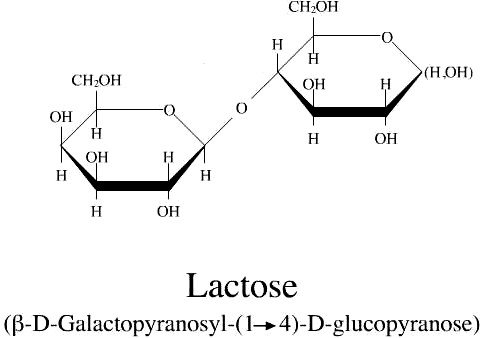
Sucre du lait : 45% des sucres du lait de vache, 70 % des sucres du lait de la femme.
Son hydrolyse par Galactosidase libère le galactose et glucose.
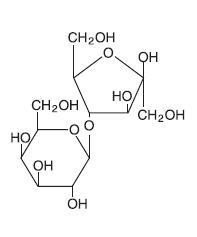
Lactulose :
Disaccharide de synthèse : Galactopyranosyl (1-4) fructofuranose.
Non dégradé par la flore intestinale ni absorbé, il s’accumule dans le colon, et sous l’effet de la flore bactérienne intestinale, il y aura formation d’acide lactique et d’acide acétique qui ont un pouvoir osmotique caractère laxatif.
Utilisé dans le traitement de la constipation.
Les Polyosides
Résultent de la condensation d’un grand nombre (>10) de résidus glucidique.
Les homopolysaccharides = un seul type d’unités monomériques.
Les hétéropolysaccharides = deux ou plusieurs types différents d’unités monomériques.
Homopolysaccharides : stockage de monosaccharides carburant, exemple : amidon, glycogène.
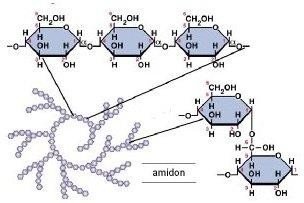
Amidon : forme de mise en réserve glucidique chez les végétaux.
Comporte deux types de polymères de glucose :
-Amylose 15-30 %: longue chaine non ramifiée d’unité D-Glucose liées par des liaisons (14).
-Amylopéctine 70-85% : unités de D-Glucose unis par des liaisons (14) linéaires ; ramifiée après chaque 24-30 résidus par des liaisons (16).
Glycogène :
Forme de stockage du glucose dans les cellules animales formé de sous unité glucose liés par des liaisons (14) ; ramifiée après chaque 8-12 résidus par des liaisons (16).
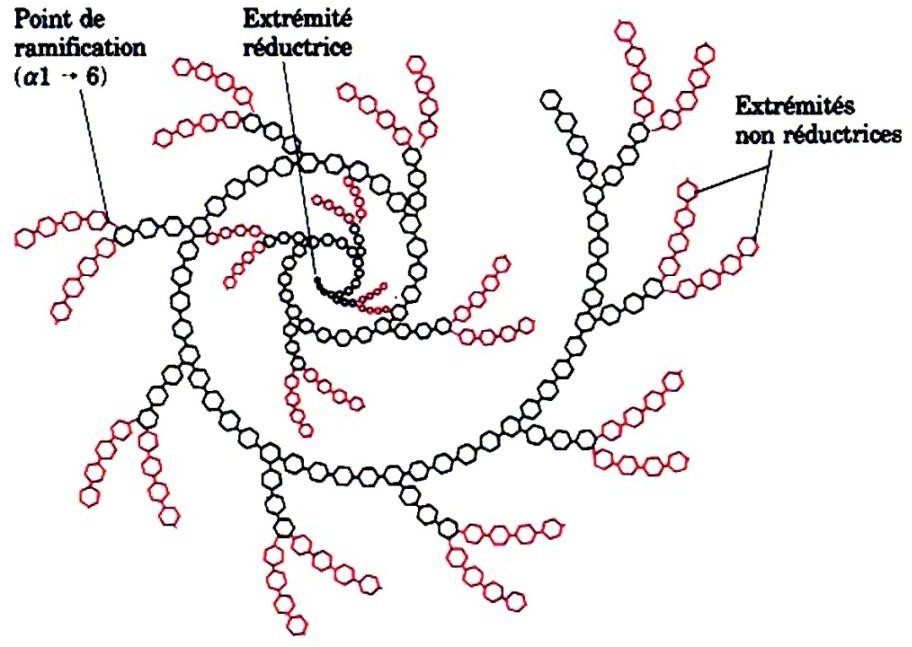
Structure arborescente plus compacte que l’amylopéctine.
Cellulose : les unités glucose sont liées par des liaisons (14) linéaires non ramifiées.
Hétéropolysaccharides : polyosides hétérogènes
GLYCOSAMINOGLYCANES : GAG (MPS) : résultent de la condensation d’un nombre élevé d’unité disaccharidiques répétitives.
L’un des deux monosaccharides est toujours soit N-acétyl-glucosamine ou N-actéyl- galactosamine, l’autre est l’acide uronique, généralement l’acide glucuronique, au moins un des oses constitutifs est porteur d’un groupement sulfate.
X : hexosamine sulfaté ou non Y : acide Hexuronique.

X
Y
Les groupements sulfate SO4 et acide COOH de l’acide hexuronique leurs confèrent une
grande acidité.
Ex :
L’acide Hyaluronique = [Acide D Glucuronique – N Ac-glucosamine]n
Composant du liquide synovial des articulations, consistance en gelée de l’humeur vitrée, responsable de la force, résistance et élasticité du cartilage et des tendons.
PROTEOGLYCANES :
Protéines qui contiennent une ou plusieurs chaines GAG liés par covalence, les liaisons entre GAG et protéines sont des liaisons O-glycosidiques entre les résidus glucidiques et le OH d’une sérine d’une protéine.
GLYCOPROTEINES
Certaines protéines sont liées par covalence (liaisons osidiques) à des chaines oligosaccharidiques
Ex glycoprotéines existant à la surface de la membrane érythrocytaire contiennent 60 % de glucides.
Mode de liaison : O-glycosidique ou N-glycosidique
Les sucres qu’on peut y trouver : Xylose, galactose, glucose, mannose, héxosamine = acide sialique en position terminale.
APPLICATION :
Détermination de la structure d’un polyoside ramifié :
Déterminer la nature des oses.
Déterminer le mode de liaison.
Déterminer la configuration anomérique.
NATURE DES OSES : après hydrolyse acide douce par HCl(d) des liaisons osidiques; on obtient soit :
Un seul type d’ose homogène Plusieurs types d’ose hétérogène
Les produits de l’hydrolyse sont séparés par CCM (chromatographie sur couche minces).
Résultat
Si le polyoside est homogène, on obtient une seule tache.
Si le polyoside est hétérogène, on obtient autant de taches que d’oses.
MODE DE LIAISON :
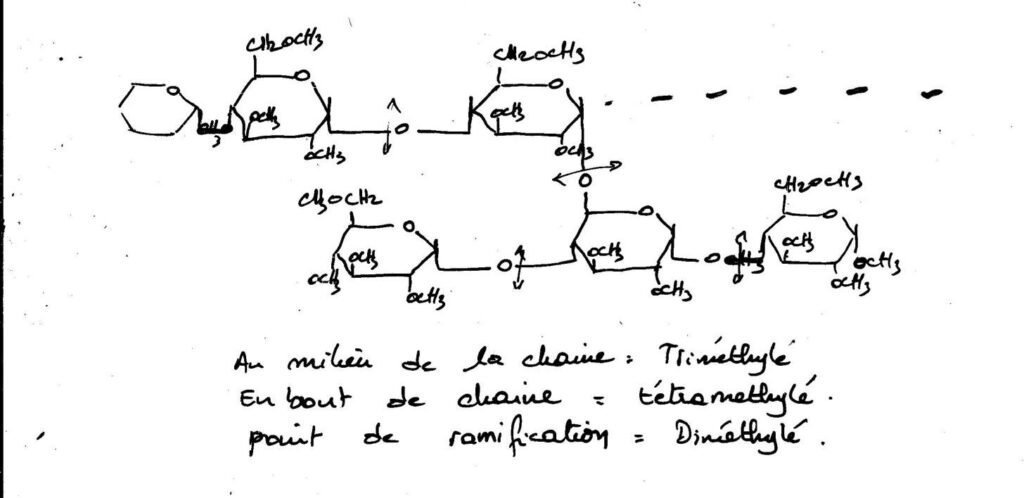
On réalise une perméthylation par SO4(CH3)2 de l’oligoside que l’on sommet ensuite à une hydrolyse acide, et on caractérise le nombre de composés tri ou tétra méthylés.
Après rupture de toutes les liaisons :
Au milieu de la chaine : triméthylé.
Au bout de la chaine : tétraméthylé.
Au point de ramification : diméthylé.
CONFIGURATION ANOMERIQUE : en utilisant des enzymes spécifiques et osidases.

