Chromatographie en Phase Supercritique (CPS) : Principe, Fonctionnement et Applications
Une technique analytique d’avenir au cœur de la chimie verte et de l’industrie pharmaceutique
Introduction : Qu’est-ce que la Chromatographie en Phase Supercritique ?
La chromatographie en phase supercritique (CPS), aussi désignée par l’acronyme anglais SFC (Supercritical Fluid Chromatography), est une technique de séparation analytique qui combine les avantages de la chromatographie en phase gazeuse (CPG) et de la chromatographie en phase liquide haute performance (CLHP/HPLC).
Son principe repose sur l’utilisation d’un fluide supercritique comme phase mobile — le plus souvent le dioxyde de carbone (CO₂) — qui se comporte simultanément comme un gaz et un liquide, offrant des propriétés de séparation exceptionnelles.
La SFC est particulièrement prisée pour les séparations chirales dans le développement et le contrôle qualité pharmaceutiques, réduisant la consommation de solvants organiques jusqu’à 90 % par rapport à la chromatographie liquide classique.
Le savoir-faire en chiffres : Le marché mondial de la CPS est estimé à 1,78 milliard USD en 2025, avec une croissance annuelle (CAGR) de 4,77 % prévue jusqu’en 2030.

I. Histoire et Origines de la CPS
1822 – La Découverte de l’État Supercritique
L’aventure scientifique commence en 1822 avec le Baron Cagniard de la Tour, qui observe la disparition de la frontière gaz-liquide de certaines substances chauffées dans un récipient fermé. Il décrit alors pour la première fois le point critique, seuil au-delà duquel apparaît un état intermédiaire inédit : l’état supercritique.
1879 – Le Pouvoir Solvant Révélé
En 1879, Hannay et Hogarth mettent en évidence le pouvoir solvant remarquable des fluides supercritiques. Leurs expériences montrent une solubilité élevée de l’iodure de potassium dans l’éthanol supercritique (Tc = 243 °C, Pc = 63 atm), suivie d’une précipitation soudaine lors de la réduction de pression.
1962 à aujourd’hui – L’Essor de la Technique
- 1962 : Klesper, Corwin et Turner réalisent les premières séparations chromatographiques en phase supercritique, appliquées aux porphyrines non volatiles.
- Années 1970 : Le développement fulgurant de la CLHP éclipse temporairement la CPS.
- 1982 : Regain d’intérêt mondial pour la technique.
- 1988 : Parution du premier ouvrage de référence dédié à la CPS.
- Aujourd’hui : L’intégration de la CPS avec la spectrométrie de masse et l’automatisation intelligente propulsent cette technique au cœur des laboratoires analytiques modernes.
II. L’État Supercritique : Comprendre les Fondamentaux
Qu’est-ce qu’un Fluide Supercritique ?
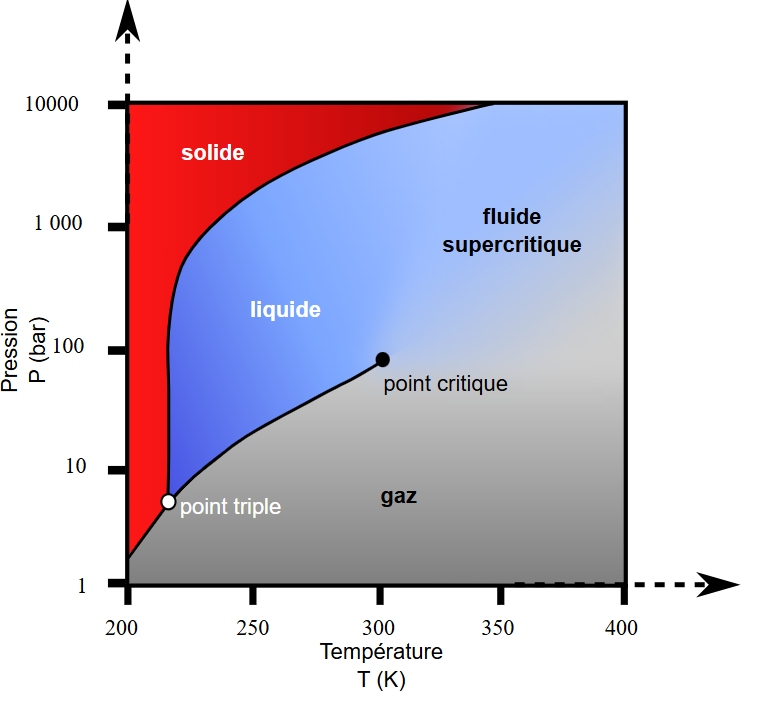
Un fluide est dit supercritique lorsqu’il est soumis simultanément à une température et une pression supérieures à ses valeurs critiques (Tc et Pc). À cet état, le fluide n’est ni un gaz ni un liquide : il présente des propriétés hybrides particulièrement utiles en chromatographie.
Les Propriétés Physico-chimiques Clés
Masse volumique (ρ) :
- Augmente avec la pression à température constante
- Diminue avec la température à pression constante
- Directement liée au pouvoir solvant du fluide → facilement contrôlable
Viscosité :
- Plus faible que celle d’un liquide
- Augmente avec la pression, mais reste proche de la viscosité gazeuse
- Permet des débits élevés avec des chutes de pression réduites
Coefficient de diffusion :
- Nettement supérieur à celui des liquides
- Diminue avec la viscosité, augmente avec la masse molaire et la masse volumique
- Favorise des transferts de masse rapides → séparations plus efficaces
Polarité :
- Augmente avec la masse volumique
- Partiellement contrôlable via des modificateurs organiques
Ces propriétés font des fluides supercritiques des solvants “à géométrie variable” : excellents solvants dans les conditions supercritiques, très mauvais à l’état de gaz comprimés.
III. Principe de la CPS
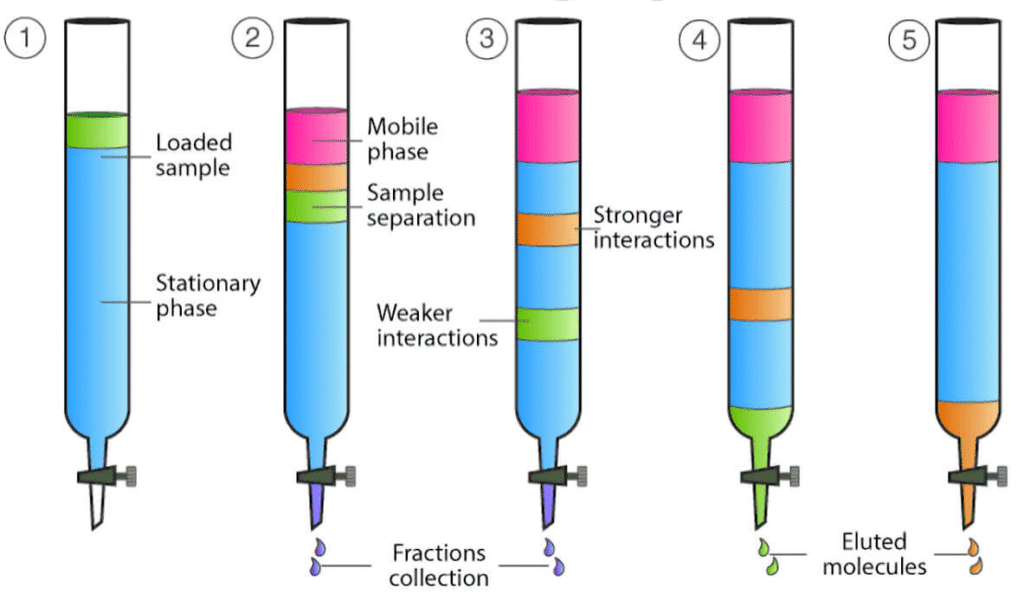
La CPS est une méthode de séparation chromatographique dans laquelle la phase mobile est un fluide porté au-delà de son point critique. La migration des solutés résulte d’un mécanisme de partage entre :
- Une phase stationnaire généralement apolaire (ou chirale)
- Une phase mobile éluante peu polaire (souvent CO₂ supercritique + modificateur)
Le soluté migre selon son affinité relative pour chacune des deux phases. En faisant varier la pression, la température ou la composition du fluide, on peut moduler finement la sélectivité de la séparation en temps réel.
IV. La Phase Mobile en CPS
Critères de Sélection
Une phase mobile adaptée à la CPS doit répondre aux exigences suivantes :
- Faible toxicité et non-inflammabilité
- Pression et température critiques accessibles
- Bonne solubilité des analytes
- Non-corrosif et compatible avec les détecteurs
- Faible coût (grandes quantités utilisées)
1 – Le CO₂ Supercritique : Le Fluide de Référence
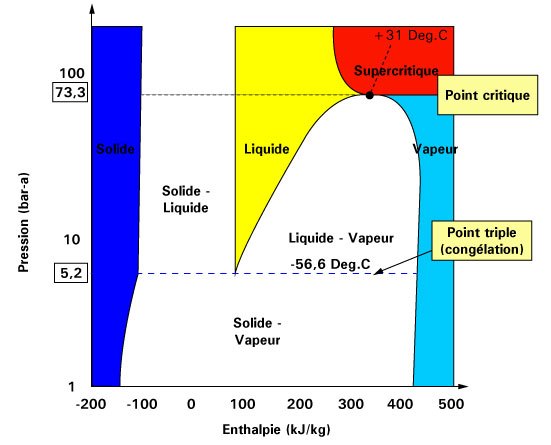
Le dioxyde de carbone (CO₂) est de loin le fluide supercritique le plus utilisé en CPS (Tc = 31,1 °C ; Pc = 73,8 bar). Ses atouts sont nombreux :
- ✅ Non toxique et inodore
- ✅ Non inflammable
- ✅ Chimiquement inerte (pas d’oxydation du produit)
- ✅ Basse température critique → compatible avec les produits thermosensibles
- ✅ Pas de solvant résiduel après traitement (évacuation à pression atmosphérique)
- ✅ Économique et disponible en grande quantité
Limite principale : Le CO₂ supercritique pur ne solubilise efficacement que les composés apolaires et de faible poids moléculaire.
2 – Les Modificateurs Organiques (Co-solvants)
Pour élargir le champ d’application aux molécules polaires, on ajoute au CO₂ un co-solvant protique (méthanol, éthanol, isopropanol). En jouant sur le ratio CO₂/co-solvant, on ajuste la polarité de la phase mobile.
Exemple du méthanol (MeOH) :
- Augmente la polarité de la phase mobile
- Améliore la solubilité du soluté
- Réduit le temps de rétention
- Contrôle la sélectivité de séparation
- ⚠️ Incompatible avec le détecteur à ionisation de flamme (FID)
3 – Gradients d’Élution
La rétention peut être modulée dynamiquement en cours de séparation par :
- Modification de la pression (→ masse volumique)
- Modification de la température
- Variation de la teneur en modificateur polaire
Ces paramètres sont programmés informatiquement, permettant des gradients d’élution complexes et reproductibles.
4 – Les Additifs
Pour les analytes ionisables (protolytes forts, ampholytes), un mélange binaire CO₂/co-solvant peut s’avérer insuffisant. Des additifs (acide formique, ammoniaque, triéthylamine) sont alors incorporés pour supprimer l’ionisation de l’analyte et améliorer la forme des pics chromatographiques.
V. La Phase Stationnaire
La phase stationnaire en CPS doit impérativement être stable dans les conditions supercritiques (haute pression, température élevée). Elle est généralement de nature polymérique.
Exemples de phases stationnaires utilisées :
- Silica-Divinylbenzène (stable jusqu’à 150 °C)
- Zircanion
- Cellulose et amylose (pour les séparations chirales)
- Phases greffées de type C18, diol, cyanopropyle
On retrouve en CPS les mêmes géométries de colonnes qu’en CLHP (colonnes remplies) et qu’en CPG (colonnes capillaires à phase greffée), y compris la grande majorité des phases chirales.
VI. Appareillage de la CPS
Ressemblances avec la CLHP
Les instruments de CPS sont structurellement proches de ceux de la CLHP. Les composants principaux sont :
- Une pompe à piston → assure le débit du fluide supercritique
- Un serpentin chauffant → élève la température au-delà du point critique
- Un injecteur automatique
- La colonne chromatographique
- Le détecteur
- Une vanne de régulation de pression (ou un restricteur pour colonnes capillaires)
Détecteurs Compatibles
- Détecteur UV ou par fluorescence (comme en CLHP)
- Détecteur à ionisation de flamme (FID) — spécificité importante de la CPS par rapport à la CLHP (uniquement sans modificateur organique)
- Spectrométrie de masse (SFC-MS) → l’association SFC-MS est en plein essor pour l’identification exhaustive de composés dans des matrices complexes.
Colonnes Remplies vs Colonnes Capillaires
| Critère | Colonnes remplies | Colonnes capillaires |
|---|---|---|
| Efficacité | Bonne | Très haute |
| Débit | Plus élevé | Plus faible |
| Utilisation des modificateurs | Oui | Non recommandé |
| Compatibilité FID | Non (avec modificateur) | Oui |
| Application | Analytique & préparatif | Analytique |
VII. Avantages de la CPS par rapport à la CLHP et à la CPG
L’un des principaux avantages de la CPS préparative est la réduction de la consommation de solvants organiques pouvant atteindre 90 % par rapport à la chromatographie liquide. C’est un argument décisif dans un contexte de chimie verte et de réduction de l’empreinte environnementale des laboratoires.
Les autres avantages majeurs sont :
- Efficacité accrue : longueur de colonne augmentable grâce à la faible viscosité de la phase mobile
- Séparations chirales performantes : la CPS est devenue la méthode de référence pour les énantiomères en industrie pharmaceutique
- Vitesse : les cinétiques de sorption-désorption sont plus rapides qu’en CLHP → analyses plus rapides
- Récupération facile des solutés en CPS préparative : simple détente de la phase mobile pour éliminer le solvant
- Sélectivités modulables : jouant sur la pression, la température et les modificateurs, on optimise la séparation sans changer de colonne
VIII. Applications de la CPS

Le domaine d’application privilégié de la CPS concerne les solutés de haute masse moléculaire (MM > 1 000 Da) ou thermolabiles ne contenant pas de groupe chromophore.
Industrie Pharmaceutique
- Séparation et purification d’énantiomères (molécules chirales)
- Contrôle qualité des principes actifs (API)
- Profilage des impuretés
- Criblage à haut débit en découverte de médicaments
Exemple concret : L’ibuprofène, l’amphotéricine B, de nombreux antibiotiques et antiviraux font l’objet de séparations chirales en CPS lors de leur développement industriel.
Alimentation et Produits Naturels
- Analyse des acides gras et lipides
- Dosage des sucres
- Séparation de caroténoïdes, tocophérols et antioxydants naturels
- Contrôle des arômes et fragrances
Environnement et Pétrochimie
- Analyse des hydrocarbures polycycliques aromatiques (HAP)
- Dosage des pesticides dans les matrices environnementales
- Caractérisation des polymères et de leurs additifs
Autres Domaines
- Analyse d’isomères difficiles à distinguer par CLHP
- Polymères et matériaux de haute masse moléculaire
- Les systèmes SFC portables permettent désormais des analyses in situ pour la sécurité alimentaire et le contrôle environnemental sur le terrain.
IX. CPS et Chimie Verte : Un Enjeu d’Avenir

Dans un contexte de fort accent sur la chimie verte, la réduction de l’utilisation de solvants organiques en CPS constitue un argument de vente majeur, en particulier dans les régions soumises à des réglementations environnementales strictes.
En substituant l’HPLC par la CPS là où cela est possible, un laboratoire peut :
- Diminuer drastiquement ses achats de solvants organiques
- Réduire ses déchets chimiques et les coûts d’élimination associés
- Accélérer ses analyses et augmenter sa productivité
- Améliorer la sécurité des opérateurs (moins d’exposition aux vapeurs organiques)
Shimadzu a lancé en 2025 une plateforme de traitement de données chromatographiques pilotée par intelligence artificielle, illustrant la convergence entre CPS et technologies numériques avancées.
X. Conclusion : La CPS, Technique Complémentaire Incontournable
La chromatographie en phase supercritique s’est imposée comme un outil analytique complémentaire et souvent supérieur à la CLHP et à la CPG pour de nombreuses applications. Grâce à la modulation de la pression, de la température et de la composition en modificateurs, la CPS offre une flexibilité analytique unique, des séparations rapides et efficaces, et une empreinte environnementale réduite.
Points clés à retenir :
- Le CO₂ supercritique est la phase mobile de référence : non toxique, inerte et économique
- La CPS excelle dans les séparations chirales et les composés de haute masse moléculaire
- Elle réduit la consommation de solvants jusqu’à 90 % par rapport à la CLHP
- Son marché mondial est en forte croissance, porté par l’industrie pharmaceutique et la chimie verte
- L’intégration avec la spectrométrie de masse ouvre de nouvelles perspectives analytiques



