Les Halogènes en Chimie Pharmaceutique : Guide Complet pour Étudiants en Pharmacie
Résumé : Les halogènes (Fluor, Chlore, Brome, Iode) sont parmi les éléments les plus utilisés en chimie médicinale. Plus d’un tiers des médicaments mis sur le marché contiennent au moins un atome de fluor, et 85 % des produits pharmaceutiques fabriqués dans le monde utilisent le chlore dans leurs schémas de synthèse. Comprendre leurs propriétés physico-chimiques est essentiel pour tout futur pharmacien.

I. Généralités : Qu’est-ce qu’un Halogène ?
Le terme “halogène” vient du grec hals (sel) et -gen- (engendrer) : ce sont littéralement les “générateurs de sel”. Ce nom reflète parfaitement leur tendance naturelle à former des sels en réagissant avec les métaux.
Sur le plan électronique, tous les halogènes partagent une configuration de valence commune : (ns)²(np)⁵, soit 7 électrons de valence. Il leur manque donc un seul électron pour atteindre la configuration de l’octet, ce qui explique leur réactivité chimique intense et leur fort pouvoir oxydant.
Les 6 éléments du Groupe 17
La famille des halogènes comprend les 6 éléments du groupe 17 (colonne VIIA) :
| n | Élément | Z | Configuration électronique | Étymologie et découverte |
|---|---|---|---|---|
| 2 | Fluor F | 9 | [He]2s²2p⁵ | De fluorite (CaF₂) ; Moissan, 1886 |
| 3 | Chlore Cl | 17 | [Ne]3s²3p⁵ | Du grec khlôros = jaune vert ; H. Davy, 1810 |
| 4 | Brome Br | 35 | [Ar]4s²3d¹⁰4p⁵ | Du latin bromus = nauséabond ; Balard, 1826 |
| 5 | Iode I | 53 | [Kr]5s²4d¹⁰5p⁵ | Du grec iôèïdes = violet ; Courtois, 1811 |
| 6 | Astate At | 85 | [Xe]6s²4f¹⁴5d¹⁰6p⁵ | Du grec astatos = instable ; Corson et al., 1940 |
| 7 | Tennessine Ts | 117 | [Rn]7s²5f¹⁴6d¹⁰7p⁵ | Synthétisé en 2014 ; Düllmann et al. |
💡 Point clé pour l’examen : L’astate est entièrement radioactif et sans importance pratique en pharmacie. Le tennessine, synthétisé artificiellement, se comporte davantage comme un métalloïde en raison des effets relativistes de son noyau très chargé.
II. État Naturel et Sources des Halogènes
Les halogènes sont tous des non-métaux (à l’exception de l’iode et de l’astate qui présentent quelques propriétés quasi métalliques). En raison de leur forte réactivité, ils n’existent pas à l’état libre dans la nature : on les retrouve sous forme d’ions halogénures X⁻ dans divers minerais et dans l’eau de mer.
Principales sources naturelles
Fluor : Les composés naturels les plus courants sont :
- La fluorite (CaF₂)
- La cryolite (Na₃AlF₆)
- La fluorapatite (Ca₅(PO₄)₃F)
Chlore : On le retrouve sous forme d’halogénures dans l’eau de mer et les dépôts salins. Il est aussi présent dans le suc gastrique (HCl, pH = 1 à 2) où il joue un rôle physiologique essentiel.
Brome : Extrait de saumures souterraines (Arkansas : 3 800–5 000 ppm ; mer Morte : 4 500–5 000 ppm).
Iode : Présent dans l’eau de mer, les animaux marins et concentré dans les algues marines. C’est le seul halogène pouvant exister à l’état naturel avec un degré d’oxydation positif.
III. Propriétés Physico-Chimiques
1. Les Molécules Dihalogènes X₂
À l’état pur, les halogènes forment des molécules diatomiques (X₂). Dans leur état standard (298 K, 1 bar), on observe :
| Élément | État physique à 25°C | Couleur | Odeur |
|---|---|---|---|
| F₂ | Gaz | Jaune pâle | Suffocante, très corrosive |
| Cl₂ | Gaz | Jaune-vert | Suffocante |
| Br₂ | Liquide | Rouge foncé | Suffocante, nauséabonde |
| I₂ | Solide | Gris violacé (éclat métallique) | Légèrement volatil |
Les températures de changement d’état augmentent régulièrement en descendant dans la colonne, car seules les interactions de van der Waals sont possibles entre molécules de X₂ (pas de liaison hydrogène, pas de dipôle permanent).
💡 Astuce mnémotechnique : “Gaz-Gaz-Liquide-Solide” → F₂, Cl₂, Br₂, I₂ à température ambiante.
2. Préparation des Dihalogènes
Difluor F₂ : Henri Moissan réussit en 1886 la première préparation du fluor par électrolyse de HF dissous dans du fluorure de potassium fondu :
2H⁺ + 2F⁻ → H₂(g) + F₂(g)
Dichlore Cl₂ : Carl Wilhelm Scheele prépara le chlore en 1774. Aujourd’hui, la méthode industrielle repose sur l’électrolyse d’une solution aqueuse de NaCl. En laboratoire, on utilise la réaction :
MnO₂(s) + 4HCl(aq) → MnCl₂(aq) + 2H₂O(l) + Cl₂(g)
Le procédé Deacon (méthode industrielle historique) utilise l’oxydation de HCl par O₂ à 400°C avec CuCl₂ comme catalyseur.
Dibrome Br₂ : Extrait des saumures souterraines par traitement au Cl₂(g), qui oxyde les ions Br⁻ en Br₂ :
Cl₂(g) + 2Br⁻(aq) → 2Cl⁻(aq) + Br₂(l)
Diiode I₂ : Obtenu par réduction des ions iodate IO₃⁻ avec l’hydrogénosulfite de sodium :
2IO₃⁻(aq) + 5HSO₃⁻(aq) → I₂(aq) + 5SO₄²⁻(aq) + 3H⁺(aq) + H₂O(l)
IV. Propriétés Chimiques Générales
1. Pouvoir Oxydant des Halogènes
Les halogènes sont tous des oxydants puissants grâce à leur forte affinité électronique. Ce pouvoir oxydant diminue régulièrement de F₂ à I₂ :
F₂ > Cl₂ > Br₂ > I₂
Ce pouvoir se traduit par les réactions de déplacement successif des halogénures :
F₂ + 2X⁻ → 2F⁻ + X₂ (X = Cl, Br ou I)
Cl₂ + 2X⁻ → 2Cl⁻ + X₂ (X = Br ou I)
Br₂ + 2I⁻ → 2Br⁻ + I₂
⚠️ Important : I₂ ne peut déplacer aucun autre halogène car c’est l’oxydant le plus faible du groupe.
2. Les Halogénures d’Hydrogène HX
En solution aqueuse, les halogénures d’hydrogène sont des acides, la plupart forts, à l’exception de HF qui est un acide faible. Cette exception s’explique par :
- La force de la liaison H–F (très élevée)
- Les liaisons hydrogène entre F⁻ et HF en solution
La préparation directe à partir des éléments :
| Réaction | Conditions | Remarque |
|---|---|---|
| H₂ + F₂ → 2HF | Température ordinaire | Très violente |
| H₂ + Cl₂ → 2HCl | Lumière ou 400°C | Violente en présence de lumière |
| H₂ + Br₂ → 2HBr | 400°C + catalyseur | Plus lente |
| H₂ + I₂ → 2HI | 500°C + catalyseur | Encore plus lente, réversible |
HF est un liquide incolore qui bout à 19,5°C (à cause des liaisons hydrogène). Tous les autres halogénures d’hydrogène sont des gaz incolores à température ambiante.
On peut aussi préparer les halogénures d’hydrogène en chauffant un sel halogéné avec H₂SO₄ concentré :
CaF₂(s) + H₂SO₄(conc) → CaSO₄(s) + 2HF(g)
2NaCl(s) + H₂SO₄(conc) → Na₂SO₄(s) + 2HCl(g)
3. Les Oxacides et Oxanions des Halogènes
Le fluor, étant le plus électronégatif de tous les éléments, a toujours un degré d’oxydation de –1. Les autres halogènes peuvent prendre des valeurs positives : +1, +3, +5, +7.
| Degré d’oxydation | Chlore | Brome | Iode |
|---|---|---|---|
| +1 | HOCl (acide hypochloreux) | HOBr | HOI |
| +3 | HOClO | — | — |
| +5 | HOClO₂ | HOBrO₂ | HOIO₂ |
| +7 | HOClO₃ | HOBrO₃ | HOIO₃ |
⚠️ Dans ces oxacides, les atomes d’hydrogène sont liés à l’oxygène, non à l’halogène. Les formules condensées HOCl, HClO₂, etc., sont souvent utilisées par convention.
L’acide hypochloreux HOCl se forme par dismutation du chlore dans l’eau :
Cl₂(g) + H₂O(l) → HOCl(aq) + H⁺(aq) + Cl⁻(aq)
C’est un antiseptique efficace, largement utilisé pour la désinfection de l’eau.
4. Réactivité avec les Autres Éléments
Avec l’oxygène : Le fluor est plus électronégatif que l’oxygène et forme des composés particuliers où l’oxygène est au degré d’oxydation +II (ex : OF₂). Ces composés sont surtout des curiosités chimiques utilisées en recherche pour synthétiser des molécules riches en énergie (carburants pour fusée).
Entre halogènes : Les halogènes peuvent se combiner entre eux pour former des composés interhalogènes :
F₂ + Cl₂ → 2ClF (à 100°C)
I₂ + Cl₂ → 2ICl (à 100°C)
V. Usages Industriels

Fluor — Applications Industrielles
- Raffinage du pétrole et fabrication de polymères fluorocarbonés comme le Téflon (PTFE) et les Fréons (agents frigorifiques)
- Gravure du verre : l’acide fluorhydrique (HF) réagit avec la silice pour graver ou “givrer” les verres (ampoules lumineuses, verres décoratifs)
Chlore — Applications Industrielles
- Agent de blanchiment de la pâte à papier
- Germicide pour la purification de l’eau potable
- Synthèse d’insecticides et herbicides
- Fabrication du PVC (polychlorure de vinyle) : tuyaux, tubes isolants, revêtements protecteurs
Brome — Applications Industrielles
- Production du dibromoéthane (BrCH₂CH₂Br) : additif anti-plomb dans les essences
- Émulsions de bromure d’argent pour les films photographiques noir et blanc
- Désinfection de l’eau de piscine
Iode — Applications Industrielles
- Purification de métaux tels que Ti, Zr et Hf
- Catalyseur pour la production de caoutchouc synthétique
- Fabrication de colorants, teintures et pigments
VI. Usages Thérapeutiques — Données Essentielles en Pharmacie

Le Fluor en Thérapeutique
Chiffre clé : Environ 20 à 30 % des médicaments modernes contiennent au moins un atome de fluor, et plus du tiers des nouvelles molécules actives mises sur le marché en comportent un.
L’insertion d’un atome de fluor dans une molécule modifie profondément sa réactivité, sa biodisponibilité, sa liposolubilité et sa résistance à la dégradation enzymatique. Ces propriétés en font un outil précieux en chimie médicinale.
Prophylaxie dentaire : Le fluor renforce l’émail dentaire en formant une couche résistante aux attaques acides bactériennes. L’OMS recommande un apport de 0,05 mg de fluor par kg de poids corporel par jour. Les dentifrices doivent contenir entre 1 000 et 1 500 ppm de fluorure pour être efficaces.
⚠️ Risque de fluorose (jaunissement des dents) en cas d’apport excessif — la supplémentation doit toujours faire l’objet d’un bilan fluoré personnalisé.
Médicaments contenant du fluor :
| Classe thérapeutique | Exemple(s) | Rôle du fluor |
|---|---|---|
| Corticostéroïdes | 9-fluoro-dihydrocortisone | 11× plus actif, sans rétention d’eau |
| Antiviraux | Trifluridine (herpès) | Stabilité métabolique |
| Antibiotiques | Fluoroquinolones (ciprofloxacine) | Pénétration cellulaire améliorée |
| Antifongiques | Fluconazole | Biodisponibilité orale élevée |
| Anesthésiques | Séoflurane, Desflurane, Isoflurane | Volatilité, non-inflammabilité, stabilité |
| Anti-inflammatoires | Flurbiprofène | Lipophilie accrue |
| Médicaments du SNC | Fluoxétine (Prozac) | Passage de la BHE facilité |
💡 Mécanisme clé : Le fluor augmente la lipophilie d’une molécule, favorisant ainsi son passage à travers la barrière hémato-encéphalique (BHE) — essentiel pour les médicaments ciblant le système nerveux central.
Le Chlore en Thérapeutique
Chiffre clé : 85 % des produits pharmaceutiques fabriqués dans le monde utilisent le Cl₂ dans leurs schémas de synthèse ou contiennent l’élément chlore.
Rôle physiologique de HCl : L’HCl est sécrété par les cellules pariétales de l’estomac (pH = 1 à 2), à raison d’1 à 2 litres par jour. Ses fonctions sont :
- Conversion du pepsinogène en pepsine (digestion des protéines)
- Hydrolyse des glucides complexes (saccharose → glucose + fructose)
- Asepsie du bol alimentaire (destruction des bactéries, virus, levures, champignons)
Médicaments à base de chlore :
| Médicament | Classe | Indication principale |
|---|---|---|
| Clopidogrel | Antiagrégant plaquettaire | Prévention des thromboses |
| Amlodipine | Antagoniste calcique (type L) | Hypertension, angine de poitrine |
| Diclofénac | AINS | Anti-inflammatoire, antalgique |
| Halopéridol | Neuroleptique | Psychoses aiguës, schizophrénie, manie |
| Solution de Dakin | Antiseptique (NaClO) | Lavage de plaies et muqueuses |
| Metformine HCl | Antidiabétique oral | Diabète de type 2 |
| Cétirizine HCl | Antihistaminique | Allergies |
| Adrénaline HCl | Sympathomimétique | Choc anaphylactique, bronchodilatation |
Le Brome en Thérapeutique
Les substances bromées sont des ingrédients importants dans de nombreux médicaments, notamment des analgésiques, sédatifs et antihistaminiques.
Médicaments à base de brome :
- Bromure de K, Na, ou Ca : sédatifs nerveux
- Bromure de pinaverium (Dicétel) : spasmolytique sélectif du tube digestif, antagoniste calcique au niveau de la cellule musculaire lisse intestinale
- Bromo-galactogluconate de calcium (Calcibronate) : sédatif nerveux
L’Iode en Thérapeutique
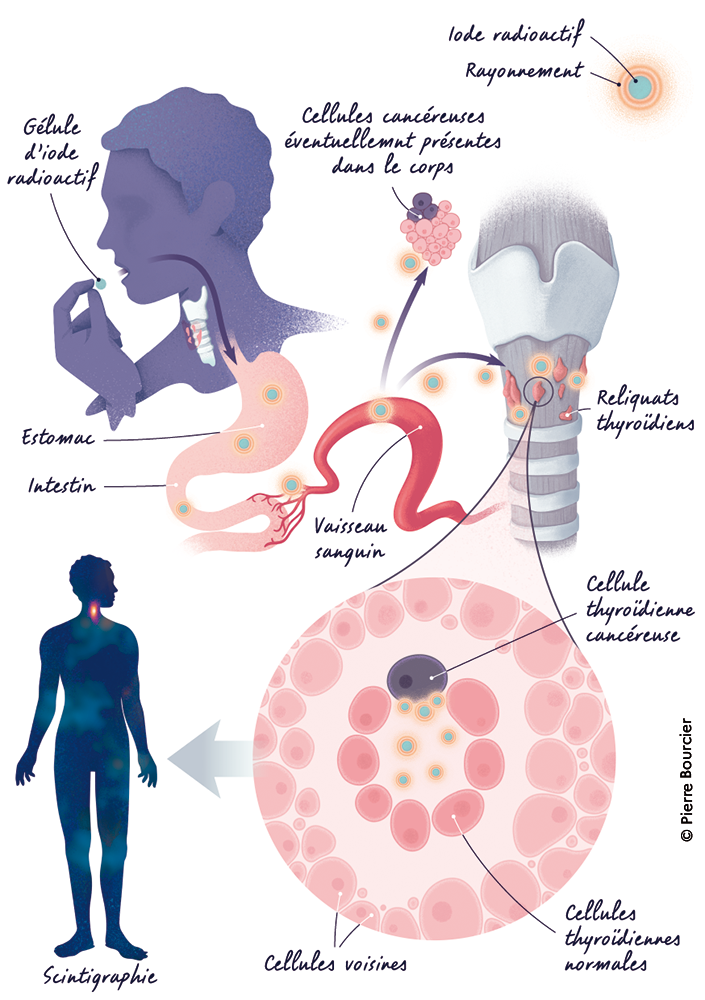
L’iode est un oligoélément indispensable à la vie humaine, notamment en raison de son rôle dans la synthèse des hormones thyroïdiennes :
- Thyroxine (T4) : 4 atomes d’iode par molécule
- Triiodothyronine (T3) : 3 atomes d’iode par molécule
Ces hormones régulent pratiquement tous les métabolismes de base : synthèse des protéines, croissance des os longs, développement neuronal, etc.
⚠️ Carence en iode : À l’origine de goitres, retards de croissance et troubles mentaux, dont le crétinisme. C’est pourquoi du sel iodé est distribué à titre préventif dans de nombreux pays.
Applications médicales de l’iode :
| Application | Principe |
|---|---|
| Agent de contraste (imagerie médicale) | Forte opacité aux rayons X → opacification des organes (reins, artères, cerveau…) |
| KI comme expectorant | Traitement de la congestion pulmonaire |
| KI contre la sporotrichose | Infection fongique |
| KI en cas de contamination radioactive | Saturation de la thyroïde en iode stable pour bloquer l’iode radioactif |
| Lugol (microbiologie) | Coloration de Gram ; différenciation bactérienne |
| Lugol (botanique) | Mise en évidence des granules d’amidon (coloration bleu intense) |
| Pacemakers (lithium-iode) | Fabrication de puces électroniques |
Médicaments à base d’iode :
| Médicament | Indication |
|---|---|
| Bétadine Dermique | Antisepsie des plaies et brûlures superficielles |
| Amiodarone | Anti-arythmique (attention : risque de troubles thyroïdiens en usage prolongé) |
| Iododeoxycytidine (Cuterpes) | Antiviral (herpès), pommade à 1% |
| Polyvidone Iodée (PVP-I) | Antiseptique bactéricide, fongicide et virucide à large spectre |
⚠️ Note clinique importante : L’amiodarone apporte une grande quantité d’iode lors d’un traitement prolongé et est souvent à l’origine de troubles thyroïdiens (hypo ou hyperthyroïdie iatrogène).
VII. Points Clés à Retenir
Récapitulatif des Propriétés Essentielles
- Les halogènes ont tous 7 électrons de valence → forte tendance à capter un électron (ions X⁻)
- Pouvoir oxydant décroissant : F₂ > Cl₂ > Br₂ > I₂
- HF est le seul acide faible parmi les halogénures d’hydrogène (liaison H–F très forte + liaisons hydrogène)
- Le fluor est toujours au degré d’oxydation –1 dans ses composés (jamais positif)
- Le chlore peut avoir les degrés d’oxydation –1, +1, +3, +5, +7 (oxacides)
Les Chiffres Clés pour Votre Pratique
- 20–30 % des médicaments modernes contiennent du fluor
- 85 % des médicaments utilisent le chlore dans leur synthèse
- 1/3 des nouvelles molécules actives mises sur le marché contiennent au moins un atome de fluor
- 1 à 2 L de HCl produits par l’estomac chaque jour

Conclusion
Les halogènes sont au cœur de la chimie pharmaceutique moderne. Du fluor qui optimise la biodisponibilité des médicaments au chlore omniprésent dans la synthèse pharmaceutique, en passant par l’iode indispensable aux hormones thyroïdiennes, chaque élément de ce groupe possède un profil unique de propriétés chimiques et biologiques.
En tant que futur pharmacien, maîtriser ces notions vous permettra non seulement de réussir vos examens, mais aussi de mieux comprendre la rationale chimique derrière les médicaments que vous dispenserez et les précautions d’emploi associées.



