Réactions de Précipitation en Chimie Analytique : Cours Complet pour Étudiants en Pharmacie
Mots-clés SEO : réactions de précipitation, produit de solubilité, argentométrie, méthode de Mohr, Charpentier-Volhard, chimie analytique pharmacie, précipitation fractionnée, solubilité électrolyte
Introduction : Pourquoi les Réactions de Précipitation sont Essentielles en Pharmacie ?
Les réactions de précipitation constituent l’un des piliers fondamentaux de la chimie analytique en pharmacie. Elles permettent d’identifier, de séparer et de doser avec précision des ions présents en solution — une compétence indispensable au futur pharmacien.
Que ce soit pour le contrôle qualité d’un médicament, l’analyse d’un échantillon biologique ou la vérification de la pureté d’une substance pharmaceutique, maîtriser ces réactions est une nécessité absolue. Ce cours couvre l’ensemble des notions théoriques et pratiques, depuis la notion de solubilité jusqu’aux méthodes argentométriques inscrites à la Pharmacopée Européenne.
1. Solubilité et Produit de Solubilité (Ks)
1.1 Définition de la Solubilité
La solubilité S est la quantité maximale d’électrolyte que l’on peut dissoudre dans un litre de solution à une température donnée.
Elle s’exprime en :
- g.L⁻¹ (grammes par litre)
- mol.L⁻¹ (moles par litre)
💡 À retenir : Dès que cette limite est atteinte, la solution est dite saturée. Tout apport supplémentaire de soluté entraîne une précipitation.

1.2 Le Produit de Solubilité (Ks)
Certains électrolytes — hydroxydes métalliques, sels peu solubles, sulfures — saturent très rapidement la solution. La fraction non dissoute coexiste avec la fraction dissoute : on parle d’équilibre hétérogène.
Exemple du chlorure d’argent (AgCl) :
AgCl(s) ⇌ Ag⁺(aq) + Cl⁻(aq)
D’après la loi d’action de masse :
Ks = [Ag⁺] × [Cl⁻]
Par définition : pKs = −log(Ks)
Règle fondamentale :
- Ks faible → pKs élevé → sel très peu soluble
- Ks élevé → pKs faible → sel plus soluble
Relation entre Ks et solubilité S pour AgCl :
Puisque [Ag⁺] = [Cl⁻] = S (d’après l’électroneutralité) :
Ks = S² → S = √Ks
Cette constante ne dépend que de la température. Elle représente le produit ionique maximum compatible avec l’absence de précipitation (solution à la saturation).
1.3 Formule Générale pour un Électrolyte AₙBₘ
Pour tout électrolyte AnBm, l’équilibre de dissolution s’écrit :
AnBm(s) ⇌ n A^(m+)(aq) + m B^(n−)(aq)
Ce qui donne :
Ks = [A^(m+)]ⁿ × [B^(n−)]ᵐ
Et donc : [A^(m+)] = n.S et [B^(n−)] = m.S
Ks = nⁿ × mᵐ × S^(n+m)
S = (Ks / nⁿ × mᵐ)^(1/(n+m))
1.4 Exemple Résolu : Solubilité du Chromate d’Argent Ag₂CrO₄
Données : Ks(Ag₂CrO₄) = 3,0 × 10⁻¹²
Équilibre :
Ag₂CrO₄(s) ⇌ 2 Ag⁺(aq) + CrO₄²⁻(aq)
Ici n = 2, m = 1 :
- [Ag⁺] = 2S
- [CrO₄²⁻] = S
Ks = (2S)² × S = 4S³
S = (Ks/4)^(1/3) = (3,0 × 10⁻¹² / 4)^(1/3)
S ≈ 9,1 × 10⁻⁵ mol.L⁻¹
1.5 Tableau des Produits de Solubilité à 25°C
| Sel | Ks | Sel | Ks |
|---|---|---|---|
| AgCl | 1,80 × 10⁻¹⁰ | Ag₂CrO₄ | 1,30 × 10⁻¹² |
| AgBr | 5,00 × 10⁻¹³ | BaSO₄ | 1,10 × 10⁻¹⁰ |
| AgI | 4,50 × 10⁻¹⁷ | AgSCN | 1,00 × 10⁻¹² |
| PbS | 1,28 × 10⁻²⁸ | — | — |
Plus le Ks est faible, plus le sel est insoluble et précipite facilement.
2. Condition de Précipitation – Le Produit Ionique (Ki)
2.1 Définition
Lorsqu’on mélange deux solutions contenant des ions A^(n+) et X^(p−), on définit le produit ionique :
Ki = [A^(n+)]₀ᵖ × [X^(p−)]₀ⁿ
2.2 Règle de Décision
| Condition | Résultat |
|---|---|
| Ki < Ks | Pas de précipitation — solution insaturée |
| Ki = Ks | Équilibre — solution saturée |
| Ki > Ks | Précipitation — coexistence du solide et des ions en solution |
💡 Astuce pour l’examen : Comparer systématiquement Ki et Ks avant de conclure sur la précipitation.
3. Influence du Milieu sur la Solubilité
3.1 Effet d’Ions Communs (Solution Homo-ionique)
Une solution est homo-ionique par rapport à un composé peu soluble lorsqu’elle contient déjà l’un de ses ions constitutifs.
Exemple : Une solution de NaCl est homo-ionique par rapport à AgCl (présence de Cl⁻).
Mécanisme : Dans une solution saturée de AgCl (AgCl ⇌ Ag⁺ + Cl⁻), si l’on ajoute du NaCl ou du KCl :
- La concentration en Cl⁻ augmente
- Le produit ionique [Ag⁺][Cl⁻] dépasse Ks
- L’équilibre se déplace dans le sens de la précipitation
Conséquence : L’effet d’ions communs diminue la solubilité et augmente la précipitation.
3.2 Effet des Électrolytes Hétéro-ioniques sur la Solubilité
Les électrolytes hétéro-ioniques contiennent des ions différents de ceux du précipité. Ils peuvent augmenter la solubilité de trois façons :
a) Action d’un Acide Fort
Un acide fort HA exerce un effet dissolvant sur les sels d’acides faibles.
- L’acide génère des ions H₃O⁺
- Ces ions réagissent avec la base A⁻ (provenant du sel)
- La concentration en A⁻ diminue → Ks devient supérieur au produit ionique → la solubilité augmente
Règle générale : La solubilité des sels d’acides faibles augmente quand le pH diminue.
Application pharmaceutique : C’est pourquoi certains médicaments peu solubles sont formulés en sels acides pour améliorer leur biodisponibilité.
b) Formation d’un Complexe
Exemple : Ajout d’ammoniac NH₃ en excès à une solution saturée d’AgCl :
AgCl ⇌ Cl⁻ + Ag⁺ Ag⁺ + 2NH₃ → [Ag(NH₃)₂]⁺ (ion complexe diamine-argent)
La complexation fait chuter [Ag⁺] libre → le produit ionique devient inférieur à Ks → dissolution du précipité → la solubilité augmente.
💡 Ce phénomène est exploité pour dissoudre des précipités et purifier certaines substances.
c) Effet de Sel (Électrolyte Inerte)
La présence de sels solubles sans ion commun (ex : KNO₃, NaNO₃) augmente la solubilité d’un sel peu soluble comme PbSO₄.
Ce phénomène est appelé effet de sel ou phénomène de sel. Il est dû à la diminution des activités ioniques en milieu très ionique.
4. Précipitation Fractionnée
4.1 Principe
Lorsqu’une solution contient plusieurs ions susceptibles de précipiter avec un même réactif, les précipités se forment successivement, dans l’ordre croissant de leur Ks (les moins solubles précipitent en premier).
4.2 Exemple : Les Halogénures d’Argent
Lors de l’ajout progressif d’une solution de AgNO₃ à un mélange d’ions I⁻, Br⁻ et Cl⁻ à concentrations voisines :
| Ordre de précipitation | Sel formé | Ks | Couleur |
|---|---|---|---|
| 1er | AgI (iodure) | 4,5 × 10⁻¹⁷ | Jaune |
| 2ème | AgBr (bromure) | 5,0 × 10⁻¹³ | Jaune pâle |
| 3ème | AgCl (chlorure) | 1,8 × 10⁻¹⁰ | Blanc |
L’ion I⁻ est séparé bien avant que Br⁻ puis Cl⁻ ne commencent à précipiter.
5. Applications en Chimie Analytique Pharmaceutique

5.1 Analyse Qualitative
La précipitation sélective permet d’identifier et de séparer des ions en solution :
- Les ions Cl⁻ sont détectés et séparés à l’état de AgCl (précipité blanc caractéristique)
- Les ions Ba²⁺ sont précipités à l’état de BaSO₄ (précipité blanc insoluble dans les acides)
- Cette méthode est utilisée en analyse systématique et en contrôle de pureté pharmaceutique
5.2 Analyse Quantitative : Méthodes Gravimétriques
L’ion à doser est précipité sous forme d’un sel insoluble, filtré puis pesé avec précision.
Exemple : Dosage des sulfates par précipitation en BaSO₄, filtration et pesée du précipité séché.
5.3 Analyse Quantitative : Méthodes Titrimétriques (Argentométrie)

L’argentométrie est la méthode titrimétrique par précipitation la plus utilisée en pharmacie. Elle repose sur le pouvoir précipitant de l’ion Ag⁺ vis-à-vis de différents anions.
Préparation de la solution titrée de AgNO₃
La solution de nitrate d’argent est l’agent titrant de référence :
AgNO₃ → Ag⁺ + NO₃⁻
- Masse molaire : M(AgNO₃) = 170 g/mol → Équivalent gramme E = 170 g
- On prépare généralement une solution 0,1 N
- Le titre est vérifié par une solution étalon de NaCl (M = 58,45 g.mol⁻¹)
⚠️ Remarque importante : Le nitrate d’argent n’est pas suffisamment soluble pour préparer des solutions normales à 1 N.
6. Les Méthodes de Dosage Argentométriques
6.1 Méthode de Mohr (Milieu Neutre)
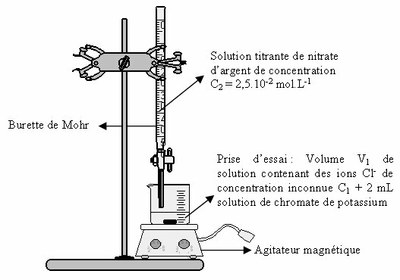
Principe : On ajoute la solution de AgNO₃ à la solution à analyser en présence d’un indicateur de fin de réaction : le chromate de potassium K₂CrO₄.
Déroulement du dosage :
- Pendant le dosage : Ag⁺ + Cl⁻ → AgCl ↓ (précipité blanc)
- Au point d’équivalence : 2Ag⁺ + CrO₄²⁻ → Ag₂CrO₄ ↓ (précipité rouge-orangé) → fin du dosage
Conditions de pH indispensables :
- pH < 6 : le chromate d’argent Ag₂CrO₄ se dissout → indicateur inactif → dosage impossible
- pH > 10,5 : formation d’oxyde d’argent (AgO) brun → interférence
- Zone optimale : pH entre 6 et 10
Applications :
- Dosage des chlorures Cl⁻ ✅
- Dosage des bromures Br⁻ ✅
- Dosage des iodures I⁻ ❌ (non applicable : caractère adsorbant et coloration jaune de AgI)
6.2 Méthode de Charpentier-Volhard (Milieu Acide)
Cette méthode est inscrite à la Pharmacopée Européenne (3ème édition).
C’est une méthode indirecte en retour, utilisée lorsqu’aucun indicateur n’est disponible en milieu acide pour les halogénures.
Elle se déroule en deux étapes :
Étape 1 – Précipitation de l’halogénure par excès de AgNO₃ :
Ag⁺ + Cl⁻ → AgCl ↓
On introduit un excès connu de AgNO₃ pour précipiter tout le chlorure.
Étape 2 – Dosage de l’excès de Ag⁺ par le thiocyanate SCN⁻ :
SCN⁻ + Ag⁺ → AgSCN ↓
En présence d’alun de fer ammoniacal (indicateur) et en milieu nitrique :
Fe³⁺ + SCN⁻ → [Fe(SCN)]²⁺ (complexe rose) → fin du dosage
Avantage : Applicable en milieu acide, ce qui la rend utilisable pour les halogénures, les cyanures et d’autres anions.
💡 La différence entre la quantité de Ag⁺ ajoutée et l’excès dosé permet de calculer la quantité d’anion initial.
7. Comparatif des Méthodes Argentométriques
| Critère | Méthode de Mohr | Méthode de Charpentier-Volhard |
|---|---|---|
| Milieu | Neutre (pH 6–10) | Acide (milieu nitrique) |
| Indicateur | K₂CrO₄ (rouge-orangé) | Fe³⁺ / SCN⁻ (rose) |
| Type de dosage | Direct | Indirect (retour) |
| Ions dosables | Cl⁻, Br⁻ | Cl⁻, Br⁻, I⁻, SCN⁻ |
| Référence | Usage courant | Pharmacopée Européenne |
8. Points Clés à Retenir pour l’Examen
Résumé des notions essentielles :
- La solubilité S est la quantité maximale d’électrolyte dissous par litre à une température donnée
- Le produit de solubilité Ks est une constante à température fixée : Ks diminue → sel moins soluble
- Si Ki > Ks → précipitation ; si Ki < Ks → pas de précipitation
- L’effet d’ions communs diminue la solubilité (déplacement d’équilibre vers la précipitation)
- Un acide fort augmente la solubilité des sels d’acides faibles (le pH joue un rôle crucial)
- La précipitation fractionnée suit l’ordre inverse des Ks (le plus faible Ks précipite en premier)
- La méthode de Mohr est directe, en milieu neutre, avec K₂CrO₄ comme indicateur
- La méthode de Charpentier-Volhard est indirecte, en milieu acide, inscrite à la Pharmacopée Européenne

Conclusion
Maîtriser les réactions de précipitation, c’est acquérir un outil analytique fondamental qui vous accompagnera tout au long de votre parcours en pharmacie : du contrôle qualité des médicaments à l’analyse biologique, en passant par la chimie thérapeutique.
La bonne compréhension du produit de solubilité Ks, des conditions de précipitation et des méthodes argentométriques vous permettra de répondre avec rigueur aux questions d’examen et de TP.
Bon courage dans vos études ! 🎓



