Complexométrie en Pharmacie : Guide Complet pour Maîtriser les Complexes et leurs Applications
À retenir : La complexométrie est l’une des techniques analytiques les plus utilisées dans les laboratoires pharmaceutiques. Elle permet le dosage précis de la quasi-totalité des cations métalliques et intervient directement dans le contrôle qualité des médicaments.
Introduction : Pourquoi la Complexométrie est Incontournable en Pharmacie
Dans de nombreux médicaments, la présence de cations métalliques — calcium, magnésium, zinc, fer — est déterminante pour leur efficacité thérapeutique. Pour en contrôler les teneurs avec précision, les pharmaciens et biologistes s’appuient sur une famille de méthodes analytiques appelées réactions de complexation.
Lorsque certains composés se dissolvent dans l’eau, ils ne se dissocient pas en leurs constituants simples. Au contraire, ils forment des entités stables et solubles appelées complexes. La maîtrise de ces équilibres est au cœur de la chimie analytique pharmaceutique.
Ce cours vous guidera pas à pas, de la définition des complexes jusqu’aux techniques de dosage appliquées au laboratoire officinal et hospitalier.

I. Définition et Structure des Complexes
Qu’est-ce qu’un complexe ?
Un complexe est un édifice polyatomique formé de :
- Un ou plusieurs ions métalliques (appelés ions coordinateurs)
- Des anions ou molécules — minéraux ou organiques — qui entourent cet ion central (appelés ligands ou coordinats)
Exemple concret : Le complexe tétramine cuivre (II), noté [Cu(NH₃)₄]²⁺, est formé d’un ion Cu²⁺ entouré de quatre molécules d’ammoniac NH₃. C’est ce complexe qui donne sa couleur bleu intense aux solutions ammoniacales de cuivre.
Terminologie essentielle à connaître
L’ion coordinateur (atome central)
- Si un seul ion central : complexe mononucléaire
- Si plusieurs ions centraux : complexe polynucléaire
Les ligands (coordinats)
- Coordinat unidenté : une seule liaison avec l’ion central (ex. : Cl⁻, NH₃, H₂O)
- Coordinat polydenté ou multidenté : plusieurs liaisons simultanées avec l’ion central
Point important : La charge globale du complexe = charge de l’ion coordinateur + somme des charges des coordinats. Un complexe peut donc être cationique, anionique ou neutre.
Exemple : [Fe(CN)₆]³⁻ → charge = (+3) + 6×(−1) = −3 → complexe anionique
Le nombre de coordination (NC)
Le nombre de coordination désigne le nombre total de liaisons formées entre l’ion coordinateur et ses ligands.
Les valeurs les plus fréquentes en chimie de coordination sont : NC = 2, 4, 6, 8
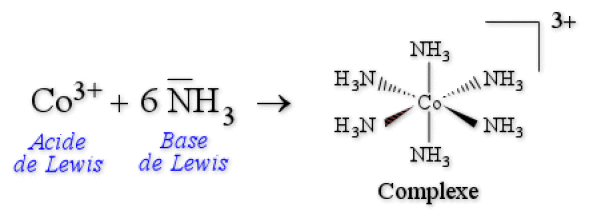
Les liaisons créées sont des liaisons de coordination (ou covalences datives) :
- L’ion coordinateur = accepteur de doublet électronique = acide de Lewis
- Le ligand = donneur de doublet électronique = base de Lewis
⚠️ Attention : Le nombre de coordination est différent du degré d’oxydation (ou nombre d’oxydation) de l’ion métallique. Exemple : Fe³⁺ dans [Fe(CN)₆]³⁻ a un degré d’oxydation de +3 mais un NC de 6.
II. Nomenclature des Complexes (Règles IUPAC)
La nomenclature suit les règles établies par l’IUPAC (International Union for Pure and Applied Chemistry).
Règles générales
Ordre dans la formule : L’atome central est indiqué en premier, puis les ligands négatifs, neutres et positifs, entre crochets.
Nom des ligands :
- Anions : suffixe « o » → Cl⁻ = chloro ; S₂O₃²⁻ = thiosulfato
- Molécules neutres : nom conservé, sauf exceptions (H₂O = aqua ; NH₃ = ammine ; CO = carbonyle ; NO = nitrosyle)
- Nombre de ligands : di-, tri-, tétra-, penta-, hexa-…
Dénomination selon la charge du complexe
| Charge | Règle | Exemple |
|---|---|---|
| Négative | nom du ligand + nom métal + suffixe « ate » + chiffre romain | [Fe(CN)₆]³⁻ = hexacyanoferrate(III) |
| Positive | nom du ligand + nom métal + chiffre romain | [Cu(NH₃)₄]²⁺ = tétraminecuivre(II) |
| Neutre | nom métal + nom du ligand | [Fe(CO)₅] = fer pentacarbonyle |
III. Types de Complexes
1. Complexes simples
Chaque coordinat n’est lié à l’ion coordinateur que par une seule liaison.
2. Complexes internes ou chélates
Les chélates sont formés par des coordinats multidentés qui contractent toutes leurs liaisons avec un même ion métallique. Il en résulte une structure cyclique dans laquelle l’ion est “pincé” par le ligand chélateur.
Le terme “chélate” vient du grec chêlê signifiant “pince de crabe” — une image parlante de la façon dont le ligand saisit l’ion métallique.
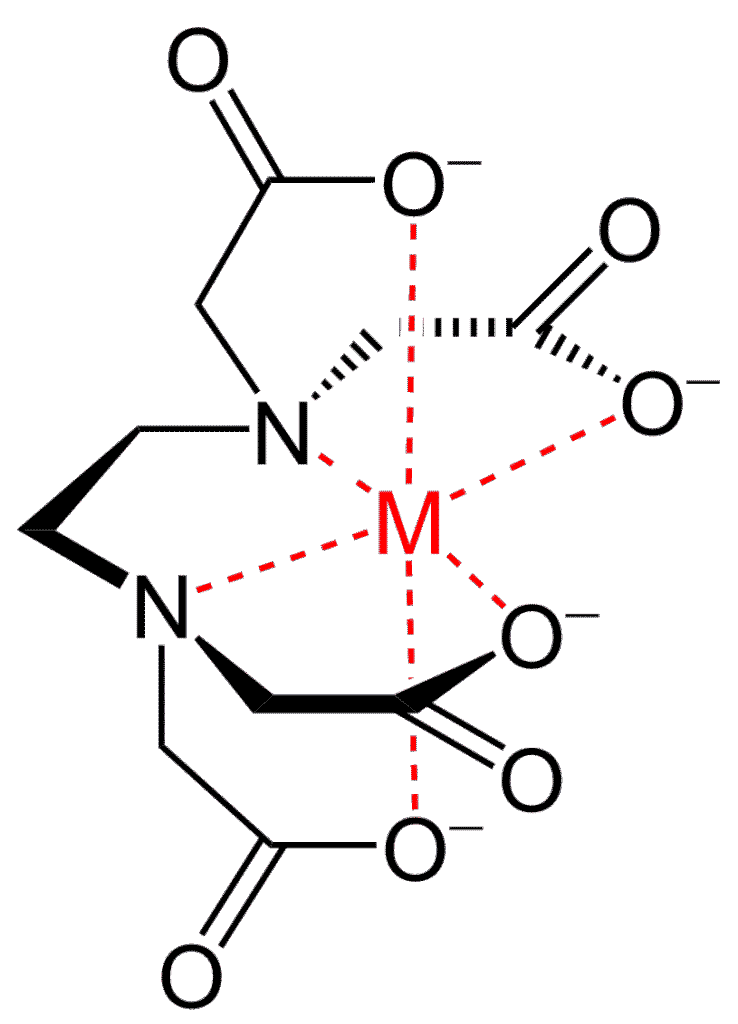
L’EDTA : le chélateur de référence en pharmacie
L’Acide Éthylène Diamine Tétracétique (EDTA) est le complexon le plus utilisé en complexométrie. Ses atouts :
- Il peut former jusqu’à 6 liaisons avec un ion bivalent (hexadenté)
- Il forme des chélates stables avec pratiquement tous les métaux
- Il existe sous formes variées : H₄Y (EDTA libre), Na₂H₂Y (sel disodique utilisé en pratique)
Applications pharmaceutiques de l’EDTA :
- Agent conservateur dans les collyres et solutions injectable (prévient la croissance microbienne)
- Agent séquestrant dans les préparations cosmétiques et pharmaceutiques
- Actif dans le traitement du saturnisme (intoxication au plomb)
IV. Stabilité des Complexes
Complexes parfaits vs complexes imparfaits
| Critère | Complexe parfait | Complexe imparfait |
|---|---|---|
| Dissimulation des constituants | Totale | Partielle |
| Dissociation | Très faible | Plus ou moins grande |
| Stabilité | Élevée | Modérée à faible |
Règle générale : Plus la stabilité est grande → plus la dissociation est faible → plus les concentrations des constituants libres sont faibles.
VI-1. Constante de stabilité des complexes
Pour un complexe [MₘLₙ], les deux équilibres coexistent en solution :
Formation : mM + nL ⇌ [MₘLₙ]
La constante de stabilité (ou constante de formation) Ks est définie par :
Ks = [MₘLₙ] / ([M]ᵐ × [L]ⁿ)
La constante de dissociation Kc est l’inverse : Kc = 1/Ks
📌 À retenir : Plus Ks est grand → complexe plus stable. Plus Kc est grand → complexe moins stable. On utilise souvent les formes logarithmiques : pKs = −log Ks.
Constantes successives pour le complexe [MLₙ] :
Chaque étape d’addition d’un ligand possède sa propre constante partielle :
M + L ⇌ [ML] Ks₁
ML + L ⇌ [ML₂] Ks₂
...
MLₙ₋₁ + L ⇌ [MLₙ] Ksₙ
La constante globale de stabilité est le produit des constantes partielles :
Ks = Ks₁ × Ks₂ × Ks₃ × ... × Ksₙ
VI-2. Calcul des concentrations à l’équilibre
Pour le complexe [ML] formé entre M et L, avec les concentrations initiales CM et CL :
Équations de conservation de la masse :
- CM = [M] + [ML]
- CL = [L] + [ML]
Cas simplifié (CL = CM = C) :
[M] = (−1 + √(1 + 4·Ks·C)) / (2·Ks)
Simplification pour un complexe stable (pKc > 7, donc Ks > 10⁷) :
Si [M] << C, alors :
[M] ≈ √(C / Ks)
Application numérique : Pour [CaY]²⁻ avec Ks = 10¹⁰·⁷ et C = 10⁻² M :
[Ca²⁺] ≈ √(10⁻² / 10¹⁰·⁷) ≈ 10⁻⁶·³⁵ mol/L — extrêmement faible, complexe très stable.
VI-3. Prévision de formation des complexes
Lorsque deux ions métalliques M₁ et M₂ sont en compétition pour un même ligand L :
M₁L + M₂ ⇌ M₂L + M₁ K = Ks₂ / Ks₁
Règle générale : La réaction de complexation se produit dans le sens de formation du complexe le plus stable.
- Si Ks₂ > Ks₁ → formation de [M₂L] favorisée
- Si Ks₁ > Ks₂ → maintien de [M₁L]
Application en pharmacie : Ce principe est exploité dans le traitement du saturnisme. L’administration de [CaY]²⁻ (EDTA-calcium) permet de substituer le calcium par le plomb, beaucoup plus affin pour l’EDTA, et d’éliminer le plomb sous forme de [PbY]²⁻ par voie urinaire.
V. Facteurs Influençant la Stabilité des Complexes
1. Facteurs internes
a) Nature de l’ion coordinateur
Un complexe est d’autant plus stable que l’ion coordinateur présente :
- Une valence ionique élevée (charge importante)
- Un faible volume atomique (densité de charge élevée)
Classement pratique :
- Alcalins (groupe IA) : Li⁺, Na⁺, K⁺ → ne forment pas de complexes stables
- Métaux de transition (bloc d) : Fe, Co, Ni, Cu, Zn → forment les complexes les plus stables
⚠️ Conséquence analytique directe : La complexonométrie permet de doser la quasi-totalité des métaux sauf les alcalins.
b) Nature du coordinat
Un complexe est d’autant plus stable que ses coordinats sont de fortes bases de Lewis (fort pouvoir donneur de doublet électronique).
Stabilité des chélates — facteurs clés :
| Facteur | Condition optimale |
|---|---|
| Rapport : nb ligands / nb ions | Valeur ≈ 1 |
| Nombre de cycles formés | Plus il y en a, plus le complexe est stable |
| Taille des cycles | Cycles à 5 chaînons (pentagonaux) = stabilité maximale |
| Nature des atomes donneurs | O et N → chélates les plus stables |
L’EDTA remplit tous ces critères : il forme des cycles à 5 chaînons, ses atomes donneurs sont O et N, et il est hexadenté. C’est pourquoi il est le complexon de choix en analyse pharmaceutique.
2. Facteurs externes — Constante conditionnelle de stabilité K’s
En pratique, des réactions parasites accompagnent toujours la complexation principale : protonation des ligands, hydrolyse des métaux, compétition avec d’autres ligands. Ces réactions parasites réduisent l’efficacité de la complexation.
Pour en tenir compte, on définit la constante conditionnelle de stabilité K’s :
K's = [MLₙ] / ([M'] × [L']ⁿ)
Où [M’] et [L’] représentent les concentrations totales des espèces libres (toutes formes confondues, hors complexe).
Relation avec Ks via les coefficients de Schwarzenbach (α) :
K's = Ks / (αM × αLⁿ)
log K's = log Ks − log αM − n × log αL
Comme α ≥ 1 toujours, on a : K’s ≤ Ks
Les réactions parasites diminuent toujours la stabilité apparente du complexe.
Influence du pH sur la stabilité des complexes
Le pH est le facteur externe le plus important en complexonométrie. Son influence est déterminante lorsque le coordinat est la base conjuguée d’un acide faible (comme F⁻, Y⁴⁻, etc.).
Exemple 1 : Complexe [FeF]²⁺ (Ks = 10⁵·²)
En milieu acide, F⁻ est protonée en HF (Ka = 10⁻³·⁷) :
αF = 1 + [H₃O⁺]/Ka
K's = Ks / (1 + [H₃O⁺]/Ka)
→ Si pH ↓, [H⁺] ↑ → αF ↑ → K’s ↓ → le complexe se dissocie → Si pH ↑, [H⁺] ↓ → αF → 1 → K’s → Ks → le complexe est plus stable
Exemple 2 : Stabilité des chélates EDTA-métal en fonction du pH
L’EDTA est un tétracide (H₄Y) qui se dissocie en solution en quatre étapes successives :
H₄Y ⇌ H₃Y⁻ ⇌ H₂Y²⁻ ⇌ HY³⁻ ⇌ Y⁴⁻
Ka1 Ka2 Ka3 Ka4
1,02×10⁻² 2,14×10⁻³ 6,92×10⁻⁷ 5,5×10⁻¹¹
La forme active pour la complexation est Y⁴⁻. Le coefficient αY s’exprime par :
αY = 1 + [H⁺]/Ka4 + [H⁺]²/(Ka4·Ka3) + [H⁺]³/(Ka4·Ka3·Ka2) + [H⁺]⁴/(Ka4·Ka3·Ka2·Ka1)
Conséquences pratiques :
- À pH basique (>10) : αY ≈ 1 → K’s ≈ Ks → efficacité maximale
- À pH acide : αY >> 1 → K’s << Ks → efficacité très réduite
- À pH > 10 : précipitation des hydroxydes métalliques (problème pratique)
✅ En pratique : Les dosages par l’EDTA sont réalisés dans un tampon NH₃/NH₄Cl à pH 9–10, qui optimise la stabilité des complexes sans provoquer la précipitation des hydroxydes.
Un avantage majeur : En ajustant le pH, on peut réaliser des dosages sélectifs. Exemple : à pH 2, l’EDTA forme un complexe très stable avec Fe³⁺ (log K’s élevé) mais pratiquement aucun complexe avec Ca²⁺ → on peut doser le fer en présence de calcium sans interférence.
VI. Applications Analytiques des Complexes en Pharmacie
Vue d’ensemble
Les applications des réactions de complexation en pharmacie et en biologie couvrent quatre grands domaines :
- Analyse qualitative (identification des ions)
- Analyse quantitative (dosage par mercurimétrie et complexonométrie)
- Traitement thérapeutique (chélation des métaux toxiques)
- Pharmacologie des interactions médicamenteuses
A. Analyse qualitative
- Formation de complexes colorés pour identifier des ions métalliques (ex. : [Fe(SCN)]²⁺ rouge sang pour Fe³⁺)
- Solubilisation de sels peu solubles via formation de complexes solubles (ex. : AgCl + NH₃ → [Ag(NH₃)₂]⁺)
- Masquage d’ions lors de réactions de caractérisation (ex. : masquage de Cu²⁺, Ni²⁺, Mn²⁺ sous forme de complexes cyanés pour permettre la caractérisation sélective de Cd²⁺)
B. Analyse quantitative — Complexonométrie
Définition et intérêt
La complexonométrie est l’ensemble des méthodes titrimétriques basées sur la formation de complexes métalliques solubles par des chélateurs appelés complexons (acides aminocarboxyliques).
Elle permet :
- Le dosage de la quasi-totalité des métaux, sauf les alcalins (Li⁺, Na⁺, K⁺)
- Des dosages sélectifs dans des mélanges (en jouant sur K’s via le pH)
En laboratoire hospitalier : La complexonométrie est notamment utilisée pour doser le calcium et le magnésium sanguins, le zinc dans les préparations injectables, et contrôler la pureté des sels métalliques pharmaceutiques.
Principe d’un titrage complexonométrique
- Mise en présence de quantités équivalentes de l’agent complexant (EDTA) et du cation métallique à doser
- Détection du point de fin de titrage par un moyen approprié (indicateur coloré, potentiométrie, photométrie)
- Ajustement du pH : choix d’un pH pour lequel :
- K’s ≥ 10⁷ pour le chélate de l’ion à doser (dosage quantitatif)
- K’s ≤ 10² pour les ions métalliques interférants (sélectivité)
- Pas de précipitation d’hydroxyde métallique
Coordinats utilisés en complexonométrie
| Complexon | Formule | pKa |
|---|---|---|
| Complexon I (NTA) | H₃A | 1,9 ; 2,5 ; 9,7 |
| Complexon II (EDTA) | H₄Y | 1,9 ; 2,7 ; 6,1 ; 10,3 |
| Complexon III (sel disodique EDTA) | Na₂H₂Y | — |
Le complexon III (Na₂H₂Y·2H₂O, sel disodique de l’EDTA) est la forme la plus utilisée en pratique en raison de sa bonne solubilité dans l’eau.
Solutions étalons en complexonométrie
Étalons d’ions coordinateurs :
- Solutions de Ca²⁺ : dissolution de CaCO₃ dans un minimum d’HCl
- Solutions de Zn²⁺ : dissolution du métal Zn dans un minimum d’HCl
Étalons chélateurs :
- Na₂H₂Y·2H₂O de qualité « pour analyse »
- Titres compris entre 0,001 M et 0,1 M
⚠️ Éviter toute contamination par des ions métalliques étrangers (eau distillée et verrerie peuvent en apporter). Il est préférable d’étalonner l’EDTA par rapport à des sels métalliques très purs.
C. Courbes de titrage et détection du point d’équivalence
La courbe de titrage représente pM (ou pM’) en fonction du volume V’ d’EDTA ajouté.
Pour le titrage de 10 mL de Zn²⁺ (10⁻² M) par l’EDTA (10⁻² M), on observe :
- Avant l’équivalence : pM faible (métal libre en excès)
- Au point d’équivalence : saut brutal de pM
- Après l’équivalence : pM dictée par l’excès d’EDTA
Ce saut de pM permet de déterminer graphiquement le point d’équivalence.
D. Indicateurs de métaux (métalloindicteurs)
Les indicateurs colorés sont des ligands organiques (notés I) qui :
- Forment un complexe coloré [MI] avec le cation à doser
- Ont une couleur différente sous forme libre (I) et sous forme complexée ([MI])
- Forment un complexe moins stable que le complexe [MY] (EDTA-métal)
Condition de choix : K’s[MI] < K’s[MY]
Mécanisme du virage :
- Début du titrage : solution colorée par [MI]
- Cours du titrage : l’EDTA complexe d’abord le métal libre
- Au point d’équivalence : l’EDTA déplace l’indicateur de [MI] → virage vers la couleur de I libre
| Famille | Indicateurs | Ions sensibles |
|---|---|---|
| Dérivés azoïques | NET (Eriochrome Black T) | Mg²⁺ |
| Dérivés azoïques | Calcon | Ca²⁺ |
| Dérivés azoïques | Patton/Reeder | Ca²⁺ |
| Dérivés azoïques | PAN | Hg²⁺, Cu²⁺ |
| Phtaléines | Calcéine | Ca²⁺ |
| Triphénylméthane | Aluminon | Al³⁺ |
| Composés hétérocycliques | Murexide | Ca²⁺, Co²⁺, Ni²⁺, Cu²⁺ |
E. Techniques de dosage
1. Dosage direct
Conditions : indicateur disponible + réaction rapide avec l’EDTA
Début : I + M²⁺ → [MI] (couleur du complexe)
Point d'équivalence : Y⁴⁻ + [MI] → [MY]²⁻ + I (couleur de l'indicateur libre)
Calcul : C = (Veq × C₀) / V
Exemples : dosage de Ca²⁺ en présence de murexide, calcon ou calcéine ; dosage de Mg²⁺ avec le NET.
2. Dosage en retour
Utilisé quand : aucun indicateur approprié disponible, ou réaction analyte/EDTA trop lente.
Principe :
- On ajoute un excès connu d’EDTA à la solution à doser
- On laisse la réaction se compléter
- L’excès d’EDTA est ensuite titré par une solution métallique titrée M₁ (Zn²⁺ ou Mg²⁺) en présence d’un indicateur
Condition : K’s[MY] > K’s[M₁Y] ≥ 10⁷
Calcul : C = (V’C’ − Veq·C₀) / V
3. Dosage par déplacement (substitution)
Utilisé quand : aucun indicateur disponible pour l’analyte considéré.
Principe :
- On ajoute la solution de M₁ à un excès de complexe [M₂Y] moins stable
- M₁ déplace M₂ : M₁ + [M₂Y] → [M₁Y] + M₂
- M₂ libéré est titré par l’EDTA en présence d’indicateur
Condition : K’s[M₁Y] > K’s[M₂Y] ≥ 10⁷
Calcul : C = Veq·C₀ / V
VII. Applications Thérapeutiques des Complexes
A. Traitement des intoxications métalliques (chélation)
Lorsqu’un métal toxique est présent dans l’organisme en quantités excessives, l’administration d’un médicament chélateur permet de le complexer et de l’éliminer.
Exemple phare : Le traitement du saturnisme (intoxication au plomb)
[CaY]²⁻ + Pb²⁺ → [PbY]²⁻ + Ca²⁺
Ks (PbY) > Ks (CaY)
- L’EDTA est administré sous forme de chélate de calcium (non toxique)
- Le plomb, plus affin pour l’EDTA, déplace le calcium
- Le complexe [PbY]²⁻ hydrosoluble est éliminé par voie urinaire
- Le calcium libéré, non toxique, reste dans l’organisme
Autres applications thérapeutiques de la chélation :
- Intoxication au mercure → chélateurs sulfurés (DMSA, DMPS)
- Surcharge en fer (hémochromatose, thalassémie) → déféroxamine, déférasirox
- Intoxication à l’arsenic → BAL (British Anti-Lewisite)
B. Interactions médicamenteuses liées aux complexes
Certains médicaments peuvent former des complexes avec des cations bivalents présents dans les aliments ou dans d’autres médicaments, réduisant leur absorption.
Exemples cliniques importants :
- Tétracyclines + Ca²⁺/Mg²⁺ : formation de complexes insolubles → réduction majeure de l’absorption intestinale → ne pas prendre avec le lait ou des antiacides
- Fluoroquinolones + Ca²⁺/Mg²⁺/Fe²⁺ : même phénomène → intervalle d’au moins 2h entre la prise de l’antibiotique et celle d’un antiacide ou d’un supplément de fer
- Furosémide + cations bivalents : chélation partielle
Message clinique : Ces interactions médicamenteuses doivent être systématiquement prises en compte lors des prescriptions et des conseils officinaux, notamment chez les patients polymédiqués ou supplémentés en minéraux.
Résumé des Points Clés à Retenir
Voici les notions fondamentales à maîtriser pour l’étudiant en pharmacie :
- Un complexe est un édifice polyatomique formé d’un ion coordinateur entouré de ligands liés par des liaisons de coordination (acide de Lewis / base de Lewis)
- Ks quantifie la stabilité : plus Ks est grand, plus le complexe est stable et moins il se dissocie
- K’s (constante conditionnelle) reflète la réalité en tenant compte des réactions parasites ; K’s ≤ Ks toujours
- Le pH est le facteur externe le plus critique : un pH optimal autour de 9–10 est requis pour les dosages à l’EDTA
- L’EDTA est le chélateur de référence : hexadenté, il forme des complexes très stables avec pratiquement tous les métaux de transition
- Trois techniques de dosage existent : direct, en retour, par déplacement — le choix dépend de la disponibilité d’un indicateur et de la cinétique de la réaction
- En thérapeutique, la chélation est utilisée pour traiter les intoxications métalliques et les surcharges en métaux
- En officine, les interactions médicamenteuses par complexation (antibiotiques + minéraux) doivent être systématiquement prévenues

Pour Aller Plus Loin
- Pratiquer les calculs de pM et des concentrations à l’équilibre avec différents complexes
- S’entraîner sur les courbes de titrage et l’identification graphique du point d’équivalence
- Consulter les monographies de la Pharmacopée Européenne relatives aux dosages par complexonométrie (Ca, Mg, Zn dans les préparations injectables)
- Explorer les fiches de l’ANSM sur les interactions médicamenteuses impliquant des chélateurs