Méthodes de Séparation en Chimie Analytique : Guide Complet pour les Étudiants en Pharmacie
Résumé : Maîtriser les méthodes de séparation est une compétence fondamentale en pharmacie. De la filtration à l’ultracentrifugation, en passant par la précipitation et le relargage, ce guide complet vous explique chaque technique avec clarté, exemples concrets et applications pharmaceutiques.
I. Généralités sur les Méthodes de Séparation
Les méthodes de séparation constituent l’une des branches les plus anciennes de la chimie analytique, autrefois désignée sous le nom d’analyse immédiate. Elles ont permis l’isolement de nombreuses substances d’intérêt pharmaceutique et biologique, notamment :
- Les corps gras (lipides, cires végétales)
- Les alcaloïdes (morphine, quinine, caféine)
- Les hétérosides (digitaline, salicine)
Avec l’évolution des sciences, de nouvelles substances ont pu être isolées grâce à des techniques plus avancées : vitamines, hormones, antibiotiques. Ces progrès ont été rendus possibles grâce au développement des méthodes chromatographiques et électrophorétiques, qui restent aujourd’hui incontournables dans les laboratoires pharmaceutiques et hospitaliers.

💡 À retenir : En pharmacie industrielle, les méthodes de séparation interviennent à chaque étape du processus : extraction des principes actifs, purification des substances, contrôle qualité des médicaments.
II. Principes Généraux de l’Analyse Immédiate
Avant de choisir une méthode de séparation, il est essentiel d’identifier la nature du mélange de départ. Deux grandes situations se présentent :
1. Une solution homogène — obtenue par extraction d’un mélange naturel (plante, tissu animal) ou issue d’une réaction de synthèse chimique.
2. Un mélange hétérogène — comme des organes végétaux ou animaux broyés, contenant plusieurs phases (solide, liquide, etc.).
Le choix de la méthode dépend directement de cette distinction. Une mauvaise identification peut conduire à des pertes de rendement ou à une dégradation du principe actif.
III. Séparation des Constituants d’un Mélange Hétérogène
1. Mélange Phase Solide / Phase Liquide
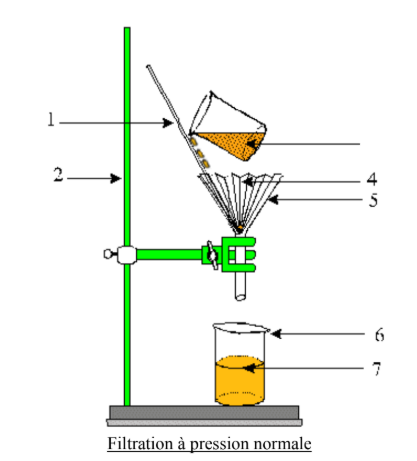
a) La Filtration
Filtrer consiste à faire passer un mélange à travers une membrane poreuse, perméable aux liquides mais imperméable aux solides en suspension.
Deux éléments sont essentiels à maîtriser : le choix de la matière filtrante et la technique de mise en œuvre.
🔬 Les Matières Filtrantes
Substances organiques :
| Matériau | Avantages | Inconvénients |
|---|---|---|
| Papier filtre / Pâte de cellulose | Économique, facile d’usage | Attaqué par acides/bases forts ; forme des alcali-celluloses solubles |
| Polymères organiques (disques) | Porosité précisément définie ; filtration jusqu’aux bactéries | Solubles dans certains solvants organiques |
💊 Application en pharmacie : Le papier filtre, bien que limité pour les milieux agressifs, est utilisé en chromatographie sur papier pour séparer des mélanges de médicaments ou d’acides aminés.
Substances minérales :
Les plus utilisées sont les dérivés de la silice, notamment le verre fritté, préparé en chauffant une poudre de verre de granulation définie afin de souder les particules entre elles tout en conservant des espaces (lacunes) entre elles.
La classification des filtres en verre fritté se fait selon leur porosité :
| Numéro | Taille des pores | Efficacité | Rapidité |
|---|---|---|---|
| N° 0 | ~200 µm (très larges) | Faible | Très rapide |
| N° 5 | ~1 µm (très fins) | Très élevée | Lente |
⚠️ Point critique : L’efficacité augmente avec le numéro, mais la rapidité diminue. Les filtres en verre fritté sont fragiles face aux solutions fortement alcalines qui les dissolvent sous forme de silicates.
⚙️ Les Techniques de Filtration
Trois techniques principales existent selon la pression appliquée :
1. Filtration à pression normale La plus simple. Le liquide traverse le filtre uniquement sous l’effet de la gravité. Utilisée pour les mélanges peu visqueux.
2. Filtration sous surpression (filtre-presse) Un gaz comprimé pousse le liquide à travers le filtre. Adaptée aux mélanges visqueux ou aux volumes importants en industrie pharmaceutique.
3. Filtration sous vide (aspiration) La plus courante en laboratoire. On utilise :
- Une fiole de Kitasato (fiole conique avec ajutage latéral relié à une trompe à vide)
- Un entonnoir de Büchner (support en porcelaine avec disque poreux) ou un creuset en verre fritté
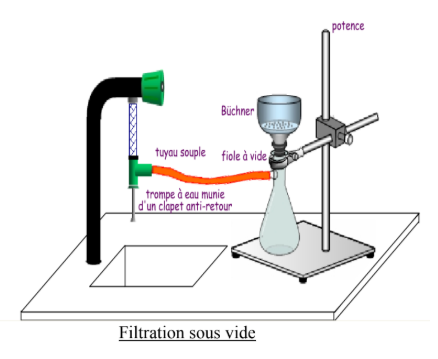
💡 Conseil pratique : La filtration sous vide est préférable pour accélérer la séparation de précipités fins. Veillez cependant à ne pas créer de dépression trop forte qui pourrait déformer le filtre papier.
b) La Centrifugation
La centrifugation exploite la force centrifuge pour accélérer la sédimentation des particules.
Principe physique
Lorsqu’une masse m tourne sur une circonférence de rayon R, elle est soumise à une force centrifuge F :
F = m · ω² · R avec ω = 2π·n (n = nombre de tours/seconde)
Soit : F = 4π²·R·n²·m
L’efficacité dépend donc :
- Du rayon R (généralement 10 à 30 cm)
- Surtout du nombre de tours n (au carré → impact majeur)
Classification des centrifugeuses
| Type | Vitesse | Force (× g) | Applications |
|---|---|---|---|
| Centrifugeuse simple | ~3 000 tr/min | ~1 500 g | Séparation cellules / plasma sanguin |
| Centrifugeuse haute vitesse | ~20 000 tr/min | ~50 000 g | Isolement de bactéries, organites |
| Ultracentrifugeuse | jusqu’à 50 000 tr/min | 250 000 à 1 000 000 g | Séparation de macromolécules (protéines, ADN) |
Avantages et applications pharmaceutiques
- Méthode rapide et efficace, particulièrement pour les suspensions biologiques
- Permet de détruire les émulsions formées entre deux liquides de densités différentes
- L’ultracentrifugation peut séparer des protéines ou des dextrans selon leur masse moléculaire, sans recours à des solvants agressifs
💊 Exemple concret : En pharmacologie, l’ultracentrifugation est utilisée pour isoler des liposomes (vecteurs de médicaments) ou pour purifier des vaccins à base de protéines virales.
2. Mélange de Deux Liquides Non Miscibles : La Décantation
La séparation de deux liquides non miscibles s’effectue par décantation dans une ampoule à décanter (aussi appelée ampoule de separación). Le mélange est laissé au repos jusqu’à séparation nette des deux phases.
Problème fréquent : la formation d’émulsions
Les émulsions sont des dispersions stables d’un liquide dans un autre, stabilisées par des tensioactifs naturels. Elles gênent considérablement la décantation. Pour les détruire, on peut recourir à :
- Un chauffage modéré (déstabilise les tensioactifs)
- Une modification du pH (les émulsions sont plus stables en milieu alcalin)
- L’ajout d’un agent tensioactif opposé (contre-tensioactif)
- La centrifugation (solution la plus rapide et efficace)
💡 Conseil de TP : Lors d’une extraction liquide-liquide (ex. : extraction d’un alcaloïde dans un solvant organique), si une émulsion se forme, essayez d’abord de modifier le pH avant d’agiter trop vigoureusement.
3. Mélange de Phases Solides : La Lévigation
La séparation d’un mélange de solides de densités différentes est possible grâce au procédé de lévigation.
Anecdote historique : C’est Louis Pasteur qui, à l’aide d’une simple pince et d’une loupe, sépara manuellement les cristaux de tartrate droit et lévogyre — une expérience fondatrice de la stéréochimie !
Le principe de la lévigation repose sur l’entraînement par un courant de liquide non solvant des fractions les moins denses d’un mélange. En pratique, pour des mélanges complexes, on rend d’abord le solide aussi homogène que possible par voie mécanique (broyage, tamisage), avant de le traiter comme une phase solide homogène.
IV. Traitement d’une Phase Homogène
A. Séparation par Rupture de Phase (Solution Liquide)
Une fois la solution isolée, l’objectif est de séparer un ou plusieurs constituants à l’état solide ou liquide le plus pur possible. On réalise pour cela une rupture de l’homogénéité, soit par élimination du solvant, soit par modification de la solubilité.
1. Élimination du Solvant
Cas 1 — À pression atmosphérique : Nécessite une élévation importante de température → risques :
- Oxydation à l’air des substances sensibles
- Altération des produits thermolabiles (vitamines, enzymes, hormones)

Cas 2 — Sous pression réduite (recommandé) : Double avantage :
- Opération sous atmosphère protectrice (à l’abri de l’oxydation)
- Température d’évaporation abaissée → préservation des molécules fragiles
On utilise pour cela un évaporateur rotatif (rotavapor), qui associe rotation, chauffage modéré et dépression pour une évaporation douce et efficace.

Élimination des traces résiduelles de solvant
Après évaporation principale, pour éliminer les dernières traces, on place le produit dans un exsiccateur (avec ou sans vide) contenant un agent desséchant adapté :
| Solvant résiduel | Agent desséchant |
|---|---|
| Eau et solvants basiques | Acide sulfurique concentré, anhydride sulfurique |
| Eau uniquement | Silicagel, chlorure de calcium |
| Solvants acides | Pastilles de potasse (KOH) ou de soude (NaOH) |
⚠️ Attention : Ne jamais utiliser le chlorure de calcium pour éliminer des solvants basiques — il réagit avec eux. Toujours adapter le desséchant à la nature chimique du solvant.
2. Précipitation : Diminution du Pouvoir Solvant
La précipitation consiste à réduire la solubilité d’un composé dans son solvant jusqu’à provoquer sa cristallisation ou son précipité. Trois approches principales :
a) Variation de Température
La solubilité de la plupart des solides augmente avec la température. Par conséquent, un refroidissement contrôlé provoque la cristallisation du soluté. Cette méthode, douce et peu dénaturante, est utilisée pour purifier des substances pharmaceutiques par recristallisation.
💊 Exemple : La recristallisation de l’acide acétylsalicylique (aspirine) après synthèse se fait par dissolution à chaud dans l’éthanol, puis refroidissement lent.
b) Addition d’un Non-Solvant
L’ajout d’un second liquide miscible au premier mais non solvant pour la substance entraîne sa précipitation.
Exemples concrets :
- Solution alcoolique d’acide salicylique + eau → précipitation de l’acide (eau et alcool sont miscibles, mais l’acide salicylique est peu soluble dans l’eau)
- Solution chloroformique de digitaline + éther de pétrole → précipitation de la digitaline
- Solution méthanolique d’alcaloïde + éther éthylique → précipitation de l’alcaloïde
⚠️ Inconvénient : Cette méthode est brutale et peut entraîner l’inclusion d’impuretés dans le précipité. Elle est rarement utilisée seule pour des purifications poussées.
c) Le Relargage (Salting-Out)
Le relargage est une méthode de précipitation douce qui consiste à ajouter un sel minéral à la solution, lequel entre en compétition avec le soluté organique pour les molécules d’eau, provoquant la séparation de ce dernier.
Mécanisme : Le sel dissous fixe les molécules d’eau de solvatation, réduisant ainsi la disponibilité du solvant pour maintenir le soluté en solution.
🔎 Composés Relargables
Les composés relargables sont de nature très variable :
- Petites molécules : l’acétone (miscible à l’eau) est relarguée par addition de sulfate d’ammonium
- Macromolécules : différentes protéines (globulines) peuvent être précipitées sélectivement par des solutions de chlorure de lithium, magnésium ou ammonium à des concentrations précises
Principe clé : Plus une molécule possède un pôle hydrophobe important, plus elle est facile à relarguer.
🧪 Les Agents Relargants
Ce sont essentiellement des sels minéraux à forte solubilité dans l’eau. Les principaux agents utilisés sont :
- Sulfate d’ammonium (NH₄)₂SO₄ — le plus utilisé en biochimie
- Chlorure de sodium NaCl
Les agents relargants sont classés selon leur efficacité dans les séries de Hofmeister :
Anions (efficacité décroissante) :
F⁻ > SO₄²⁻ > citrate > tartrate > Cl⁻ > Br⁻
Cations (efficacité décroissante) :
Li⁺ > Na⁺ > K⁺ > NH₄⁺ > Mg²⁺
💡 Astuce mnémotechnique : Les ions en début de série de Hofmeister sont dits kosmotropes (structurants de l’eau) → meilleurs agents relargants. Les ions en fin de série sont chaotropes (perturbateurs) → moins efficaces pour le relargage.
✅ Avantage Majeur du Relargage
Le relargage est une méthode de séparation très douce :
- Pas d’élévation de température
- Pas de solvants organiques dénaturants
- Idéale en biochimie pour préserver l’activité des protéines (enzymes, anticorps)
💊 Application industrielle : Le relargage des protéines par le sulfate d’ammonium (précipitation fractionnée) est une étape clé dans la production industrielle d’anticorps thérapeutiques (immunoglobulines) et d’enzymes pharmaceutiques.
V. Tableau Récapitulatif des Méthodes de Séparation
| Méthode | Type de mélange | Principe | Avantages | Inconvénients |
|---|---|---|---|---|
| Filtration | Solide/Liquide | Membrane poreuse | Simple, économique | Colmatage possible |
| Centrifugation | Solide/Liquide ou émulsions | Force centrifuge | Rapide, efficace | Matériel coûteux |
| Décantation | Liquide/Liquide non miscibles | Différence de densité | Très simple | Lente ; émulsions problématiques |
| Lévigation | Solide/Solide | Courant de liquide | Séparation par densité | Peu précise |
| Évaporation | Solution liquide | Élimination solvant | Concentre le soluté | Risque thermique |
| Précipitation | Solution liquide | ↓ solubilité | Rapide | Risque d’impuretés |
| Relargage | Solution aqueuse | Compétition ionique | Très douce | Nécessite dessalage ultérieur |
Conclusion : L’Essentiel à Retenir pour vos Examens
Les méthodes de séparation sont au cœur de la pratique pharmaceutique. Qu’il s’agisse d’extraire un principe actif d’une plante, de purifier une protéine thérapeutique ou de contrôler la qualité d’un médicament, chaque technique répond à une logique précise.

Les points clés à maîtriser :
- Identifier la nature du mélange avant toute chose (hétérogène vs homogène, phases en présence)
- Adapter la matière filtrante à la nature chimique du milieu (acidité, basicité, solvants organiques)
- Choisir la technique de centrifugation selon la taille des particules à séparer
- Connaître les séries de Hofmeister pour choisir le bon agent relargant
- Préférer les méthodes douces (relargage, évaporation sous vide) pour les molécules biologiques fragiles
📚 Pour aller plus loin : Associez ces méthodes aux techniques chromatographiques (HPLC, CCM, chromatographie sur colonne) et électrophorétiques (PAGE, électrophorèse capillaire) qui en sont le prolongement naturel en chimie analytique moderne.