Les Dispositifs Médicaux : Guide Complet pour les Étudiants en Pharmacie
Introduction : Du Bois à la Nanotechnologie, l’Incroyable Histoire des Implants
Depuis l’Antiquité, l’être humain cherche à réparer son corps lorsqu’un tissu est lésé ou défaillant. Les premières tentatives d’implantation de dents remontent à l’Égypte ancienne et aux cultures précolombiennes : elles étaient sculptées dans l’ivoire ou dans le bois, puis retenues entre elles par des fils d’or. Un savoir-faire artisanal qui, en quelques millénaires, a évolué jusqu’aux nanotechnologies.
Aujourd’hui, le marché mondial des dispositifs médicaux représente 542 milliards de dollars en 2024 et devrait dépasser 886 milliards de dollars d’ici 2032, avec un taux de croissance annuel de 6,5 %. Plus de 2,3 millions de dispositifs médicaux sont enregistrés en circulation dans le monde. Ces chiffres illustrent à quel point la maîtrise de ce domaine est devenue incontournable pour tout professionnel de santé.
Selon la conférence de consensus de Chester (1991), un biomatériau est défini comme :
« Un matériau non vivant, utilisé dans un dispositif médical et conçu pour interagir avec des systèmes biologiques, qu’il participe à la constitution d’un appareillage à visée diagnostique ou à celle d’un substitut de tissu ou d’organe, ou encore à celle d’un dispositif de suppléance (ou assistance) fonctionnelle. »
La première génération de biomatériaux d’origine naturelle a progressivement été remplacée par des implants fabriqués à partir de polymères synthétiques, de céramiques, de métaux et d’alliages métalliques. Ces matériaux entrent en contact direct avec les fluides biologiques et doivent absolument être biocompatibles : ils ne doivent ni activer la cascade du complément, ni modifier la coagulation sanguine, ni induire de réactions inflammatoires délétères.

1. Définition et Périmètre des Dispositifs Médicaux
Qu’est-ce qu’un dispositif médical ?
On entend par dispositif médical tout instrument, appareil, équipement, matière, produit — à l’exception des produits d’origine humaine — ou autre article utilisé seul ou en association, y compris les accessoires et logiciels intervenant dans son fonctionnement.
Il est destiné par le fabricant à être utilisé chez l’homme à des fins :
- De diagnostic, prévention, contrôle, traitement ou atténuation d’une maladie : thermomètre médical, hémodialyseur, stéthoscope…
- De diagnostic, prévention, traitement, atténuation ou compensation d’une blessure ou d’un handicap : pansements, lentilles intraoculaires, fauteuils roulants, sutures résorbables ou non…
- D’étude, remplacement ou modification de l’anatomie ou d’un processus physiologique : pacemaker, prothèse articulaire, colles biologiques, produits de comblement dentaire…
- De maîtrise de la conception : dispositif intra-utérin (DIU), préservatif, diaphragme…
⚠️ Point clé à retenir : tout dispositif médical est susceptible de présenter des dangers pour le patient ou l’utilisateur, directement ou indirectement. C’est pourquoi leur réglementation est stricte.
Ce qui distingue un dispositif médical d’un médicament
Contrairement au médicament, un dispositif médical n’agit pas par voie pharmacologique, immunologique ou métabolique. Il agit principalement par un mécanisme physique ou mécanique. Cette distinction est fondamentale pour le pharmacien, qui joue un rôle clé dans leur dispensation et leur conseil.
2. Classification des Dispositifs Médicaux
Les critères de classification
La classification des dispositifs médicaux repose sur le niveau de risque potentiel pour le patient. Quatre critères principaux sont pris en compte :
- Le caractère invasif ou non invasif
- La durée d’utilisation :
- Temporaire : utilisation continue inférieure à 60 minutes
- Court terme : utilisation continue jusqu’à 30 jours
- Long terme : utilisation continue supérieure à 30 jours
- Le caractère actif (alimenté par une source d’énergie)
- La destination anatomique (orifices naturels, chirurgical, implantable)
Les quatre classes réglementaires
| Classe | Types de dispositifs | Niveau de risque |
|---|---|---|
| Classe I | Dispositifs non invasifs, dispositifs invasifs utilisés moins d’1 heure, dispositifs stériles ou avec fonction de mesurage | Faible → Élevé |
| Classe IIa | Dispositifs invasifs utilisés en continu entre 1h et 30 jours | Modéré |
| Classe IIb | Dispositifs implantables utilisés plus de 30 jours | Élevé |
| Classe III | Dispositifs fabriqués à partir d’un tissu d’origine animale ou associés à un médicament | Très élevé |
💡 Astuce mémo : Plus la classe est élevée, plus les procédures d’évaluation de la conformité sont contraignantes. Un dispositif de classe III (ex : valves cardiaques biologiques) exige une évaluation clinique complète avant sa mise sur le marché.
3. Les Biomatériaux : Cœur de la Conception des Dispositifs Médicaux
Un marché en plein essor
Le secteur des biomatériaux ne cesse de croître, porté par deux tendances majeures :
- Le vieillissement de la population mondiale : les personnes de 65 ans et plus représenteront 22 % de la population mondiale d’ici 2030.
- L’augmentation des traumatismes chez des patients de plus en plus jeunes, nécessitant des prothèses plus résistantes sur le long terme.
On dénombre à travers le monde environ 100 millions de prothèses en service et près de 10 millions de nouvelles prothèses posées par an, toutes constituées de biomatériaux.
Biocompatibilité négative vs bioactivité
Deux notions essentielles à distinguer :
- Biocompatibilité « négative » : l’implant est inerte. Il ne doit pas générer de réaction inflammatoire, de toxicité, ni d’allergie. Exemple : les implants en alumine.
- Biocompatibilité « élargie » ou bioactivité : l’implant n’est plus inerte, il stimule une réponse appropriée des tissus vivants. Exemple : les sutures résorbables, où la réaction inflammatoire participe à la résorption, ou encore les ostéoconducteurs qui facilitent la croissance osseuse.
Les quatre grandes familles de biomatériaux
4. Les Polymères
Polymères fonctionnels
Les polymères fonctionnels ont pour vocation de générer des fonctions chimiques particulières à l’interface matériau/tissu vivant. Ils améliorent l’interaction avec les ostéoblastes (cellules formatrices de l’os) ou les fibroblastes (cellules du tissu conjonctif).
Il est possible d’enrichir leur surface avec des groupements ionisés (orthophosphates, carbonates, carboxylates…) par implantation ionique ou par greffage, afin de modifier leur état de surface et favoriser l’adhésion cellulaire.
Polymères résorbables
Les polymères résorbables ont pour objectif d’être entièrement assimilés par l’organisme :
- Copolymères acide lactique / acide glycolique (PLGA) → utilisés en chirurgie orthopédique traumatologique (vis résorbables, plaques de fixation)
- Polyanhydrides / polyaminoacides → utilisés comme systèmes de libération retardée de médicaments (drug delivery)
🔬 Exemple concret : Les fils de suture résorbables en PGA (acide polyglycolique) sont dégradés en 60 à 90 jours par hydrolyse dans l’organisme. Aucun retrait chirurgical n’est nécessaire.
5. Les Céramiques
Des matériaux aux propriétés proches de l’os humain
Les céramiques sont des biomatériaux plus récents, relativement difficiles à mettre en œuvre en raison de leur haut point de fusion et de leur comportement fragile. Trois types dominent le secteur :
- L’alumine (Al₂O₃) → très dure, utilisée dans les têtes de prothèses de hanche
- La zircone (ZrO₂) → alternative à l’alumine, meilleure résistance aux chocs
- Les céramiques à base de phosphate de calcium → hydroxyapatite (HAP) et phosphate tricalcique β (TCP)
Focus : Hydroxyapatite et phosphate tricalcique
L’HAP et le TCP sont particulièrement intéressants car leurs propriétés se rapprochent au plus près de la matrice minérale de l’os humain. Le tissu osseux représente 65 % de la masse globale d’un individu.
Bien que la formule chimique soit proche de l’HAP, l’agencement spatial diffère : les cristaux d’HAP sont accolés aux fibres de collagène. La principale difficulté est de synthétiser une HAP en maîtrisant la taille de ses pores pour favoriser la colonisation cellulaire.
Des bioverres de Hench et des verres au phosphate peuvent compléter cette famille, en permettant une accroche quasi chimique avec le tissu osseux.
6. Les Matériaux d’Origine Naturelle
Biocompatibles par nature
Ces matériaux sont logiquement biocompatibles puisqu’ils constituent l’organisme ou en sont proches. On distingue deux sous-catégories :
Tissus recyclés :
- Valves porcines (chirurgie cardiaque)
- Carotide de bœuf
- Veine ombilicale
Extraits d’origine naturelle :
- Chitine (polysaccharide extrait des coquilles de crabe) → fils de suture, chirurgie reconstructive, peau artificielle
- Fucanes (extraits des algues marines) → propriétés anticoagulantes
- Cellulose → membranes de dialyse
- Collagène (animal extrait de la peau, ou humain extrait du placenta) → implants oculaires, cosmétologie, peau artificielle
7. Les Métaux et Alliages Métalliques
Propriétés mécaniques et résistance à la corrosion
Les métaux sont les biomatériaux les plus anciens et les plus utilisés en implantologie, grâce à leurs excellentes propriétés mécaniques. En termes de résistance à la corrosion, on les classe dans l’ordre suivant :
Titane > Alliages Co-Cr > Aciers inoxydables
Tableau récapitulatif des matériaux métalliques
| Matériaux | Applications biomédicales | Éléments constitutifs |
|---|---|---|
| Titane et alliages | Prothèses de hanche, vis, implants dentaires | Ti, Al, V |
| Nitinol | Stents, filtres à veine cave, odontologie | Ni, Ti |
| Alliages Co-Cr | Odontologie, prothèses de hanche, valves cardiaques | Co, Cr, Mo, Fe, Ni |
| Aciers inoxydables | Stents, vis et plaques de fixation, pompes, valves | Fe, Cr, Ni, Mn, Mo |
Points forts de chaque famille métallique
Aciers inoxydables :
- Bonne ductilité (capacité à se déformer sans se rompre)
- Structure austénitique → compatible avec l’IRM (non ferromagnétiques)
- Utilisation la plus répandue en raison de leur faible coût
Alliages de cobalt :
- Excellente résistance à l’usure → idéaux pour les prothèses de hanche et valves cardiaques sollicitées en mouvement répété
Alliages de titane :
- Meilleure biocompatibilité : adhésion spontanée de l’os (ostéo-intégration)
- Faible densité : 4,3 g/cm³ (plus léger que l’acier)
- Mémoire de forme avec le Nitinol (Ti + 55 % Ni) → très utile pour les stents, qui se déforment à froid pour l’insertion, puis reprennent leur forme à la température corporelle
⚠️ Limite importante : tous les alliages métalliques présentent un risque de dissolution d’ions métalliques dans le sang (libération de Ni²⁺, Co²⁺, Cr³⁺…). Cela peut entraîner des effets toxiques systémiques à long terme. C’est pourquoi la recherche de nouveaux alliages biopassivants se poursuit activement. Le titane pur et l’alliage CoCrMo forment une couche de passivation protectrice qui limite ce phénomène.
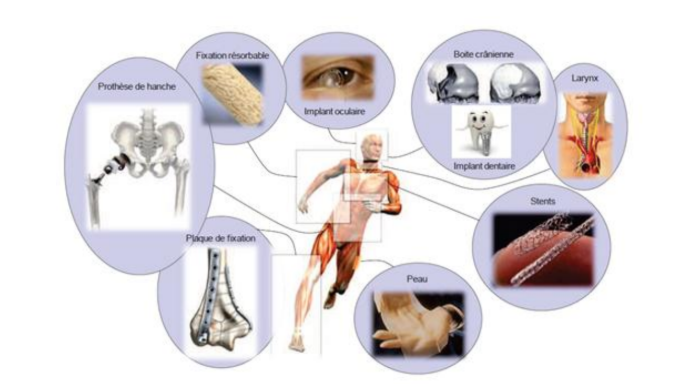
8. Les Prothèses : Applications Cliniques et Mécanismes d’Ancrage
Les trois types de chirurgie
Les prothèses sont présentes dans tout le corps humain et permettent de répondre à trois grands types de besoins chirurgicaux :
- Chirurgie des traumatismes → suite à un accident (fractures, ruptures ligamentaires)
- Chirurgie fonctionnelle → remplacement des parties défectueuses utiles au mouvement (hanche, genou, épaule)
- Chirurgie reconstructrice → amélioration de la qualité de vie des personnes ayant des malformations ou ayant subi une ablation
Les mécanismes d’ancrage à l’os
Selon le biomatériau utilisé, le mode de fixation à l’os diffère :
| Type d’implant | Mécanisme d’ancrage | Exemples de matériaux |
|---|---|---|
| Inerte | Accroche mécanique (fixation morphologique) | Métaux, alumine, zircone, polyéthylène (PE) |
| Poreux | Croissance des tissus dans les pores (fixation biologique) | Hydroxyapatite, métal poreux revêtu d’HA |
| Bioactif | Croissance de l’os à l’interface | Verre bioactif, HA |
| Résorbable | Remplacé progressivement par les tissus | TCP β, acide polylactique (PLA) |
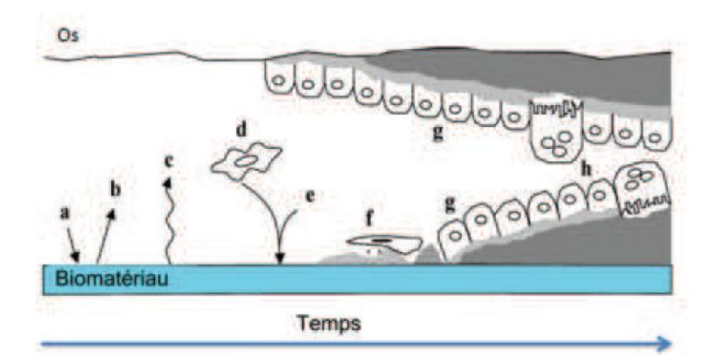
La réaction de l’organisme face à un implant
Lorsque le corps entre en contact avec un corps étranger, une cascade de réactions s’enclenche automatiquement, de la première interaction avec les cellules sanguines jusqu’à la régénération osseuse complète :
- (a) Adsorption des protéines à partir du sang et des fluides corporels
- (b) Désorption des protéines
- (c) Modification de la surface de l’implant
- (d) Réaction inflammatoire
- (e) Formation d’une matrice protéique avec adsorption de protéines spécifiques : BS (Sialoprotéine osseuse) et OPN (Ostéopontine) — qui relie l’HAP aux cellules osseuses
- (f) Formation d’une membrane et adhésion ostéoblastique
- (g) Croissance osseuse côté implant et côté os natif
- (h) Remodelage osseux
🔬 À retenir : les propriétés de surface de l’implant (rugosité, chimie de surface, propriétés mécaniques) sont déterminantes pour la qualité de l’ostéo-intégration. Deux implants identiques en composition mais différents en rugosité n’auront pas la même cinétique d’intégration.
9. Tendances Actuelles et Perspectives pour le Pharmacien
L’essor des technologies connectées et de l’IA
Le secteur des dispositifs médicaux est en pleine mutation. Parmi les innovations majeures à connaître :
- Dispositifs portables intelligents : plus de 18 millions d’unités expédiées en 2024. Un Américain sur trois utilise déjà un dispositif portable pour surveiller sa santé.
- Intelligence artificielle : les outils de dépistage IA en ophtalmologie détectent la rétinopathie diabétique avec une sensibilité de 95 %.
- Chirurgie robotique : les volumes de remplacement articulaire robotique croissent de 35 % par an.
- Dispositifs à mémoire de forme : applications croissantes dans la cardiologie interventionnelle et la neurologie.
Le rôle du pharmacien face aux dispositifs médicaux
Le pharmacien est un acteur central dans la filière des dispositifs médicaux :
- Dispensation et conseil aux patients (pansements, dispositifs orthopédiques, matériel de diabétologie…)
- Vérification de la conformité réglementaire (marquage CE, classe du dispositif)
- Pharmacovigilance et matériovigilance : signalement des incidents liés à un dispositif médical
- Accompagnement à l’observance : éducation thérapeutique pour les utilisateurs de dispositifs complexes (pompes à insuline, CPAP…)

Conclusion : Ce Qu’il Faut Retenir
Les dispositifs médicaux constituent un domaine vaste, à la croisée de la chimie, de la biologie et de l’ingénierie. En tant qu’étudiant en pharmacie, voici les points fondamentaux à maîtriser :
✅ Un dispositif médical agit par mécanisme physique ou mécanique, et non pharmacologique.
✅ La classification en 4 classes (I, IIa, IIb, III) repose sur le niveau de risque et la durée d’utilisation.
✅ Les quatre familles de biomatériaux (polymères, céramiques, matériaux naturels, métaux) ont chacune leurs indications, leurs avantages et leurs limites.
✅ La biocompatibilité — qu’elle soit négative (inertie) ou élargie (bioactivité) — est le critère premier de tout biomatériau.
✅ L’interface biomatériau/tissu vivant est une zone dynamique : la rugosité et la chimie de surface conditionnent l’intégration de l’implant.
✅ Le marché mondial est en forte croissance, porté par le vieillissement démographique et l’innovation technologique : l’IA, les nano-technologies et les matériaux résorbables ouvrent de nouvelles perspectives thérapeutiques.