Méthodes Électrochimiques d’Analyse : Guide Complet pour les Étudiants en Pharmacie
À retenir : Les méthodes électrochimiques sont au cœur du contrôle qualité pharmaceutique. Le marché mondial des tests analytiques pharmaceutiques était estimé à 8,98 milliards USD en 2024 et devrait atteindre 13,43 milliards USD d’ici 2029, témoignant de l’importance croissante de ces techniques dans l’industrie du médicament.
Introduction : Pourquoi les Méthodes Électrochimiques sont Indispensables en Pharmacie
Les méthodes électrochimiques d’analyse occupent une place centrale dans la formation du pharmacien. Elles permettent de doser les principes actifs, de contrôler la qualité des médicaments, et de surveiller les réactions chimiques avec une grande précision.
En laboratoire pharmaceutique, ces techniques sont utilisées quotidiennement pour :
- Le dosage des formes ioniques de médicaments (antibiotiques, anti-inflammatoires, etc.)
- Le contrôle du pH des préparations injectables et des formes liquides orales
- La vérification de la pureté des matières premières
- Le suivi des réactions de synthèse de principes actifs
Dans ce cours, nous aborderons les quatre grandes familles de méthodes électrochimiques : la potentiométrie, l’ampérométrie, la coulométrie et la conductimétrie.

1. Classification des Méthodes Électrochimiques d’Analyse
Les méthodes électrochimiques se divisent en deux grandes catégories selon la quantité d’électricité mise en jeu.
1.1 Méthodes Indicatrices
Ces méthodes ne perturbent pas la composition de la solution : les quantités d’électricité mises en jeu sont très faibles, voire nulles.
À l’état de régime, les variables sont l’intensité du courant (i), le potentiel (E) et les concentrations (C), reliées par la relation f(i, E, C) = 0.
Deux sous-catégories en découlent :
- Potentiométrie : on fixe l’intensité et on mesure le potentiel → E = f(C)
- Ampérométrie : on fixe le potentiel et on mesure l’intensité → i = f(C)
En régime transitoire, le temps devient une variable supplémentaire. Ces méthodes provoquent un régime variable, utile pour des mesures dynamiques plus complexes.
1.2 Méthodes Coulométriques
La coulométrie met en jeu la totalité du corps à doser dans une réaction électrochimique. La mesure de la quantité d’électricité consommée permet de calculer précisément la quantité de substance électrolysée.
1.3 Méthodes Variées
La conductimétrie mesure la conductance de la solution. Les réactions électrochimiques ne constituent pas ici le phénomène principal : c’est la conductivité ionique globale qui est exploitée.

2. Potentiométrie
2.1 Principe Général
La potentiométrie regroupe toutes les méthodes analytiques basées sur la mesure d’un potentiel électrique. Elle permet de :
- Déterminer des paramètres thermodynamiques (constantes de complexation, produits de solubilité)
- Contrôler une fabrication industrielle en temps réel
- Identifier le point équivalent d’un titrage avec précision
Le potentiel mesuré par une cellule électrochimique est donné par :
U = Eᵢnd − Eᵣéf + Eⱼ
Où :
- Eᵢnd = potentiel de l’électrode indicatrice
- Eᵣéf = potentiel de l’électrode de référence
- Eⱼ = potentiel de jonction (différence de potentiel à l’interface entre deux solutions d’électrolytes de compositions différentes)
⚠️ Point clé pour l’examen : Le potentiel de jonction Eⱼ ne peut pas être calculé théoriquement. Il est impératif d’étalonner les électrodes expérimentalement avec des solutions tampons avant toute mesure.
Pour un cation Xⁿ+ à 25 °C, la réponse de l’électrode suit la loi de Nernst :
Eᵢnd = L + (0,06 / n) × log(aₓ)
En combinant avec l’équation de la cellule, on obtient la relation générale :
- Pour les cations : U = K − (0,06/n) × Px
- Pour les anions : U = K + (0,06/n) × PA
Où n est la valeur absolue de la charge de l’ion.
2.2 Mesure Potentiométrique du pH
La mesure du pH est l’application la plus courante de la potentiométrie en pharmacie. Elle est indispensable pour le contrôle des formes injectables, des collyres, des sirops, et de nombreuses autres préparations.
Protocole d’étalonnage :
Lors de l’étalonnage avec une solution tampon, la relation est :
pH_Étalon = (U_Étalon − K) / 0,06
Pour la solution inconnue :
pHᵢ = (Uᵢ − K) / 0,06
En soustrayant les deux équations, on obtient la définition opérationnelle du pH, adoptée mondialement :
pHᵢ = pHₑ − (Uᵢ − Uₑ) / 0,06
💊 Application pharmaceutique : Le pH d’une solution injectable doit être très proche de 7,4 (pH physiologique du sang). Une variation de ±0,5 unités peut provoquer douleur, hémolyse ou précipitation du principe actif. La potentiométrie est la méthode de référence pour ce contrôle qualité.

2.3 Titrages Potentiométriques
Un titrage potentiométrique mesure le potentiel d’une électrode indicatrice en fonction du volume de titrant ajouté, à intensité nulle ou quasi-nulle.
Avantages par rapport aux indicateurs colorés :
- Mesure plus fiable et objective
- Utilisable sur des solutions colorées ou troubles
- Permet de doser des mélanges complexes
Trois méthodes de détection du point équivalent :
- Méthode directe : On repère le point d’inflexion de la courbe E = f(V)
- Première dérivée (ΔE/ΔV) : Le point équivalent correspond au maximum de cette courbe
- Seconde dérivée (ΔE²/ΔV²) : Le changement de signe indique le point équivalent avec précision — méthode utilisée dans les titrateurs automatiques modernes
2.4 Titrage Potentiométrique par Précipitation
Exemple classique : dosage des ions chlorure par les ions argent (argentimétrie)
Le potentiel de l’électrode d’argent est calculé selon l’espèce en excès :
- En présence d’excès de Cl⁻ : E = 0,222 − 0,06 × log[Cl⁻]
- En présence d’excès d’Ag⁺ : E = 0,799 + 0,06 × log[Ag⁺]
💊 Application pharmaceutique : Cette méthode est utilisée pour doser les chlorures dans les solutions de NaCl à 0,9 % (sérum physiologique) et dans les solutions de Ringer, deux médicaments injectables de première importance.
2.5 Titrages par Formation de Complexes
Des électrodes métalliques ou à membrane permettent de détecter le point équivalent des titrages faisant intervenir la formation de complexes. Cette technique est utilisée notamment avec l’EDTA pour le dosage des ions métalliques.
2.6 Titrages Acido-Basiques
Les titrages potentiométriques sont particulièrement utiles pour :
- Doser les acides polyfonctionnels (ex : acide citrique, acide tartrique — excipients courants)
- Analyser les mélanges d’acides ou de bases
- Déterminer les constantes de dissociation pKa
Détermination du pKa :
Au point de demi-équivalence, les concentrations [HA] = [A⁻], donc :
Ka = [H₃O⁺] et pH = pKa
⚗️ Remarque importante : L’utilisation des concentrations au lieu des activités peut entraîner une erreur sur Ka d’un facteur 2 ou plus. L’expression rigoureuse fait intervenir les coefficients d’activité γ (delta) :
Ka = (aₕ₃O⁺ × γₐ⁻) / γₕA
2.7 Titrages d’Oxydoréduction
On utilise une électrode indicatrice inerte (platine, or, palladium, mercure) pour détecter les points équivalents des réactions rédox. Les courbes obtenues sont similaires à celles des autres titrages potentiométriques.
💊 Application pharmaceutique : Le dosage de la vitamine C (acide ascorbique) dans les préparations pharmaceutiques repose fréquemment sur des titrages d’oxydoréduction suivis potentiométriquement.
3. Ampérométrie
3.1 Principe
L’ampérométrie suit les variations de concentration de la substance dosée en mesurant l’intensité du courant aux électrodes, à potentiel fixé. Le point équivalent correspond à un point singulier (minimum, maximum ou rupture de pente) de la courbe i = f(V).
3.2 Types de Systèmes Électrodes
Il existe deux types de montages :
- Une électrode indicatrice + une électrode de référence : le plus courant
- Deux électrodes indicatrices (identiques ou différentes) avec tension constante imposée
3.3 Exemple Pratique : Dosage du Plomb par les Ions Sulfate
Réaction : Pb²⁺ + SO₄²⁻ → PbSO₄↓
Le plomb est l’espèce électroactive ; les ions sulfate ne le sont pas dans ces conditions.
Au fur et à mesure de l’addition de SO₄²⁻ :
- La concentration en Pb²⁺ diminue progressivement
- Le courant diminue proportionnellement (i ∝ [Pb²⁺])
- Au point équivalent : [Pb²⁺] = 0, donc i = 0
Ce point est facile à détecter et correspond à la fin de la réaction.
3.4 Allures des Courbes de Titrage Ampérométrique
Trois cas principaux :
- (a) L’analyte est réduit, le réactif ne l’est pas → la courbe décroît jusqu’au point équivalent, puis reste plate
- (b) Le réactif est réduit, l’analyte ne l’est pas → la courbe est plate jusqu’au point équivalent, puis croît
- (c) Les deux espèces sont réduites → courbe en V avec un minimum au point équivalent
3.5 Avantages de la Technique Ampérométrique
- Rapidité d’exécution
- Adapté aux solutions très diluées (impossibles à titrer par voie classique)
- Tolérance aux espèces étrangères en grande quantité, à condition qu’elles ne soient pas électroactives au potentiel imposé
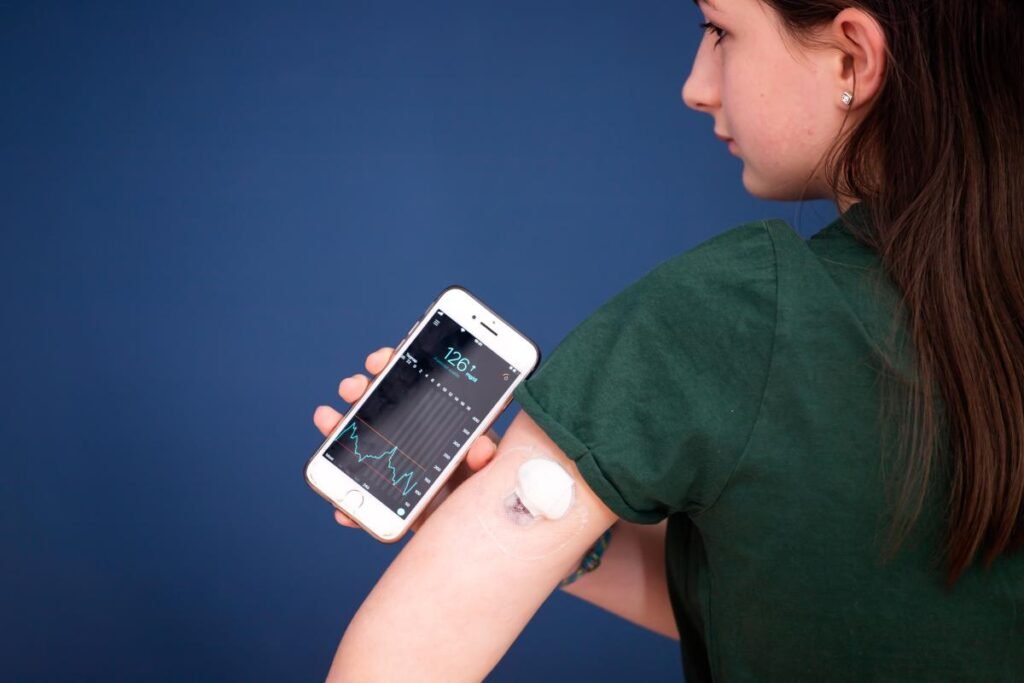
💊 Application pharmaceutique : Les glucomètres utilisés par les patients diabétiques reposent sur un principe ampérométrique : une enzyme (glucose oxydase) convertit le glucose en signal électrique proportionnel à sa concentration. Ce biocapteur électrochimique est l’un des plus utilisés au monde.
4. Coulométrie
4.1 Principe Général
Les méthodes coulométriques mesurent la quantité d’électricité (charge) nécessaire pour modifier quantitativement l’état d’oxydation de l’analyte.
Unités fondamentales :
- Le Coulomb (C) : charge transportée par 1 ampère pendant 1 seconde → Q = i × t
- Le Faraday (F) = 96 500 C = quantité d’électricité correspondant à 1 mole d’électrons
Pour un courant variable :
Q = ∫₀ᵗ i dt
Exemple de calcul :
Pour la réaction : Fe³⁺ + 1e⁻ → Fe²⁺
Un courant de 10⁻³ A pendant 100 secondes met en jeu 0,1 coulombs, ce qui correspond à 57,8 μg d’ions Fe³⁺ consommés.
4.2 Coulométrie à Potentiel Contrôlé
Le potentiel de travail est maintenu constant de façon à ce que seul l’analyte contribue au transfert de charges. L’intensité, initialement élevée, décroît exponentiellement au cours du temps jusqu’à atteindre zéro.
La quantité de substance oxydée (en moles) = Q / (n × F)
Applications :
- Dosage et synthèse électrolytique de composés organiques (ex : acide trichloracétique)
- Dépôt d’environ 25 métaux différents sur électrode de mercure (cathode la plus utilisée)
4.3 Coulométrie à Intensité Constante
Cette méthode est utilisée quand le corps à électrolyser est à l’état solide sur l’électrode (métal, oxyde, sel insoluble).
Elle est particulièrement adaptée pour :
- Les dosages en retour (dépôt connu, consommation partielle par l’analyte, dosage du restant)
- L’analyse des revêtements métalliques, couches d’oxydes et films minces
4.4 Titrages Coulométriques
Principe : Un réactif A est produit électrochimiquement à partir d’un précurseur C, puis réagit avec le corps B à doser :
C + e⁻ → A et B + A → AB
Le rendement de conversion doit être de 100 % (condition impérative).
Analogie avec la volumétrie :
| Volumétrie | Coulométrie |
|---|---|
| Volume de titrant | Temps d’électrolyse |
| Titre de la solution | Valeur précise de l’intensité |
| Robinet de burette | Interrupteur du circuit |
Applications des titrages coulométriques :
- Réactions acido-basiques :
- Réduction de l’eau : 2H₂O + 2e⁻ → 2OH⁻ + H₂(g) → dosage des acides (acidimétrie)
- Oxydation de l’eau : 2H₂O → O₂(g) + 4H⁺ + 4e⁻ → dosage des bases (alcalinimétrie)
- Réaction de complexation avec l’EDTA :
- On prépare Hg²⁺ par oxydation d’une électrode de mercure, qui réagit ensuite avec l’EDTA (Y⁴⁻) :
- Hg↓ + Y⁴⁻ → HgY²⁻ + 2e⁻
💊 Application pharmaceutique : Les titrages coulométriques sont utilisés pour contrôler la concentration en principes actifs des formes injectables avec une très grande précision, notamment pour les médicaments à index thérapeutique étroit (digoxine, lithium, aminosides).
5. Conductimétrie
5.1 Conduction de l’Électricité dans les Solutions
Une solution contenant des ions est appelée solution électrolytique. En l’absence d’ions, un liquide est pratiquement isolant.
Quand on plonge deux électrodes dans une solution électrolytique et qu’on applique une tension :
- Les cations migrent vers le pôle négatif (cathode)
- Les anions migrent vers le pôle positif (anode)
5.2 Définition et Mesure de la Conductance
En appliquant une tension alternative sinusoïdale de valeur U entre deux électrodes, la solution est parcourue par un courant I proportionnel à U :
I = G × U
G est la conductance de la solution, exprimée en Siemens (S).
La résistance R est l’inverse de la conductance : R = 1/G (exprimée en Ohm, Ω).
Montage de mesure :
Le circuit comprend :
- Un générateur basse fréquence (GBF) délivrant une tension sinusoïdale
- Un voltmètre mesurant la tension U aux bornes de la cellule
- Un ampèremètre mesurant l’intensité I
⚠️ Remarque technique : On utilise une tension alternative de fréquence suffisamment élevée pour éviter des dépôts parasites (électrolyse) sur les électrodes.
5.3 Conductivité Ionique
La conductivité d’une solution est la somme des contributions de chaque ion présent :
σ = Σ λₐ × zₐ × Cₐ
Où λₐ est la conductivité molaire ionique de l’ion A (caractéristique de chaque espèce).
Tableau des conductivités molaires ioniques à 25 °C (S.m².mol⁻¹.10⁻⁴) :
| Cation | λ | Anion | λ |
|---|---|---|---|
| H⁺ | 349,8 | OH⁻ | 197,6 |
| Ag⁺ | 61,9 | Cl⁻ | 76,3 |
| Na⁺ | 50,1 | F⁻ | 55,4 |
| Fe²⁺ | 53 | I⁻ | 77 |
| Fe³⁺ | 68 | ClO₄⁻ | 67,4 |
📌 À noter : H⁺ et OH⁻ ont des conductivités molaires beaucoup plus élevées que les autres ions, car ils se déplacent par un mécanisme de transfert de proton (mécanisme de Grotthuss), plus rapide que la migration ionique classique.
La conductance G est reliée à la conductivité σ par la constante de cellule k = l/S :
G = k × σ = k × Σ λₐ × zₐ × Cₐ
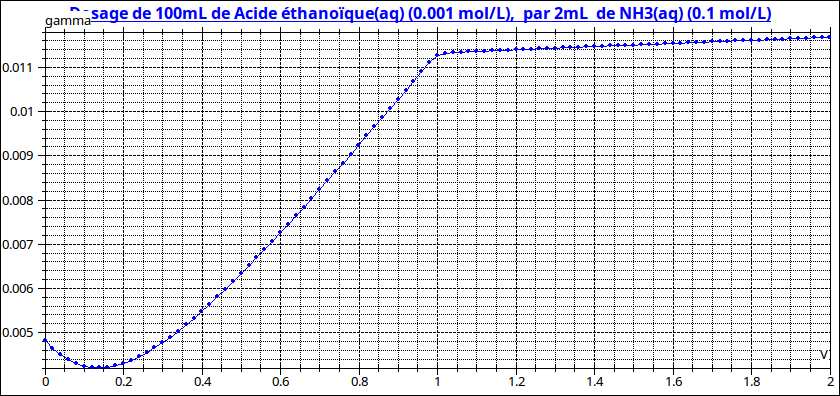
5.4 Titrages Conductométriques
La courbe de titrage conductométrique est généralement formée de branches de droites qui se croisent au point équivalent.
Exemple : Dosage d’HCl par NaOH
Avant le point équivalent :
- H⁺ (λ = 349,8) est remplacé par Na⁺ (λ = 50,1)
- La conductivité diminue (on perd des ions très mobiles)
Après le point équivalent :
- La soude ajoutée apporte Na⁺ (λ = 50,1) et OH⁻ (λ = 197,6)
- La conductivité augmente
Résultat : courbe en V avec un minimum au point équivalent.
5.5 Domaines d’Application et Limites
Avantages :
- Compatible avec tous types de réactions (acido-basique, rédox, complexation, précipitation, échange d’ions) à condition que des ions soient impliqués
- Utilisable jusqu’à des concentrations de 10⁻⁴ M (milieu dilué)
Inconvénient majeur :
- Tous les ions présents contribuent à la conductivité. En présence d’une forte concentration d’ions étrangers, les variations relatives de conductivité dues au titrage deviennent trop faibles pour être détectées avec précision (erreur relative des appareils courants : ~0,5 %)
💊 Application pharmaceutique : La conductimétrie est utilisée pour contrôler la pureté de l’eau purifiée et de l’eau pour préparations injectables (eau PPI), deux excipients fondamentaux en pharmacie. La Pharmacopée Européenne impose des limites strictes de conductivité pour ces eaux.
6. Comparatif des Méthodes Électrochimiques
| Méthode | Grandeur mesurée | Point fort | Application pharm. typique |
|---|---|---|---|
| Potentiométrie | Potentiel (E) | Précision, universalité | Mesure du pH, titrages |
| Ampérométrie | Intensité (i) | Sensibilité, rapidité | Capteurs enzymatiques, glucomètre |
| Coulométrie | Charge (Q) | Haute précision absolue | Dosage formes injectables |
| Conductimétrie | Conductance (G) | Contrôle de l’eau | Eau PPI, eaux pharmaceutiques |
7. Perspectives Modernes : Les Biocapteurs Électrochimiques
Les méthodes électrochimiques connaissent une révolution technologique avec le développement des biocapteurs. Ces dispositifs associent un élément biologique reconnaissant (enzyme, anticorps, ADN) à un transducteur électrochimique.
Des électrodes modifiées par des cyclodextrines permettent désormais la détermination simultanée de l’acide ascorbique et de l’acide urique dans des produits pharmaceutiques et des échantillons biologiques.
Des capteurs portables basés sur la nanotechnologie sont en cours de développement pour améliorer la sensibilité et la spécificité de la détection des principes actifs, en particulier pour les produits pharmaceutiques et nutraceutiques.
Ces avancées ouvrent la voie à des analyses plus rapides, plus sensibles et réalisables directement en dehors du laboratoire — une tendance majeure pour le pharmacien de demain.
Conclusion et Points Clés à Retenir
Les méthodes électrochimiques constituent un arsenal analytique puissant et polyvalent, indispensable au pharmacien analyste. Voici les points essentiels à maîtriser :
- La potentiométrie est fondée sur la mesure d’un potentiel à courant nul. L’étalonnage préalable est obligatoire. La définition opérationnelle du pH dérive directement de cette méthode.
- L’ampérométrie mesure l’intensité à potentiel fixé. Le courant est proportionnel à la concentration de l’espèce électroactive. Application directe : le glucomètre.
- La coulométrie exploite la loi de Faraday (Q = n × F × N). Elle garantit une précision absolue quand le rendement de conversion est de 100 %.
- La conductimétrie mesure la conductance globale de la solution. Elle est idéale pour le contrôle de la qualité de l’eau pharmaceutique, mais sensible aux interférences ioniques.

📚 Pour aller plus loin : Consultez les monographies de la Pharmacopée Européenne sur les méthodes électrochimiques (chapitre 2.2 : Méthodes de détermination physico-chimiques) pour voir comment ces techniques sont standardisées et appliquées au contrôle officiel des médicaments.



