Méthodes Électrochimiques : Guide Complet des Électrodes, Courbes et Phénomènes de Transport
L’électrochimie est l’une des disciplines scientifiques les plus stratégiques du XXIe siècle. Entre le développement des batteries pour véhicules électriques, la surveillance de la qualité de l’eau et le dosage médical en temps réel, ses applications transforment notre quotidien. Ce guide détaillé vous accompagne pas à pas dans la compréhension des méthodes électrochimiques : des fondamentaux aux applications analytiques modernes.
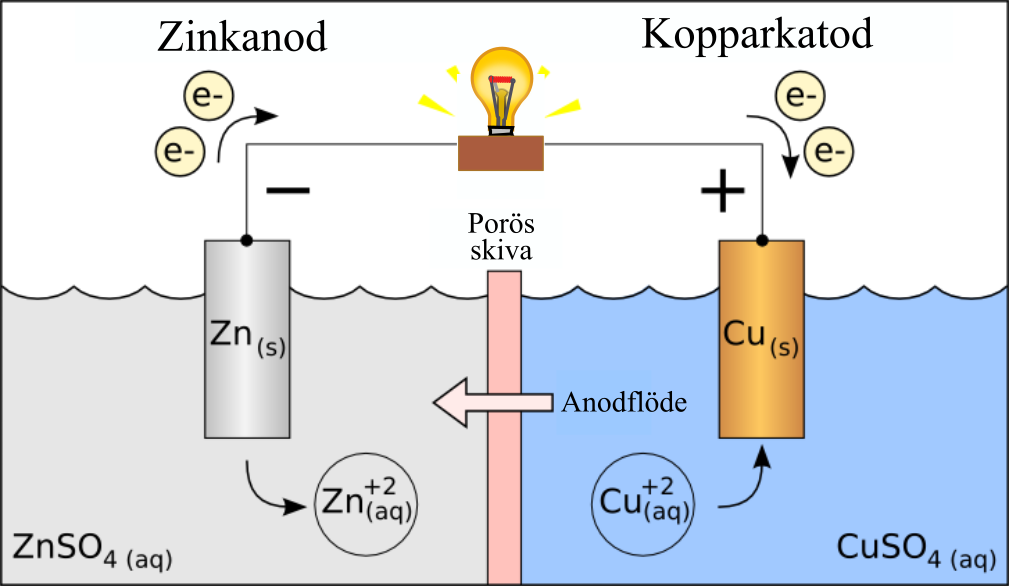
Pourquoi l’Électrochimie est-elle Incontournable Aujourd’hui ?
L’électrochimie étudie les relations entre les transformations chimiques et le passage du courant électrique. Son champ d’application est immense :
- Production d’énergie : piles, accumulateurs, batteries lithium-ion
- Électrolyse industrielle : fabrication de l’aluminium (~24 Mt/an), du chlore et de la soude (~40 Mt/an)
- Analyse chimique : détection et dosage d’espèces en solution
- Traitement de surface : protection contre la corrosion, galvanoplastie
- Applications biomédicales : capteurs de glycémie, biosenseurs
Le marché mondial des appareils électrochimiques était valorisé à 12,5 milliards de dollars en 2024 et devrait atteindre 20,8 milliards de dollars d’ici 2033, avec un taux de croissance annuel de 7,5 %. Cette expansion est portée par les besoins croissants en stockage d’énergie propre, en surveillance environnementale et en diagnostics médicaux précis.
L’étude des réactions électrochimiques fait appel à plusieurs domaines de la chimie et de la physique : thermodynamique, cinétique, phénomènes de transport, électricité et hydrodynamique. Ce guide introduit les notions fondamentales indispensables : oxydant, réducteur, électrode, cellule et potentiel électrochimique.
1. Les Électrodes : Définition et Classification
Une électrode est une pièce conductrice (généralement un métal) reliée à un pôle d’un appareil électrique et plongeant dans une solution électrolytique. Elle est le siège des réactions d’oxydation et de réduction.
Dans les montages électrochimiques, on distingue deux grandes catégories d’électrodes :
- Les électrodes de référence — potentiel fixe et connu
- Les électrodes indicatrices (ou spécifiques) — potentiel variable, fonction de l’analyte
2. Les Électrodes de Référence
Une électrode de référence est une demi-cellule dont le potentiel est stable, reproductible et indépendant de la composition de la solution analysée. Elle sert de point de comparaison pour mesurer le potentiel de l’électrode indicatrice.
2.1 L’Électrode Normale à Hydrogène (ENH ou ESH)
L’ENH est l’électrode de référence absolue, universellement adoptée comme zéro de l’échelle des potentiels. Elle met en jeu le couple redox H⁺(aq) / H₂(g).
Potentiel standard : E°(H⁺/H₂) = 0,00 V
En pratique, cette électrode est difficile à manipuler en laboratoire courant, car elle nécessite un flux continu de dihydrogène pur. On lui préfère donc des électrodes de référence secondaires plus commodes.
2.2 L’Électrode au Calomel Saturé (ECS)
C’est l’électrode de référence la plus utilisée en laboratoire analytique. Elle repose sur le couple mercure / chlorure mercureux :
Réaction : Hg₂Cl₂(s) + 2e⁻ → 2 Hg(l) + 2 Cl⁻
Trois concentrations en KCl sont couramment employées :
| Concentration KCl | Potentiel vs ENH (25°C) |
|---|---|
| 0,1 M | + 0,334 V |
| 1 M | + 0,281 V |
| Saturé (~4,6 M) | + 0,2444 V |
L’ECS au KCl saturé est la plus répandue en raison de sa simplicité de préparation et de sa stabilité.
2.3 L’Électrode Argent / Chlorure d’Argent (Ag/AgCl)
Cette électrode constitue une excellente alternative à l’ECS. Un fil d’argent plonge dans une solution saturée en KCl et en AgCl.
Demi-réaction : AgCl(s) + e⁻ → Ag(s) + Cl⁻
Potentiel : E = +0,222 V vs ENH à 25°C
Ses avantages : elle est non toxique (contrairement au mercure), miniaturisable, et très utilisée dans les électrodes combinées pour la mesure du pH.
3. Les Électrodes Indicatrices
Une électrode indicatrice est une demi-cellule dont le potentiel varie de manière prédictible en fonction de l’activité de l’espèce chimique à analyser (l’analyte).
3.1 Électrodes Métalliques
On distingue trois espèces d’électrodes métalliques selon leur mode de fonctionnement.
Électrodes de Première Espèce
Il s’agit d’un métal en contact direct avec l’un de ses ions en solution. Le potentiel obéit à l’équation de Nernst.
Exemple — Électrode d’argent :
Ag⁺ + e⁻ → Ag : E = E°(Ag⁺/Ag) + 0,06 × log[Ag⁺]
Ou encore, en termes de fonction pAg :
E = E°(Ag⁺/Ag) − 0,06 × pAg
Cette électrode est idéale pour suivre les titrages par précipitation (ex. : Ag⁺ + Cl⁻ → AgCl↓) ou par complexation.
Précaution importante : certains métaux comme le cuivre, le zinc ou le cadmium se dissolvent en milieu acide ; d’autres comme le fer, le nickel ou le chrome donnent des résultats non reproductibles en raison de leur oxydation superficielle.
Électrodes de Deuxième Espèce
Un métal est en contact avec l’un de ses sels peu solubles et un anion commun. C’est le cas de l’électrode Ag/AgCl en présence d’ions chlorure.
Équation de Nernst :
E = 0,222 + 0,06 × pCl
Cette électrode est utilisée comme indicatrice de l’ion chlorure dans les titrages de précipitation, et simultanément comme électrode de référence interne dans les systèmes combinés.
Électrodes de Troisième Espèce (Électrodes Redox)
Il s’agit d’un métal inerte (platine, or, carbone vitreux) plongeant dans une solution contenant les deux formes d’un même couple redox.
Exemple — Fil de platine dans une solution de Fe³⁺/Fe²⁺ :
E = E°(Fe³⁺/Fe²⁺) + 0,06 × log([Fe³⁺]/[Fe²⁺])
Ce type d’électrode permet de suivre l’évolution d’un couple redox au cours d’un titrage, notamment pour déterminer le point d’équivalence.
3.2 Électrodes à Membrane (Électrodes Sélectives d’Ions)
Les électrodes sélectives d’ions (ESI) sont des capteurs électrochimiques qui répondent sélectivement à une seule espèce ionique. Leur élément clé est une membrane sélective qui sépare la solution d’analyte de la solution interne de référence.
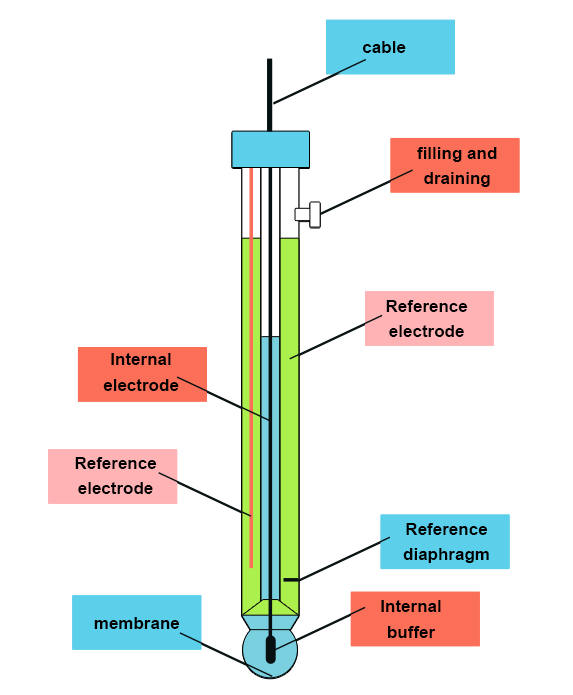
Électrode à Membrane de Verre (Mesure du pH)
C’est l’application la plus répandue des ESI. Le système complet comprend :
- Une électrode de verre (indicatrice)
- Une électrode de référence externe (ECS)
- Une référence interne intégrée (Ag/AgCl)
La membrane de verre est composée de : 72 % SiO₂ + 22 % Na₂O + 6 % CaO (verre Corning 015). Cette composition assure des mesures reproductibles pour des pH inférieurs à 9.
Le potentiel mesuré est uniquement celui de la membrane :
Eₘ = E₁ − E₂
Où E₁ et E₂ sont les potentiels aux deux faces de la membrane. Ce potentiel est directement lié au pH de la solution selon une relation linéaire (pente théorique de −59,2 mV/unité pH à 25°C).
Électrode à Membrane Liquide (Ex. : Ion Calcium)
Dans ce type d’électrode, la sélectivité est assurée par un échangeur d’ions liquide incorporé dans la membrane. Ce système crée des liaisons sélectives avec l’ion cible.
Composition :
- Membrane conductrice sélective aux ions Ca²⁺
- Solution interne de concentration fixe en CaCl₂
- Électrode de référence interne (Ag/AgCl)
Ces électrodes ont été développées pour le dosage potentiométrique direct de nombreux cations polyvalents (Ca²⁺, Mg²⁺, Pb²⁺…) et de certains anions (NO₃⁻, Cl⁻…).
Bon à savoir : Il existe des électrodes combinées qui intègrent l’électrode indicatrice et l’électrode de référence dans un même corps. Elles simplifient considérablement la mise en œuvre, en particulier pour la mesure du pH dans les laboratoires industriels et les analyses de terrain.
4. Les Courbes Intensité-Potentiel (Courbes de Polarisation)
4.1 Principe
Un système électrochimique est constitué d’un couple redox et d’une électrode. À la surface de l’électrode se produit la réaction :
Ox + ne⁻ ⇌ Red
À l’équilibre, le potentiel est donné par l’équation de Nernst :
E_éq = E° + (0,06/n) × log(aₒx / aᵣed)
Lorsqu’on impose un potentiel E différent de E_éq :
- Si E > E_éq : oxydation de Red (courant anodique, I > 0)
- Si E < E_éq : réduction de Ox (courant cathodique, I < 0)
La surtension est définie par : η = E − E_éq
La vitesse de la réaction électrochimique est proportionnelle au courant :
|I| = n × F × v
Où F est la constante de Faraday (96 485 C/mol).
4.2 Systèmes Rapides et Systèmes Lents
Le comportement d’un système électrochimique dépend de sa cinétique de transfert de charges.
Systèmes rapides : Une faible variation de potentiel autour de E_éq provoque un courant d’intensité importante. La réaction est quasi-instantanée.
- Exemples : Cu²⁺/Cu, Fe³⁺/Fe²⁺ sur platine
Systèmes lents : Une surtension importante est nécessaire pour déclencher une réaction notable. L’intensité reste pratiquement nulle sur une large plage de tension autour de l’équilibre.
- Exemples : H⁺/H₂ et O₂/H₂O (systèmes de l’eau sur toutes les électrodes courantes)
Application pratique : la lenteur cinétique des systèmes de l’eau définit une fenêtre d’électroactivité — une plage de potentiels dans laquelle on peut travailler sans que l’eau soit réduite ou oxydée. C’est à l’intérieur de cette fenêtre que l’on détecte et dose les analytes.
4.3 Le Palier de Diffusion
Quand le transfert de matière devient le facteur limitant (et non plus le transfert de charges), la courbe intensité-potentiel présente un plateau horizontal appelé palier de diffusion.
Caractéristiques importantes :
- L’intensité du palier est proportionnelle à la concentration du réactif
- Elle est aussi proportionnelle au nombre d’électrons échangés n
- C’est la base des méthodes voltamétriques quantitatives (polarographie, voltampérométrie)
5. Les Phénomènes de Transport en Électrochimie
Toute réaction électrochimique combine deux types de phénomènes :
5.1 Le Transfert de Matière (TM)
L’alimentation de l’électrode en réactifs (et l’évacuation des produits) s’effectue par trois mécanismes :
- La migration : déplacement des ions sous l’effet d’un champ électrique. Elle est réduite par l’ajout d’un électrolyte support en excès.
- La diffusion : déplacement des espèces des zones concentrées vers les zones diluées, suivant la loi de Fick. C’est le mécanisme dominant dans les expériences voltamétriques.
- La convection : transport mécanique par agitation forcée (agitateur magnétique, électrode tournante). Elle est utilisée pour accélérer le renouvellement de l’interface et atteindre un régime stationnaire.
5.2 Le Transfert de Charges (TC)
Il correspond à l’échange d’électrons à la surface de l’électrode. Sa cinétique dépend de la surtension appliquée et est décrite par la loi de Butler-Volmer.
En pratique, dans la plupart des expériences analytiques, on minimise la migration (par électrolyte support) et on contrôle la convection, de sorte que la diffusion soit le seul facteur limitant. Cela permet de relier directement l’intensité du courant à la concentration de l’analyte.
6. Applications Pratiques des Méthodes Électrochimiques
Les méthodes électrochimiques trouvent des applications dans de nombreux secteurs :
Santé et biomédical :
- Mesure de la glycémie (capteur ampérométrique à glucose)
- Dosage de médicaments dans le sang
- Détection de biomarqueurs (troponine, hormones)
Environnement :
- Mesure du pH et de la conductivité des eaux
- Dosage des métaux lourds (plomb, cadmium, arsenic) par voltampérométrie de redissolution
- Surveillance des polluants organiques
Industrie alimentaire et pharmaceutique :
- Contrôle de la teneur en sel (potentiométrie à l’ion chlorure)
- Dosage de vitamines et antioxydants
- Vérification de la pureté des principes actifs
Énergie et matériaux :
- Caractérisation des électrolytes de batteries
- Études de corrosion sur aciers et alliages
- Développement de nouveaux matériaux d’électrodes pour supercondensateurs
Chiffre clé : Plus de 62,7 % des laboratoires de recherche avancée ont aujourd’hui adopté des postes de travail électrochimiques pour leurs analyses de haute précision, et l’intégration de l’intelligence artificielle dans ces équipements a progressé de 21,8 % en 2024 (Business Research Insights, 2026).
Conclusion : Maîtriser les Méthodes Électrochimiques, un Atout Majeur
Les méthodes électrochimiques constituent un outil analytique puissant, précis et polyvalent. Leur compréhension repose sur trois piliers fondamentaux :
- Le choix des électrodes — référence et indicatrice — adapté à l’analyte visé
- L’interprétation des courbes intensité-potentiel — pour identifier les systèmes rapides/lents et les paliers de diffusion
- La maîtrise des phénomènes de transport — pour relier le courant mesuré à la concentration de l’espèce analysée
Dans un contexte où les marchés de l’énergie propre, de la santé connectée et de la surveillance environnementale sont en pleine expansion, la maîtrise de ces méthodes représente une compétence clé pour tout chimiste, ingénieur ou chercheur.